Ruthenistan tetrapropylamonný
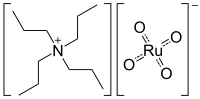
Ruthenistan tetrapropylamonný (zkráceně TPAP nebo TPAPR) je chemická sloučenina se vzorcem N(C3H7)4RuO4, používaná v organické syntéze. Jedná se o sůl tetrapropylamonného kationtu s ruthenistanovým aniontem, RuO -
4 .
| Ruthenistan tetrapropylamonný | |
|---|---|
 | |
| Obecné | |
| Systematický název | ruthenistan tetrapropylamonný |
| Funkční vzorec | (CH3CH2CH2)4N+RuO - 4 |
| Sumární vzorec | C12H28NRuO4 |
| Vzhled | zelená pevná látka |
| Identifikace | |
| Registrační číslo CAS | 114615-82-6 |
| PubChem | 127020979 |
| SMILES | CCC[N+](CCC)(CCC)CCC.O=[Ru](=O)([O-])=O |
| InChI | InChI=1/C12H28N.4O.Ru/c1-5-9-13(10-6-2,11-7-3)12-8-4;;;;;/h5-12H2,1-4H3;;;;;/q+1;;;;-1;/rC12H28N.O4Ru/c1-5-9-13(10-6-2,11-7-3)12-8-4;1-5(2,3)4/h5-12H2,1-4H3;/q+1;-1 |
| Vlastnosti | |
| Molární hmotnost | 351,43 g/mol |
| Teplota rozkladu | 160 °C (433 K) |
| Bezpečnost | |
| [1] | |
| H-věty | H272 H315 H319 H335[1] |
| P-věty | P210 P220 P221 P261 P264 P271 P280 P302+352 P304+340 P305+351+338 P312 P321 P332+313 P337+313 P362 P370+378 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Použití
Oxid rutheničelý je velmi silným oxidačním činidlem, TPAP, jeho jednoelektronově redukovaný derivát, je mírnější. Primární alkoholy oxiduje na aldehydy,[2] sekundární alkoholy se pak přeměňují na ketony.[3]
Při použití většího množství katalyzátoru a kooxidantu a přidání dvou ekvivalentů vody lze primární alkoholy oxidovat až na karboxylové kyseliny. V tomto případě se vytváří hydrát geminálního diolu, který se poté znovu oxiduje.[4]
Vodu vznikající při oxidaci je možné odstranit pomocí molekulárních sít. TPAP je nákladný, ovšem postačuje použití katalytických množství. Průběh katalytického cyklu zajišťuje stechiometrický kooxidant, jako například N-methylmorfolin-N-oxid[5] nebo molekulární kyslík.[6]

TPAP se také používá ke štěpení vicinálních diolů na aldehydy.[3]
Reference
V tomto článku byl použit překlad textu z článku Tetrapropylammonium perruthenate na anglické Wikipedii.
Externí odkazy
 Obrázky, zvuky či videa k tématu Ruthenistan tetrapropylamonný na Wikimedia Commons
Obrázky, zvuky či videa k tématu Ruthenistan tetrapropylamonný na Wikimedia Commons


