Thioestery
Thioestery jsou organické sloučeniny obsahující funkční skupiny s obecným vzorcem R–S–CO–R', jedná se o analogy karboxylátových esterů, u kterých je atom kyslíku spojující zbytek kyseliny s alkoholovým nahrazen atomem síry. Vznikají esterifikačními reakcemi karboxylových kyselin s thioly. V biochemii jsou významnými zástupci deriváty koenzymu A, například acetyl-CoA.[1]

Příprava
Nejčastěji se thioestery připravují reakcemi acylchloridů s thioláty alkalických kovů:[1]
- RSNa + R′COCl → R′COSR + NaCl
Další často používaný způsob spočívá v odštěpení halogenidů solemi alkalických kovů s thiokarboxylovými kyselinami, například thioacetáty lze získat z thiooctanu draselného:[1]
- CH3COSK + RX → CH3COSR + KX
Obdobná alkylace octanových solí se provádí jen ojediněle. Lze ji provést působením Mannichových zásad na thiokarboxylové kyseliny:
- CH3COSH + R′2NCH2OH → CH3COSCH2NR′2 + H2O
Thioestery mohou být rovněž připraveny kondenzací thiolů a karboxylových kyselin za přítomnosti dehydratačního činidla:[2][3]
- RSH + R′CO2H → RSC(O)R′ + H2O
Obvykle používaným dehydratačním činidlem je zde [N,N'-dicyklohexylkarbodiimid (DCC).[4] Lepší udržitelnosti přípravy a výroby thioesterů bylo dosaženo použitím bezpečnějšího činidla v podobě anhydridu kyseliny propanfosfonové (T3P) a k přírodě šetrnějšího rozpouštědla cyklopentanonu.[5] Acylanhydridy a některé laktony mohou být použity na přípravu thioesterů reakcemi s thioly za přítomnosti zásady.
Thioestery mohou být vytvořeny přeměnou alkoholů Micunobovou reakcí za využití kyseliny thiooctové.[6]
Jinou možností je karbonylace alkynů a alkenů za přítomnosti thiolu.[7]
Reakce
Karbonylová skupina thioesterů je reaktivní vůči nukleofilům, dokonce reaguje i s vodou. Thioestery jsou tak častými meziprodukty přeměn alkylhalogenidů na alkylthioly. Thioestery reagují s aminy za tvorby amidů:
V podobné reakci, využívající „měkký“ kov k zachycení thiolátu, jsou thioestery přeměňovány na estery.[8]
Thioestery poskytují užitečnou chemoselektivitu při syntézách biomolekul.[9]
Reakcí probíhající výhradně u thioesterů je Fukujamovo párování, při němž thioester reaguje organozinečnatým halogenidem za katalýzy palladiem, přičemž se tvoří keton.

Biochemie

Thioestery jsou častými meziprodukty biosyntetických reakcí, jako jsou tvorba a rozklad mastných kyselin a kyseliny mevalonové, sloužící jako prekurzor steroidů. Jako příklady lze uvést malonyl-CoA, acetoacetyl-CoA, propionyl-CoA, cinamoyl-CoA a ACP. Acetogeneze probíhá přes syntézu acetyl-CoA. Do biosyntézy ligninů jsou zapojeny thioesterové deriváty kyseliny kávové.[10]
Tyto thioestery se tvoří podobně jako syntetické, rozdíl spočívá v tom, že dehydratačním činidlem je ATP. Thioestery mají také velký význam při značení bílkovin ubikvitinem, který označuje proteiny určené k degradaci.
Oxidací atomu síry u thioesterů (či thiolaktonů) je součástí bioaktivace léčiv proti srážení krve tiklopidinu, klopidogrelu a prasugrelu.[11][12]
Thionoestery
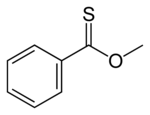
Thionoestery jsou sloučeniny izomerní s thioestery, atomem síry je zde nahrazen karbonylový kyslík esteru; například methylthionobenzoát má vzorec C6H5C(S)OCH3. Tyto látky se obvykle připravují reakcemi thioacylchloridů s alkoholy.[13]

Také mohou být získány reakcí Lawessonova činidla s příslušným esterem nebo Pinnerových solí se sulfanem. Další variantu představuje transesterifikace methylthionoesteru za přítomnosti alkoholu v zásaditém prostředí.[14]

Odkazy
Reference
V tomto článku byl použit překlad textu z článku Thioester na anglické Wikipedii.
Související články
- Thiokarboxylové kyseliny
- Liebeskindova–Šroglova reakce
- 2,2'-dipyridyldisulfid
Externí odkazy
 Obrázky, zvuky či videa k tématu Thioestery na Wikimedia Commons
Obrázky, zvuky či videa k tématu Thioestery na Wikimedia Commons


