Κουμουλένιο
Το κουμουλένιο ή βουτατριένιο είναι η (κανονικά) οργανική χημική ένωση με ημισυντακτικό τύπο H2C=C=C=CH2, αλλά οι έννοιες αυτές επεκτείνονται, επίσης, και σε μια σειρά άλλων υδρογονανθράκων με δύο ή περισσότερους συνεχόμενους διπλούς δεσμούς.[1] Αν μια ένωση περιέχει δύο (μόνο) συνεχόμενους διπλούς δεσμούς ανήκει στα αλλένια, το πρώτο μέλος της των οποίων είναι το προπαδιένιο. Σε αντίθεση με τα περισσότερα αλκάνια και (κάπως λιγότερο) αλκένια, τα κουμουλένια τείνουν να είναι άκαμπτα, γεγονός που τα καθιστά ελκυστικά για τη μοριακή νανοτεχνολογία. Τα πολυΐνια αποτελούν ένα άλλο είδος άκαμπτων ανθρακούχων ενώσεων. Τα κουμουλένια βρίσκονται σε περιοχές του διαστήματος όπου το υδρογόνο είναι (σχετικά) σπάνιο (βλέπετε αστροχημεία). Τα κουμουλένια που περιέχουν ετεροάτομα (δηλαδή και άλλα χημικά στοιχεία εκτός του άνθρακα και του υδρογόνου) ονομάζονται ετεροκουμουλένια[2]. Παραδείγματα ετεροκουμουλενίων είναι το σουλφοξείδιο του άνθρακα (CH2=S=O), αλλά και η κετένη (CH2=C=O).
| Κουμουλένιο | |||
|---|---|---|---|
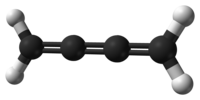 | |||
| Γενικά | |||
| Όνομα IUPAC | Βουτατριένιο | ||
| Άλλες ονομασίες | Κουμουλένιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C4H4 | ||
| Μοριακή μάζα | 52,07456 amu | ||
| Σύντομος συντακτικός τύπος | CH2=C=C=CH2 | ||
| Αριθμός CAS | 2873-50-9 | ||
| SMILES | C=C=C=C | ||
| Δομή | |||
| Μοριακή γεωμετρία | Επίπεδη | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 13 | ||
| Φυσικές ιδιότητες | |||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Επικινδυνότητα | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||

Σύνθεση
Η πρώτη σύνθεση κουμουλενίου που αναφέρθηκε ήταν η σύνθεση τετραφαινυλοβουτατριένιου, το 1921.[3] Η πιο κοινή συνθετική μέθοδος για σύνθεση κουμουλενίων βασίστηκε στην αναγωγική σύζευξη 1,1-διαλοβινυλιδενίων.[4] Το 1977, αναφέρθηκε ότι συνθέθηκε τετραφαινυλοβουτατριένιο με ομοσύζευξη του 2,2-διφαινυλο-1,1,1-τριβρωμοαιθανίου, παρουσία στοιχειακού χαλκού, σε διμεθυλοφορμαμίδιο (ως διαλύτη).[5]
Δομή
Η ακαμψία στα κουμουλένια προκύπτει από το γεγονός ότι υπάρχει σε αυτά ένα (τουλάχιστον) εσωτερικό άτομο άνθρακα που σχηματίζει δύο διπλούς δεσμούς. Αυτά τα εσωτερικά άτομα άνθρακα βρίσκονται σε sp υβριδισμό και τα (νοητά) επίπεδα διπλών δεσμών τους είναι κάθετα μεταξύ τους. Τα κουμουλένια με ζυγό αριθμό συνεχόμενων διπλών δεσμών και δύο (τουλάχιστον) ανόμοιους υποκαταστάτες μπορεί να είναι χειρόμορφα, αν και δεν έχουν κλασσικού τύπου στερεοκεντρικό σημείο. Από την άλλη πλευρά, τα κουμουλένια με μονό αριθμό συνεχόμενων διπλών δεσμών και δύο (τουλάχιστον) ανόμοιους υποκαταστάτες μπορεί να παροσιάσουν cis–trans ισομέρεια.
Αντιδράσεις
Οι χαρακτηριστικές αντιδράσεις των κουμουλενίων είναι όμοιες με αυτές των ενώσεων με απομονωμένους διπλούς δεσμούς. Αν και στα μόρια των κουμουλενίων τα εσωτερικά άτομα έχουν δυο π-δεσμούς σε πολύ μικρότερη απόσταση μεταξύ τους, στην ουσία αυτοί οι δυο π-δεσμοί ενεργούν όπως και οι κοινοί π-δεσμοί των ενώσεων με απομονωμένους διπλούς δεσμούς. Αυτό συμβαίνει γιατί οι δυο π-δεσμοί των εσωτερικών ατόμων άνθρακα των κουμουλενίων σχηματίζονται από τη μη υβριδισμένα p-τροχιακά. Όπως αυτά τα τροχιακά είναι κάθετα το ένα προς το άλλο και καταλαμβάνουν κάθετα γωνιακά επίπεδα, οι δυο δεσμοί είναι στην ουσία απομονωμένοι και έτσι ανίκανοι να αλληλεπιδράσουν μεταξύ τους, ώστε να δώσουν κάποια διαφορετική ιδιότητα από κάποιο συνδυασμό τους.
Κουμουλένια με μεταβατικά μέταλλα
Το πρώτο αναφερόμενο τέτοιο σύμπλοκο περιείχε ένα βινυλιδένιο ως συναρμοτή και ήταν η ένωση με μοριακό τύπο Ph2C2Fe2(CO)8, δηλαδή ο 1,1-διφαινυλοβινυλοκτακαρβονυλοδισίδηρος, που προέρχεται από την αντίδραση διφαινυλοκετένης (Ph2C=C=O) και πεντακαρβονυλοσιδήρου [Fe(CO)5]. Δομικά, αυτό το μόριο είναι παρόμοιο με τον εννεακαρβονυλοδισίδηρο [Fe2(CO)9], όπου ένας συναρμοτής μ-CO αντικαθίσταται από 1,1-διφαινυλοβινυλιδένιο. Το πρώτο μονομεταλλικό σύμπλοκο βινυλιδενίου ήταν το (C5H5)Mo(PPh3)(CO)2[C=C(CN)2]Cl[6], που ονομάζεται δικαρβονυλοκυκλοδικυανοβινυλοπενταδιενυλοτριφαινυλοφωσφινοχλωρομολυβδαίνιο.
Δείτε επίσης
Πηγές
- Speight J. G., “Chemical and Process Design Handbook”, McGraw-Hill, 2002.
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- University College of Cork