Sulfate de thallium(I)
composé chimique
(Redirigé depuis Sulfate de thallium)
Le sulfate de thallium(I) est un composé inorganique de formule Tl2SO4.
| Sulfate de thallium(I) | |
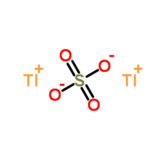 | |
| Identification | |
|---|---|
| Synonymes | Sulfate de thallium |
| No CAS | |
| No ECHA | 100.028.365 |
| No CE | 231-201-3 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | cristaux inodores, blancs ou incolores[1] |
| Propriétés chimiques | |
| Formule | Tl2SO4 |
| Masse molaire[2] | 504,829 ± 0,007 g/mol O 12,68 %, S 6,35 %, Tl 80,97 %, |
| Propriétés physiques | |
| T° fusion | 632 °C[1] |
| Solubilité | dans l'eau à 20 °C : 48,7 g·l-1[1] |
| Masse volumique | 6,77 g·cm-3[1] |
| Précautions | |
| SGH[5] | |
| H300, H315, H372 et H411 | |
| SIMDUT[6] | |
 D1A, | |
| Transport | |
| Écotoxicologie | |
| DL50 | 25 mg·kg-1 (rat, ingestion) |
| Composés apparentés | |
| Autres composés | sulfate de thallium(III) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
Propriétés
Ce sulfate est un solide cristallin blanc, inodore et sans goût, mais très toxique.
On l'utilise comme fourmicide et rodenticide. Le thallium se substitue au potassium dans le corps, inhibant la pompe sodium-potassium. Il provoque un gonflement du disque optique et une détérioration de la vue.
Traitement :
- charbon actif ;
- bleu de Prusse, ferrocyanure ferrique, Fe4[Fe(CN)6]3[7].
Les empoisonnements par thallium peuvent être détectés par analyse spectrale, même après la crémation du corps.
De faibles traces de radioisotopes sont utilisées dans les analyses médicales.






