Tétrasilane
Le tétrasilane est un composé chimique de formule Si4H10. Ce silane est l'analogue structurel du n-butane C4H10. Il se présente comme un liquide pyrophorique incolore à l'odeur repoussante qui tend à s'enflammer spontanément dans l'air au-dessus de 54 °C. Il se décompose lentement à la lumière du jour en libérant de l'hydrogène H2 et des silanes plus légers[3].
| Tétrasilane | |
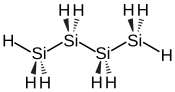 | |
| Structure du tétrasilane | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.132.456 |
| No CE | 616-515-4 |
| Propriétés chimiques | |
| Formule | Si4H10 |
| Masse molaire[1] | 122,421 4 ± 0,001 9 g/mol H 8,23 %, Si 91,77 %, |
| Propriétés physiques | |
| T° fusion | −89,9 °C[2] |
| T° ébullition | 108,1 °C[2] |
| Masse volumique | 0,792 g·cm-3[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
On peut produire un mélange de silanes en faisant réagir du siliciure de magnésium Mg2Si avec des acides dilués, par exemple de l'acide phosphorique H3PO4 à 20 % de 50 à 60 °C[4]. Le mélange obtenu peut contenir des silanes SinH2n+2 jusqu'au terme n = 15, avec de l'isotétrasilane (SiH3)3SiH en plus du n-tétrasilane. La réaction du siliciure de magnésium avec de l'acide chlorhydrique à 25 % donne 40 % de silane SiH4, 30 % de disilane Si2H6, 15 % de trisilane Si3H8, 10 % de tétrasilane Si4H10 et 5 % de silanes supérieurs[5]. Ce mélange peut être séparé par distillation fractionnée.
On obtient également des silanes supérieurs à partir du silane sous l'effet de décharges électrostatiques[4].
Le tétrasilane se dismute en 3-silylpentasilane et disilane sous l'effet de la lumière[6] :
- 2 Si4H10 ⟶ Si2H6 + H3Si–SiH(Si2H6)2.
L'isotétrasilane peut être obtenu en chauffant le n-tétrasilane dans du xylène en présence de chlorure d'aluminium[7] :
- H3Si–SiH2–SiH2–SiH3 ⟶ H3Si–SiH(SiH3)–SiH3.
