Butan
| Egenschoppen in’n Vergliek | ||
| Naam | n-Butan[1] | Isobutan[2] |
| Strukturformel | 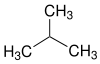 | |
| CAS-Tall | 106-97-8 | 75-28-5 |
| Summenformel | C4H10 | |
| Molare Masse | 58,12 g·mol−1 | |
| Kortbeschrieven | bi 20 °C un 1013 mbar gasförmig | |
| Smöltpunkt | −138,29 °C | −159,42 °C |
| Kaakpunkt | −0,50 °C | −11,7 °C |
| Dampdruck (20 °C) | 208 kPa | 301,9 kPa |
| Dicht bi 0 °C, 1013 hPa | 2,71 kg·m−3 | 2,70 kg·m−3 |
| Löslichkeit | 61 mg·l−1 | 49 mg·l−1 |
| Ünnere Explosionsgrenz (UEG) | 1,4 Vol% | 1,5 Vol% |
| 33 g·m−3 | 37 g·m−3 | |
| Bövere Explosionsgrenz (OEG) | 9,4 Vol% | 9,4 Vol% |
| 231 g·m−3 | 231 g·m−3 | |
De Butanen sünd en Stoffgrupp binnen de Grupp vun de Alkanen, de dör de Summenformel C4H10 kenntekent sünd. De Grupp besteiht blots ut twee Vertreders, de as n-Butan un iso-Butan betekent warrt un to’nanner isomer sünd. Bi beide Stoffen hannelt sik dat üm brennbore Gasen ahn Klöör, de licht fletig to maken gaht (Fletiggas). Se löst sik kuum in Water, dorför aver goot in Ethanol un Ether[3].
Vörkamen un Dorstellen
De Butanen kamt natürlich in’t Eerdgas vör, warrt aver ok dör Cracken ut Eerdööl wunnen. Scheedt warrn künnt de beiden Isomeren dör Adsorpschoon un frakschoneerte Desorpschoon an Aktivkahl oder Zeolithen. Iso-Butan warrt in grote Mengden ut n-Butan dör Isomeriseren wunnen mit en Mischen ut Aluminiumchlorid un Chlorwaterstoff as Katalysater[3].
Bruuk
In de cheemschen Industrie warrt Butanen veel to’n Dorstellen vun C4-Alkenen as 1,3-Butadien, But-1-en, But-2-enen un Isobuten bruukt, as ok för de Synthees vun högere Kohlenwaterstoffen (för „Alkylatbenzin“), Thiophen oder Oxidatschoonsprodukten as tert-Butylhydroperoxid. Grote Bedüden hebbt de Gasen ok as Brenngas to’n Heizen, Küllmiddels oder as Driefgasen[3][4].
Sekerheit
As all Alkanen hebbt ok de Butanen en narkotiseren Wirken. Bi en Atendepresschoon, de dordör utlöst warrt, künnt Effekten op dat Zentralnervensystem utlöst warrn, so as Opregen, Euphorie oder Övergeven. Hoge Dosen künnt sik ok slecht op den Bloodkreisloop un dat Hart utwirken un to’n Bispeel Hartrhythmusstören utlösen[4].