الهيكل المغناطيسي
مصطلح التركيب المغناطيسي للمادة يتعلق بالتنظيم المرتب للدوران المغناطيسي عادة داخل شبكة بلورية مرتبة. ودراستها هي فرع من فيزياء الجوامد .

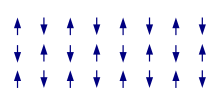

الهياكل المغناطيسية
معظم المواد الصلبة غير مغناطيسية ، أي أنها لا تعرض أي بنية مغناطيسية. نظرًا لمبدأ استبعاد باولي ، فإن كل حالة تشغلها إلكترونات تدور بشكل معاكس ، بحيث يتم تعويض كثافة الشحنة في كل مكان وتكون درجة حرية الدوران طفيفة. ومع ذلك فإن مثل هذه المواد تظهر سلوكًا مغناطيسيًا ضعيفًا ، على سبيل المثال بسبب مبادئ باولي البارامغناطيسية أو لانجفين أو لانداو المغناطيسية .
الحالة الأكثر إثارة للاهتمام هي عندما ينكسر إلكترون المادة تلقائيًا بسبب التناظر المذكور أعلاه. بالنسبة للمغناطيسية الحديدية في الحالة الأرضية ، يوجد محور تكميم دوران شائع وفائض عالمي من الإلكترونات لرقم كمي مغزلي معين ، وهناك عدد أكبر من الإلكترونات التي تشير في اتجاه واحد أكثر من الاتجاه الآخر ، مما يعطي مغنطة مجهرية (عادةً تم اختيار غالبية الإلكترونات للإشارة). في أبسط حالات المغناطيسية المضادة (المتداخلة) ، لا يزال هناك محور تكميم شائع ، لكن الإدارات الإلكترونية تشير بالتناوب لأعلى ولأسفل ، مما يؤدي مرة أخرى إلى إلغاء المغنطة المجهرية. على وجه التحديد في حالة تثبيط التفاعلات ، يمكن أن تصبح الهياكل الناتجة أكثر تعقيدًا مع وجود توجهات ثلاثية الأبعاد للإدارات المحلية. وأخيرًا المغناطيسية الحديدية كما يتم عرضها بشكل نموذجي بواسطة المغنتيت هي حالة وسيطة: هنا يكون المغنطة عالميًا غير معوض كما هو الحال في المغناطيسية الحديدية ، ولكن نقاط المغنطة المحلية توجه في اتجاهات مختلفة.
المناقشة أعلاه تتعلق ببنية الحالة الأساسية. بالطبع تؤدي درجات الحرارة المحدودة إلى إثارة تكوين الدوران. هنا يمكن التباين بين وجهتي نظر متطرفتين: في صورة جامدة للمغناطيسية (وتسمى أيضًا المغناطيسية المتجولة) ، يتم فصل الحالات الإلكترونية ، ويؤدي تفاعل المجال المتوسط إلى كسر التناظر. من وجهة النظر هذه ، مع زيادة درجة الحرارة ، ستنخفض المغنطة المحلية بشكل متجانس ، حيث يتم نقل الإلكترونات المفردة غير المحددة من القناة العلوية إلى القناة السفلية. من ناحية أخرى ، في حالة اللحظة المحلية ، يتم ترجمة الحالات الإلكترونية إلى ذرات معينة ، مما يعطي دورانًا ذريًا ، والذي يتفاعل فقط على مدى قصير ويتم تحليله عادةً باستخدام نموذج هايزنبرغ . هنا ، تؤدي درجات الحرارة المحدودة إلى انحراف توجهات الدورات الذرية عن التكوين المثالي ، وبالتالي فإن المغناطيس الحديدي يقلل أيضًا من المغنطة العيانية.
بالنسبة للمغناطيسية الموضعية يمكن وصف العديد من الهياكل المغناطيسية بواسطة مجموعات الفضاء المغناطيسية ، والتي تعطي حسابًا دقيقًا لجميع مجموعات التماثل الممكنة للتكوينات الأعلى / الأسفل في بلورة ثلاثية الأبعاد. ومع ذلك ، فإن هذه الشكلية غير قادرة على تفسير بعض الهياكل المغناطيسية الأكثر تعقيدًا ، مثل تلك الموجودة في المغناطيسية .
تقنيات دراستها
يمكن دراسة هذا الترتيب من خلال ملاحظة الحساسية المغناطيسية كدالة لدرجة الحرارة و / أو حجم المجال المغناطيسي المطبق ، ولكن من الأفضل الحصول على صورة ثلاثية الأبعاد لترتيب السبينات عن طريق حيود النيوترونات . [1] [2] تتشتت النيوترونات بشكل أساسي بواسطة نوى الذرات في الهيكل. وعند درجة حرارة أعلى من نقطة ترتيب اللحظات المغناطيسية حيث تتصرف المادة على أنها مادة بارامغناطيسية ، فإن حيود النيوترون سيعطي بالتالي صورة للبنية البلورية فقط. تحت نقطة الترتيب على سبيل المثال درجة حرارة نيل للمغناطيس المضاد أو نقطة كوري للمغناطيس الحديدي ، ستختبر النيوترونات أيضًا تشتتًا من اللحظات المغناطيسية لأنها تمتلك الدوران. لذلك ستتغير شدة انعكاسات Bragg . في الواقع في بعض الحالات ستحدث انعكاسات Bragg جديدة تمامًا إذا كانت خلية الوحدة الخاصة بالترتيب أكبر من خلية التركيب البلوري. هذا شكل من أشكال تكوين البنية الفوقية . وبالتالي قد يختلف تناظر الهيكل الكلي عن البنية التحتية البلورية. يجب أن يتم وصفه من قبل إحدى المجموعات المغناطيسية (Shubnikov) التي يبلغ عددها 1651 بدلاً من واحدة من مجموعات الفضاء غير المغناطيسية. [3]
على الرغم من أن حيود الأشعة السينية العادي «أعمى» بالنسبة إلى ترتيب الدورات ، فقد أصبح من الممكن استخدام شكل خاص من حيود الأشعة السينية لدراسة التركيب المغناطيسي. إذا تم تحديد طول موجي قريب من حافة الامتصاص لأحد العناصر الموجودة في المواد ، يصبح التشتت شاذًا ويكون هذا المكون للتشتت حساسًا (إلى حد ما) للشكل غير الكروي للإلكترونات الخارجية للذرة مع دوران غير مزدوج. هذا يعني أن هذا النوع من حيود الأشعة السينية الشاذ يحتوي على معلومات مطلوبة.
في الآونة الأخيرة ، يتم تطوير تقنيات سطح الطاولة التي تسمح بدراسة الهياكل المغناطيسية دون اللجوء إلى مصادر النيوترون أو السنكروترون. [4]
التركيب المغناطيسي للعناصر الكيميائية
هناك ثلاثة عناصر فقط مغنطيسية في درجة حرارة الغرفة وضغطها: الحديد والكوبالت والنيكل . هذا لأن درجة حرارة كوري ، Tc ، أعلى من درجة حرارة الغرفة (Tc> 298K). يحتوي الجادولينيوم على مغنطة تلقائية أقل بقليل من درجة حرارة الغرفة (293 كلفن) وأحيانًا يُحسب كعنصر مغناطيسي حديدي رابع. كان هناك بعض الاقتراحات بأن الجادولينيوم له ترتيب مغناطيسي شمسي ، [5] لكن البعض الآخر يدافع عن وجهة النظر القديمة بأن الجادولينيوم هو مغناطيس حديدي تقليدي. [6]
كل من عناصر الدسبروزيوم والإربيوم لهما اثنين من التحولات المغناطيسية. إنها مغناطيسية في درجة حرارة الغرفة ، لكنها تصبح مغنطيسية شمسية أقل من درجات حرارة نيل الخاصة بها ، ثم تصبح مغنطيسية مغناطيسية أقل من درجات حرارة كوري. تعرض عناصر هولميوم وتربيوم وثوليوم هياكل مغناطيسية أكثر تعقيدًا. [7]
هناك أيضًا ترتيب مضاد للمغناطيسية ، والذي يصبح مضطربًا فوق درجة حرارة نيل . يشبه الكروم إلى حد ما مغناطيسًا مضادًا بسيطًا ، ولكنه يحتوي أيضًا على تعديل غير متكافئ لموجة كثافة الدوران أعلى تناوب الدوران البسيط من الأعلى إلى الأسفل. [8] يحتوي المنغنيز (في شكل α-Mn) على 29 خلية وحدة ذرة ، مما يؤدي إلى ترتيب معقد ، ولكن متكافئ و مضاد مغناطيسي عند درجات حرارة منخفضة ( مجموعة الفضاء المغناطيسي P 4 2'm '). [9] [10] على عكس معظم العناصر ، التي تكون مغناطيسية بسبب الإلكترونات ، فإن الترتيب المغناطيسي للنحاس والفضة يهيمن عليه عزم مغناطيسي نووي أضعف بكثير (قارن ماغنيتون بور والمغنيطون النووي ) مما يؤدي إلى درجات حرارة انتقالية قريبة من الصفر المطلق . [11] [12]
تلك العناصر التي تصبح موصلات فائقة تظهر قوة مغناطيسية فائقة تحت درجة حرارة حرجة.
