2,2′-bipyridin
2,2'-bipyridin je organická sloučenina se vzorcem C10H8N2, patřící mezi bipyridiny. Jedná se o bidentátní chelatující ligand, který tvoří komplexní sloučeniny s mnoha přechodnými kovy. Jeho komplexy s rutheniem a platinou se vyznačují silnou luminiscencí.
| 2,2′-bipyridin | |
|---|---|
 Strukturní vzorec | |
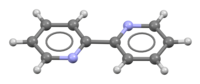 Model molekuly | |
| Obecné | |
| Systematický název | 2,2′-bipyridin |
| Ostatní názvy | bipy, bpy |
| Sumární vzorec | C10H8N2 |
| Vzhled | bílé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 366-18-7 |
| EC-no (EINECS/ELINCS/NLP) | 206-674-4 |
| PubChem | 1474 |
| SMILES | C1=CC=NC(=C1)C2=CC=CC=N2 |
| InChI | 1S/C10H8N2/c1-3-7-11-9(5-1)10-6-2-4-8-12-10/h1-8H |
| Vlastnosti | |
| Molární hmotnost | 156,18 g/mol |
| Teplota tání | 72 °C (345 K)[1] |
| Teplota varu | 273 °C (546 K)[1] |
| Hustota | g/cm3 |
| Rozpustnost ve vodě | 0,593 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v ethanolu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v benzenu a diethyletheru[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H301 H302 H311 H312 H319 H412[1] |
| P-věty | P264 P270 P273 P280 P301+310 P301+312 P302+352 P305+351+338 P312 P321 P322 P330 P337+313 P361 P363 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Příprava, struktura a vlastnosti
2,2'-bipyridin se připravuje dehydrogenací pyridinu pomocí Raneyova niklu:[2]
- 2 C5H5N → (C5H4N)2 + H2
I když bývá nekoordinovaný bipyridin zobrazován s atomy dusíku v poloze cis, tak má v pevné formě i v roztoku ze všech konformací nejnižší energii rovinná, s dusíkovými atomy v polohách trans.[3]
Monoprotonovaný bipyridin zaujímá cis konformaci.[4]
Tvorba komplexů obdobného N,N-heterocyklického ligandu fenantrolinu nevyžaduje překonání entalpických a entropických bariér, a tak jsou tyto komplexy obvykle stabilnější. pKa konjugovaných kyselin jsou 4,86 a 4,3 a fenantrolin a bipy jsou tak podobně silnými zásadami.[5]
Koordinačně chemické vlastnosti
Příklady komplexů
- Mo(CO)4(bipy), odvozený od Mo(CO)6
- RuCl2(bipy)2,[8] prekurzor komplexů se smíšenými ligandy
- [Ru(bipy)3]Cl2, používaný jako luminofor.
- [Fe(bipy)3]2+ se využívá ke kolorimetrické analýze železnatých iontů.
Tris-bipy komplexy
Komplexy bypyridinu silně absorbují ve viditelném spektru, což lze využít v ultrafialovo-viditelné spektroskopii. Přechody elektronů mezi energetickými hladinami souvisí s přenosy nábojů mezi kovy a ligandy. V „tris(bipy) komplexech“ se na kov koordinují tři molekuly bipyridinu, což lze zapsat jako [M(bipy)3]n+ (M = ion kovu; například Cr, Fe, Co, Ru nebo Rh; bipy = 2,2′-bipyridin). Tyto komplexy obsahují šestikoordinované oktaedrické struktury a mají dva enantiomery:

Tyto i jiné homoleptické tris-2,2′-bipy komplexy přechodných kovů jsou elektroaktivní. Jak na kov, tak i na ligand zaměřené elektrochemické reakce jsou vratné jednoelektronové reakce, které lze pozorovat pomocí cyklické voltametrie. Za silně redukujících podmínek může být většina komplexů tris(bipy) redukována na neutrální sloučeniny obsahující ligandy bipy−; jako příklad lze uvést M(bipy)3, kde M = Al, Cr, Si.
Odkazy
Související články
- 2,2'-bichinolin
Externí odkazy
 Obrázky, zvuky či videa k tématu 2,2′-bipyridin na Wikimedia Commons
Obrázky, zvuky či videa k tématu 2,2′-bipyridin na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku 2,2′-Bipyridine na anglické Wikipedii.




