3-μεθυλοπεντάνιο
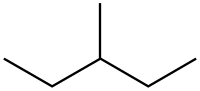
Το 3-μεθυλοπεντάνιο είναι ένα διαλκαδισμένο αλκάνιο δηλαδή κορεσμένος υδρογονάνθρακας και πιο συγκεκριμένα ένα από τα ισομερή εξάνια. Το 3-μεθυλοπεντάνιο έχει μοριακό τύπο C6H14 και ημισυντακτικό τύπο CH3CH2CH(CH3)CH2CH3.
| 3-μεθυλοπεντάνιο | |||
|---|---|---|---|
 | |||
 | |||
 | |||
 | |||
| Γενικά | |||
| Όνομα IUPAC | 3-μεθυλοπεντάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C6H14 | ||
| Μοριακή μάζα | 86,18 amu | ||
| Σύντομος συντακτικός τύπος | CH3CH2CH(CH3)CH2CH3 | ||
| Συντομογραφίες | sBuΕτ | ||
| Αριθμός CAS | 96-14-0 | ||
| SMILES | CCC(C)CC | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 4 εξάνιο 2-μεθυλοπεντάνιο 2,2-διμεθυλοβουτάνιο 2,3-διμεθυλοβουτάνιο | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -118 °C | ||
| Σημείο βρασμού | 64 °C | ||
| Εμφάνιση | Άχρωμο υγρό | ||
| Χημικές ιδιότητες | |||
| Βαθμός οκτανίου | 74,3 | ||
| Βαθμός κετανίου | 30 | ||
| Επικινδυνότητα | |||
   | |||
| Εξαιρετικά εύφλεκτο (F+), Επιβλαβές (Xn), Τοξικό για τους υδρόβιους οργανισμούς (N) | |||
| Φράσεις κινδύνου | 12, 51/53, 65, 66, 67 | ||
| Φράσεις ασφαλείας | 2, 9, 16, 29, 33, 61, 62 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Ονοματολογία
Η ονομασία «3-μεθυλοπεντάνιο» από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το αρχικό πρόθεμα «μεθυλο-» δηλώνει την παρουσία διακλάδωσης ενός (1) ατόμου άνθρακα και συγκεκριμένα στο άτομο άνθρακα #3, όπως δηλώνει ο αρχικός αριθμός θέσης, το τμήμα «πεντ-» δηλώνει την παρουσία πέντε (5) ατόμων άνθρακα στην κύρια ανθρακική αλυσίδα της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας.
Δομή
Το μόριό του περιέχει έξι (6) άτομα άνθρακα, τρία (3) από τα οποία είναι πρωτοταγή,[1] δύο (2) δευτεροταγή[2] και ένα (1) τριτοταγές[3]. Περιέχει, ακόμη, δεκατέσσερα (14) άτομα υδρογόνου. Οι δεσμοί C-Η που σχηματίζονται είναι ελαφρά πολωμένοι (~3%) ομοιοπολικοί τύπου σ (2sp3-1s), με μήκος 108,7 pm. Ο δεσμός C-C είναι ομοιοπολικός τύπου σ (2sp3-2sp3), με μήκος 154 pm. Οι δε γωνίες 
| Δεσμοί[4] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C-C | σ | 2sp3-2sp3 | 154 pm | |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| C#1,#5,#1' | -0,09 | |||
| C#2,#4 | -0,06 | |||
| C#3 | -0,03 | |||
| H | +0,03 | |||
Παραγωγή
Απομόνωση από φυσικές και βιομηχανικές πηγές
- Απομονώνεται από το πετρέλαιο.
- Απομονώνεται από μείγματα που προκύπτουν από πυρόλυση βαρύτερων προϊόντων διύλισης πετρελαίου ή και πολυμερών υδρογονανθράκων.
Παρασκευή με αντιδράσεις σύνθεσης: Από πρώτες ύλες με μικρότερη ανθρακική αλυσίδα
1. Δομικά το 3-μεθυλοπεντάνιο αποτελείται από δυο μέρη: δευτεροταγές βουτύλιο [CH3CH2CH(CH3)] και αιθύλιο (CH3CH2). Επομένως, ο απλούστερος τρόπος παρασκευής χημικά καθαρού 3-μεθυλοπεντάνιου είναι η αντίδραση ζεύγους 2-αλοβουτανίου - αιθυλολιθίου ή αντιστοίχως δευτεροταγούς βουτυλολιθίου - αλαιθανίου:[5]


ή

2. Αν επιχειρηθεί η ανάλογη αντίδραση Βουρτζ (Wurtz) το αποτέλεσμα είναι ένα μείγμα προϊόντων, που συμπεριλαμβάνουν, εκτός του 3-μεθυλοπεντανίου, αιθάνιο και 3,4-διμεθυλεξάνιο[6]. Η αντίδραση είναι ασύμφορη σε σύγκριση με την προηγούμενη, αλλά τα προϊόντα αυτά διαχωρίζονται σχετικά εύκολα με απόσταξη: Το βαρύτερο, το 3,4-διμεθυλοεξάνιο είναι υγρό (σ.ζ.: 164 °C)[7] στις κανονικές συνθήκες περιβάλλοντος. Το ζητούμενο (εδώ) 3-μεθυλοπεντάνιο είναι επίσης υγρό, αλλά πολύ πτητικότερο (σ.ζ.: 64 °C), ενώ τέλος το βουτάνιο είναι αέριο εύκολα υγροποιήσιμο με σχετικά μικρή ψύξη ή και με συμπίεση (σ.ζ.: -0,5 °C).
Παρασκευή με αντιδράσεις χωρίς αλλαγή ανθρακικής αλυσίδας
Με αναγωγή αλογονούχων ενώσεων
1. Με «υδρογόνο εν τω γενάσθαι», δηλαδή μέταλλο + οξύ:[8]

ή
ή
ή

ή
ή
ή
3. Με αναγωγή των αντίστοιχων ιωδαλκανίων από HI:[10]

ή
ή
ή
4. Με αναγωγή των κατάλληλων αλαλκανίων από σιλάνιο, παρουσία τριφθοριούχου βορίου παράγεται βουτάνιo:[11]

ή
ή
ή
5. Αναγωγή των κατάλληλων αλκυλαλογονιδίων από ένα αλκυλοκασσιτεράνιο. Π.χ.:[12]

ή
ή
ή
6. Με αναγωγή από ιδιαίτερα ηλεκτροθετικά μέταλλα, όπως αλκάλια ή αλκαλικές γαίες, και στη συνέχεια υδρόλυση των παραγόμενων οργανομεταλλικών ενώσεων:


ή

ή

ή



ή

ή

ή

Με υδρογόνωση ακόρεστων υδρογονανθράκων
1. Από 3-μεθυλο-1-πεντένιο:[15]

2. Από 3-μεθυλο-2-πεντένιο:[15]

3. Από 2-αιθυλο-1-βουτένιο:[15]

4. Από 3-μεθυλο-1,2-πενταδιένιο:[15]

5. Από 3-μεθυλο-1,3-πενταδιένιο:[15]

6. Από 3-μεθυλο-1,4-πενταδιένιο:[15]

7. Από 3-μεθυλοπεντίνιο-1:[16]

8. Από 3-μεθυλο-1,2,4-πεντατριένιο:[15]

9. Από 3-μεθυλο-4-πεντεν-2-ίνιο:[15][16]

10. Από 3-μεθυλο-4-πεντεν-1-ίνιο:[15][16]

11. Από μεθυλοπενταδιενίνιο:[15][16]

12. Από μεθυλοπενταδιίνιο:[16]

Με αναγωγή οξυγονούχων ενώσεων
1. Με αναγωγή κατάλληλων αλδεϋδών - Αντίδραση Wolf-Kishner:[17]
- 1. Από 3-μεθυλοπεντανάλη:

- 2. Από αιθυλοβουτανάλη:

2. Με αναγωγή κατάλληλων κετονών - Αντίδραση Clemmensen[18]::
- 1. Από 3-μεθυλοπεντανόνη:

Με αναγωγή θειούχων ενώσεων
1. Με αναγωγή των κατάλληλων θειολών μπορεί να παραχθεί 3-μεθυλοπεντάνιο. Π.χ. από την αναγωγή της 3-μεθυλο-1-πεντανοθειόλης (μέθοδος Raney):[19]

2. Με αναγωγή των κατάλληλων θειεστέρων μπορεί να παραχθεί 3-μεθυλοπεντάνιο.. Π.χ. από την αναγωγή του δι(3-μεθυλοπεντυλο)θειαιθέρα (μέθοδος Raney):[19]

Παρασκευή με αντιδράσεις αποσύνθεσης με μείωση του μήκους της ανθρακικής αλυσίδας
- Με τη θέρμανση αΛκαλικού διαλύματος 4-μεθυλοεξανικού οξέος [CH3CH2CH(CH3)CH2CH2COOH] ή [2,3-διμεθυλοπεντανικού οξέος [CH3CH2CΗ(CΗ3)CΗ(CΗ3)COOH] ή 2-αιθυλο-2-μεθυλοβουτανικό οξέος [CH3CH2C(CH3)(CH2CH3)COOH] ή [3-αιθυλοπεντανικού οξέος [(CH3)2CHCH2CH2COOH]:[20]

ή
ή
ή
Φυσικές ιδιότητες και ισομερή
Το 3-μεθυλοπεντάνιο είναι άχρωμο υγρό με ελαφριά χαρακτηριστική οσμή. Ανήκει στην οικογένεια των αλκανίων.Με βάση το χημικό τύπο του (C6H12) προκύπτει ότι η ένωση σχηματίζει τέσσερα (4) ισομερή και συγκεκριμένα τα ακόλουθα:
- Εξάνιο: CH3(CH2)4CH3
- 2-μεθυλοπεντάνιο (ισοεξάνιο): CH3CH2CH2CH(CH3)2
- 2,2-διμεθυλοβουτάνιο (νεοεξάνιο): CH3CH2C(CH3)3
- 2,3-διμεθυλοβουτάνιο: (CH3)2CHCH(CH3)2
| Συντακτικός τύπος Δομή | Όνομα IUPAC (ελληνική μορφή) Όνομα | Μοριακό Βάρος | Σημείο ζέσεως (°C, 1 atm) | Βαθμός οκτανίου | Βαθμός κετανίου |
 | κ-εξάνιο εξάνιο | 86,18 | 69 | 26 | 42 |
 | 2-μεθυλοπεντάνιο ισοεξάνιο | 58,12 | 60 | 73,5 | 23 |
 | 3-μεθυλοπεντάνιο | 58,12 | 64 | 74,3 | 30 |
 | 2,2-διμεθυλοβουτάνιο νεοεξάνιο | 58,12 | 49,73 | 93,4 | 24,4 |
 | 2,3-διμεθυλοβουτάνιο | 58,12 | 57,9 | 94,3 |
Χημικές ιδιότητες
Οξείδωση
1. Τέλεια καύση: Όπως όλα τα αλκάνια, το 3-μεθυλοπεντάνιο με περίσσεια οξυγόνου καίγεται προς διοξείδιο του άνθρακα και νερό:[21]

2. Παραγωγή υδραερίου:

3. Καταλυτική οξείδωση κυρίως προς 3-μεθυλο-3-πεντανόλη:

4. Οξείδωση με υπερμαγγανικό κάλιο προς 3-μεθυλο-3-πεντανόλη:

5. Οξείδωση με διοξιράνιο προς 3-μεθυλο-3-πεντανόλη:
Αλογόνωση[25]

- Δραστικότητα των X2: F2 > Cl2 > Br2 > Ι2.
- όπου 0<a,b,c,d<1, a + b + c + d = 0, διαφέρουν ανάλογα με το αλογόνο:
- Τα F και Cl είναι πιο δραστικά και λιγότερο εκλεκτικά. Η αναλογία των αλοπεντανίων τους εξαρτάται κυρίως πό τη στατιστική αναλογία των προς αντικατάσταση ατόμων H. Ειδικά για το χλώριο θα έχουμε:
- 3-μεθυλο-1-χλωροπεντάνιο: 6·1 = 6.
- 3-μεθυλο-2-χλωροπεντάνιο: 4·3,8 = 15,2.
- 3-μεθυλο-3-χλωροπεντάνιο: 1·5 = 5.
- 2-αιθυλο-1-βουτάνιο: 3·1 = 3.
- Δηλαδή το μείγμα που προκύπτει είναι: 20,5% 3-μεθυλο-1-χλωροπεντάνιο, 52,1% 3-μεθυλο-2-χλωροπεντάνιο, 17,1% 3-μεθυλο-3-χλωροπεντάνιο και 10,3% 2-αιθυλο-1-χλωροβουτάνιο.
- Τα Br και I είναι πιο εκλεκτικά και λιγότερο δραστικά. Η αναλογία των αλοπεντανίων μεταβάλλεται δραστικά προς όφελος του τριτοταγούς 3-αλο-2-μεθυλοπεντανίου. Ειδικά για το βρώμιο θα έχουμε:
- 1-βρωμο-3-μεθυλοπεντάνιο: 6·1 = 6.
- 2-βρωμο-3-μεθυλοπεντάνιο: 4·82 = 328.
- 3-βρωμο-3-μεθυλοπενάνιο: 1·1600 = 1600.
- 2-αιθυλο-1-βρωμοβουτάνιο: 3·1 = 3.
- Δηλαδή το μείγμα που προκύπτει είναι: 3‰ 1-βρωμο-3-μεθυλοπεντάνιο, 16,9% 2-βρωμο-3-μεθυλοπεντάνιο, 82,6% 3-βρωμο-3-μεθυλοπεντάνιο και 1‰ 2-αιθυλο-1-βρωμο-βουτάνιο.
- Ανάλυση του μηχανισμού της χλωρίωσης του CH3CH2CH(CH3)CH2CH3:
- 1. Έναρξη: Παράγονται ελεύθερες ρίζες.

- Η απαιτούμενη ενέργεια προέρχεται από το υπεριώδες φως (UV) ή θερμότητα (Δ).
- 2. Διάδοση: Καταναλώνονται οι παλιές ελεύθερες ρίζες, σχηματίζοντας νέες.
- 3. Τερματισμός: Καταναλώνονται μεταξύ τους οι ελεύθερες ρίζες, κατά τη στατιστικά σπάνια περίπτωση της συνάντησής τους.
- Είναι όμως πρακτικά δύσκολο να σταματήσει η αντίδραση στην παραγωγή μονοααλογονιδίων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες CH3CH2CH(CH3)CH2CH3 και Χ2 θα παραχθεί μείγμα όλων των αλογονοπαραγώγων του CH3CH2CH(CH3)CH2CH3.
- Αν όμως χρησιμοποιηθει περίσσεια CH3CH2CH(CH3)CH2CH3, τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης CH3CH2CH(CH3)CH2CH3(CH3)2 με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
Παρεμβολή καρβενίων
- Τα καρβένια (π.χ. [:CH2]) μπορούν παρεμβληθούν στους δεσμούς C-H. Π.χ. έχουμε:[28]
- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε;

- Παρεμβολή στους έξι (6) δεσμούς 1,5-CH2-H: 6
- Παρεμβολή στους τέσσρεις (4) δεσμούς 2,4-CH-H: 4.
- Παρεμβολή στο δεσμό C-H: 1.
- Παρεμβολή στους τρεις (3) δεσμούς 1'-CH2-H): 4.
Προκύπτει επομένως μείγμα 3-μεθυλεξάνιου (~43%), 2,3-διμεθυλοπεντάνιου (~29%), 3,3-διμεθυλοπεντάνιο (~7%) και αιθυλοπεντάνιου (-29%).
Νίτρωση

όπου 0<a,b,c,d<1, a + b + c + d = 1.
Προσθήκη σε πολλαπλούς δεσμούς
Το 3-μεθυλοπεντάνιο μπορεί να δώσει αντιδράσεις προσθήκης σε πολλαπλούς δεσμούς κατά την έννοια (CH3CH2)2Cδ-(CH3)-Hδ+. Π.χ.:[30]

Καταλυτική ισομερείωση
To 3-μεθυλοπεντάνιο μπορεί να υποστεί καταλυτική ισομερείωση προς εξάνιο, 2-μεθυλοπεντάνιο, 2,3-διμεθυλοβουτάνιο και 2,3-διμεθυλοβουτάνιο:

Αναφορές και σημειώσεις
Πηγές
- Η σελίδα της Ε.Ε. για την ταξινόμηση και την επισήμανση των επικίνδυνων ουσιών.
- Παπαγεωργίου Β.Π., “Εφαρμοσμένη Οργανική Χημεία: Άκυκλες Ενώσεις”, Εκδόσεις Παρατηρητής, Θεσσαλονίκη 1986.
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Μερικές από τις ενέργειες αντιδράσεων υπολογίστηκαν με χρήση κατάλληλου λογισμικού. Θα διασταυρωθούν και βιβλιογραφικά το συντομότερο για μεγαλύτερη ακρίβεια.














