Acide tartronique
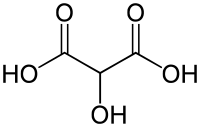
L'acide tartronique ou acide 2-hydroxymalonique est le plus simple des acides dicarboxyliques hydroxylés. Sa formule est HOOC-CH(OH)-COOH. Il peut être produit avec l'acide 2-cétogluconique par la bactérie Acetobacter acetosum dans un milieu riche en glucose[3].
| Acide tartronique | |
 | |
| Identification | |
|---|---|
| Nom UICPA | acide 2-hydroxypropanedioïque |
| Synonymes | acide tartronique |
| No CAS | |
| No ECHA | 100.001.184 |
| No CE | 201-301-1 |
| PubChem | 45 |
| SMILES | |
| InChI | |
| Apparence | poudre beige[1] |
| Propriétés chimiques | |
| Formule | C3H4O5 [Isomères] |
| Masse molaire[2] | 120,060 9 ± 0,004 2 g/mol C 30,01 %, H 3,36 %, O 66,63 %, |
| Propriétés physiques | |
| T° fusion | 158 à 160 °C (décomposition)[1] |
| Précautions | |
| SGH[1] | |
| H315, H319, H335, P261 et P305+P351+P338 | |
| NFPA 704[1] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
Propriétés
L'acide tartronique cristallise en prismes incolores qui se décomposent de 158 à 160 °C, libérant du dioxyde de carbone[4].
Ses bases conjuguées sont nommées hydrogénotartronate, HOOC-CH(OH)-COO− et tartronate, −OOC-CH(OH)-COO− et peuvent former des sels et des esters.
Synthèse
L'acide tartronique est peu ou pas présent dans la nature, mais peut être obtenu par hydrolyse de l'acide bromomalonique en présence d'hydroxyde d'argent.
Utilisation
L'acide tartronique est utilisé pour obtenir par oxydation catalytique sur platine-bismuth dans l'air pour obtenir l'acide mésoxalique[5].
Dérivés
Son dérivé 2-méthylé est connu sous le nom d'acide isomalique.


