Decavanadato de sódio
| Decavanadato de sódio Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
| Nome IUPAC | Decavanadato de sódio |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | Na6[V10O28] |
| Massa molar | 1419.6 g |
| Aparência | sólido laranja |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Decavanadato de sódio (Na6[V10O28]) é um composto inorgânico. É o sal de sódio do ânion decavanadato, [V10O28]6−.Decavanadato é o único dentre os vanadatos que forma uma solução aquosa de coloração laranja.[1] Numerosos sais de decavanadato e derivados têm sido isolados e estudados desde 1956 quando foi caracterizado pela primeira vez.[2]
Preparação
A preparação do decavanadato é conseguido por acidificação de uma solução aquosa de vanadato.[1]
- 10 Na3[VO4]·nH2O + 24 HOAc → Na6[V10O28]·18 H2O + 24 NaOAc
A formação do decavanadato é otimizada pelo controle de pH entre 4 e 7. O produto pode ser purificado através de recristalização em água. Subprodutos típicos incluem metavanadato, [VO3]−, e hexavanadato, [V6O16]2−.[1]
Estrutura

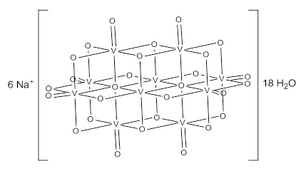
O íon decavanadato consiste em seis octaedros de VO6 fundidos e possui simetria D2h.[3][4][5] A estrutura do Na6[V10O28]·18H2O foi confirmada com a cristalografia de raio X.[6]
Os ânions de decavanadato contêm três grupos de átomos de vanádio equivalentes (ver fig. 1).[3] Inclui dois octaédros centrais de VO6 (Vc) e quatro grupos tetragonais-piramidais periféricos de VO5 (Va and Vb). Existem sete grupos de átomos de oxigênio (assinalado de A ao G). Dois desses (A) se ligam aos V dos centros, quatro (B) se ligam aos V dos centros, quatorze (C, D e E) entre os limites das arestas dos pares de V centrais, e por fim (F and G) estão em posição periférica.
O estado de oxidação do vanádio em decavanadato é +5. Vanádio pode agir como agente oxidante e forma vanádio(IV) ou vanádio(III).[7] A exposição ao ar mantém o vanadato, tornando-os compostos estáveis.[7]
Decavanadatos relacionados
Muitos sais de decavanadato estão sendo caracterizados. NH4+, Ca2+, Ba2+, Sr2+, e sais de decavanadato com cátions do grupo I estão sendo praparados por reação ácido-base entre V2O5 e o óxido, hidróxido, carbonato, ou hidrogenocarbonato dos cátions desejados.[1]
- 6NH3 + 5V2O5 + 3H2O ⇌ (NH4)6[V10O28]
Outros decavanadatos:

