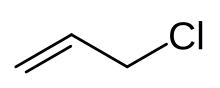
Clorură de alil
| Clorură de alil | |
 | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 107-05-1 |
| ChEMBL | CHEMBL451126 |
| PubChem CID | 7850 |
| Formulă chimică | C₃H₅Cl[1] |
| Masă molară | 76 u.a.m.[2] |
| Proprietăți | |
| Densitate | 1 g/cm³[3] |
| Punct de topire | −210 Fahrenheit[3] |
| Punct de fierbere | 113 Fahrenheiti[3] |
| Solubilitate | 0 gram per 100 gram of solvent[3] |
| Presiune de vapori | 295 mm Hg[3] |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Clorura de alil este un compus organic cu formula chimică CH2=CHCH2Cl, fiind un derivat clorurat al propilenei. Este un lichid incolor și insolubil în apă dar solubil în solvenți organici comuni. Este utilizată pentru obținerea epiclorohidrinei și a materialelor plastice dar este și un agent alchilant.[4]
Obținere
În laborator
Clorura de alil a fost obținută pentru prima dată în anul 1857 de către Auguste Cahours și August Hofmann în urma reacției dintre alcoolul alilic și triclorura de fosfor.[5][4] Metodele moderne de sinteză au înlocuit utilizarea triclorurii de fosfor cu acid clorhidric și un catalizator, precum este clorura cuproasă.[6]
La nivel industrial
Clorura de alil este obținută la nivel industrial în urma reacției de substituție alilica a propilenei cu Cl2. La temperaturi mai mici, prdusul principal de reacție este 1,2-dicloropropanul, dar la temperatura de 500 °C, predomină formarea clorurii de alil, reacția decurgând printr-un mecanism radicalic:
S-a estimat că în anul 1997 aproximativ 800.000 de tone au fost produse prin această metodă.[4]
Proprietăți chimice
Mare parte din clorura de alil este convertită la epiclorohidrină.[4] Alți derivați ai săi importanți din punct de vedere comercial sunt: alcool alilic, alilamină, izotiocianat de alil,[7] și 1-bromo-3-cloropropan.
Ca agent alchilant, este utilizată în obținerea produselor farmaceutice și pesticidelor.
Exemple de reacții
Un exemplu ilustrativ pentru reactivitatea clorurii de alil este reacția de obținere a cianurii de alil (CH2=CHCH2CN).[8] De asemenea, fiind un derivat halogenat reactiv, clorura de alil suferă o reacție de cuplare formând dialilul sau 1,5-hexadiena:[9]
Suferă și reacții de adiție oxidativă la paladiu metalic, dând un dimer denumit clorură de alil-paladiu: (C3H5)2Pd2Cl2. Prin dehidrohalogenare dă ciclopropenă.

