Trombin
Trombin (EC 3.4.21.5, fibrinogenaza, trombaza, trombofort, trombin-C, tropostazin, aktivirani faktor zgrušavanja krvi II, faktor zgrušavanja krvi IIa, faktor IIa, E-trombin, beta-trombin, gama-trombin) jest serin-proteaza, enzim koji je kod ljudi kodiran genom F2 sa hromosoma 11.[5][6] Protrombin (faktor zgrušavanja II) se proteolitski cijepa kako bi se formirao trombin u proces zgrušavanja. Trombin zauzvrat djeluje kao serinska proteaza koja pretvara rastvorljivi fibrinogen u netopive niti fibrina, katalizirajući i mnoge druge reakcije povezane sa koagulacijom.
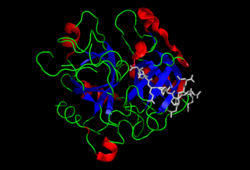
Struktura

Molekulska težina protrombina je približno 72.000 Da. Katalitski domen se oslobađa iz protrombinskog fragmenta 1.2, kako bi se stvorio aktivni enzim trombin, koji ima molekulsku težinu od 36.000 Da. Strukturno, član je velikog PA-klana proteaza.
Protrombin se sastoji od četiri domena; N-terminal Gla domen, dva Kringelova domen]]a i C-terminalni tripsinu-sličan domen serin-proteaza.Faktor Xa sa faktorom V kao kofaktorom dovodi do cijepanja Gla i dva Kringleova domena (formirajući zajedno fragment nazvan fragment 1.2) i ostavlja trombin, koji se sastoji isključivo od domen serinske proteaze.[8]
Kao što je slučaj sa svim serin-proteazama, protrombin se pretvara u aktivni trombin proteolizom unutrašnje peptidne veze, izlažući novi N-terminalni Ile-NH3. Historijski model aktivacije serinskih proteaza uključuje inserciju ovog novoformiranog N-kraja teškog lanca u β-barelsko podsticanje ispravne konformacije katalitskih ostataka.[9] Za razliku od kristalnih struktura aktivnog trombina, studije masene spektrometrije razmjene vodika i deuterija pokazuju da se ovaj N-terminalni Ile-NH3 ne ubacuje u β-barel u apo obliku trombina. Međutim, čini se da vezivanje aktivnog fragmenta trombomodulina alosterno promoviše aktivnu konformaciju trombina insercijom ovog N-terminalnog regiona.[10]
Gen
Gen za trombin (protrombin) nalazi se na hromosomu 11, regija p11-q12.[5]
Procjenjuje se da u svijetu postoji oko 30 ljudi kojima je dijagnosticiran urođeni oblik nedostatka faktora II,[11] koji ne treba brkati sa mutacijom protrombin G20210A, koja se također naziva mutacijom faktora II. Prothrombin G20210A je urođen.[12]
Protrombin G20210A obično nije praćen drugim mutacijama faktora (tj. najčešći je faktora V Leiden). Gen može biti naslijeđen heterozigotno (1 par), ili mnogo rjeđe, homozigotno (2 para), i nije povezan sa spolom ili krvnom grupom. Homozigotne mutacije povećavaju rizik od tromboze više od heterozigotnih mutacija, ali relativno povećan rizik nije dobro dokumentiran. Ostali potencijalni rizici za trombozu, kao što su oralni kontraceptivi mogu biti dodatni. Prethodno prijavljeni odnos upalne bolesti crijeva (tj. Crohnova bolest ili ulcerozni kolitis) i mutacije protrombina G20210A ili faktor V Leidenove mutacije je suprotstavljen istraživanjima.[13]
Aminokiselinska sekvenca
Dužina polipeptidnog lanca je 622 aminokiseline, a molekulska težina 70.037 Da.
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MAHVRGLQLP | GCLALAALCS | LVHSQHVFLA | PQQARSLLQR | VRRANTFLEE | ||||
| VRKGNLEREC | VEETCSYEEA | FEALESSTAT | DVFWAKYTAC | ETARTPRDKL | ||||
| AACLEGNCAE | GLGTNYRGHV | NITRSGIECQ | LWRSRYPHKP | EINSTTHPGA | ||||
| DLQENFCRNP | DSSTTGPWCY | TTDPTVRRQE | CSIPVCGQDQ | VTVAMTPRSE | ||||
| GSSVNLSPPL | EQCVPDRGQQ | YQGRLAVTTH | GLPCLAWASA | QAKALSKHQD | ||||
| FNSAVQLVEN | FCRNPDGDEE | GVWCYVAGKP | GDFGYCDLNY | CEEAVEEETG | ||||
| DGLDEDSDRA | IEGRTATSEY | QTFFNPRTFG | SGEADCGLRP | LFEKKSLEDK | ||||
| TERELLESYI | DGRIVEGSDA | EIGMSPWQVM | LFRKSPQELL | CGASLISDRW | ||||
| VLTAAHCLLY | PPWDKNFTEN | DLLVRIGKHS | RTRYERNIEK | ISMLEKIYIH | ||||
| PRYNWRENLD | RDIALMKLKK | PVAFSDYIHP | VCLPDRETAA | SLLQAGYKGR | ||||
| VTGWGNLKET | WTANVGKGQP | SVLQVVNLPI | VERPVCKDST | RIRITDNMFC | ||||
| AGYKPDEGKR | GDACEGDSGG | PFVMKSPFNN | RWYQMGIVSW | GEGCDRDGKY | ||||
| GFYTHVFRLK | KWIQKVIDQF | GE |
Sinteza
Trombin se proizvodi enzimskim cijepanjem dva mjesta na protrombinu aktiviranim faktorom X (Xa). Aktivnost faktora Xa je znatno poboljšana vezivanjem za aktivirani faktor V (Va), nazvan protrobinazni kompleks. Protrombin se proizvodi u jetri i kotranslacijski modificira u reakciji ovisnoj o vitaminu K koja pretvara 10-12 glutaminskih kiselina na N-kraju molekule u gama-karboksiglutaminsku kiselinu (Gla).[14] U prisustvu kalcija, Gla ostaci pospešuju vezivanje protrombina za fosfolipidne dvoslojeve. Nedostatak vitamina K ili primjena antikoagulansa varfarina inhibira proizvodnju ostataka gama-karboksiglutaminske kiseline, usporavajući aktivaciju koagulacijske kaskade.
Kod odraslih ljudi, normalan nivo aktivnosti antitrombina u krvi je izmjeren na oko 1,1 jedinica/mL. Nivo trombina u novorođenčadi se stalno povećava nakon rođenja, kako bi dostigao normalne nivoe kod odraslih, od nivoa od oko 0,5 jedinica/ml 1 dan nakon rođenja, do nivoa od oko 0,9 jedinica/ml nakon 6 mjeseci života.[15]
Klinički značaj
Aktivacija protrombina je ključna u fiziološkoj i patološkoj koagulaciji. Opisane su različite rijetke bolesti koje uključuju protrombin (npr. hipoprotrombinemija). Antiprotrombinska antitela u autoimunskoj bolesti može biti faktor u formiranju lupus-antikoagulansa (također poznatog kao antifosfolipidni sindrom). Hiperprotrombinemija može biti uzrokovana mutacijom G20210A.
Trombin, snažan vazokonstriktor i mitogen, uključeni su kao glavni faktori u vazospazamu nakon subarahnoidalnog krvarenja. Krv iz rupture moždane aneurizme zgrušava se oko cerebralnih arterija, oslobađajući trombin. Ovo može izazvati akutno i produženo sužavanje krvnog suda, što može dovesti do cerebralne ishemije i infarkta (moždani udar).
Osim ključne uloge u dinamičkom procesu stvaranja tromba, trombin ima izražen proupalni karakter, koji može uticati na nastanak i napredovanje ateroskleroze. Djelujući preko svojih specifičnih receptora na ćelijskoj membrani (receptora aktiviranih proteazom: PAR-1, PAR-3 i PAR-4), koji su obilno eksprimirani u svim sastojcima zidova arterijskih sudova , trombin ima potencijal da ispoljava proaterogeno djelovanje kao što su upala, regrutacija leukocita u aterosklerotski plak, pojačani oksidativni stres, migracija i proliferacija vaskularnih glatkih mišićnih ćelija, apoptoza i angiogeneza.[16][17][18]
Trombin je uključen u fiziologiju krvnih ugruška. Njegovo prisustvo ukazuje na postojanje ugruška. U 2013. godini razvijen je sistem za detekciju prisustva trombina kod miševa. Kombinira peptidom obložen gvožđe-oksid povezan sa "reporterskim hemikalijama". Kada se peptid veže za molekulu trombina, oslobađa se reporter i pojavljuje u urinu, gdje se može otkriti. Testiranje na ljudima nije sprovedeno.[19]
Također pogledajte
- Kerastocitin
- Fibrinsko ljepilo
- Fibrinogen
- Proteaza
- Mapa proteolize
- Test stvaranja trombina
Reference
Dopunska literatura
Vanjski linkovi
- The MEROPS online database for peptidases and their inhibitors: S01.217 Arhivirano 19. 9. 2019. na Wayback Machine
- Kujovich JL (februar 2021). Adam MP, Ardinger HH, Pagon RA, et al. (ured.). "Prothrombin Thrombophilia". GeneReviews. Seattle WA: University of Washington, Seattle. PMID 20301327. NBK1148.
- Anti-coagulation & proteases na YouTubeu by The Proteolysis Map-animation
- [1] PMAP: The Proteolysis Map/Thrombin
- Thrombin: RCSB PDB Molecule of the Month Arhivirano 5. 10. 2013. na Wayback Machine
- Prothrombin Structure
- PDBe-KB provides an overview of all the structure information available in the PDB for Human Thrombin.
- PDBe-KB provides an overview of all the structure information available in the PDB for Mouse Thrombin.