Ciklobutadién
| ciklobutadién | |||
 ciklobutadién | 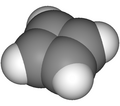 | ||
| IUPAC-név | 1,3-ciklobutadién | ||
| Más nevek | ciklobutadién [4]annulén | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 1120-53-2 | ||
| PubChem | 136879 | ||
| ChemSpider | 120626 | ||
| ChEBI | 33657 | ||
| |||
| |||
| InChIKey | HWEQKSVYKBUIIK-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H4 | ||
| Moláris tömeg | 52,07 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A ciklobutadién telítetlen gyűrűs szénhidrogén, összegképlete C4H4. A legegyszerűbb [n]-annulén ([4]-annulén), rendkívül instabil, szabad állapotban élettartama nem éri el az öt másodpercet.[forrás?]
Bár molekulájában váltakozva egyes és kettős kötések találhatók, a Hückel-szabály szerint antiaromás karakterű, instabil, triplett állapotú részecske,[1] mivel gyűrűjében 4 π-elektron található. Egyes ciklobutadién-fém komplexek stabil vegyületek, aminek feltehetően az az oka, hogy a fématom további két elektront juttat a rendszerbe. A szingulett alapállapothoz képest torzult, nem planáris szerkezetet a Jahn–Teller-effektus okozza.[2] Tetra-t-butil szubsztituált származéka kellően stabil ahhoz, hogy szerkezetét röntgenkrisztallográfiával meg lehessen határozni, a kapott adatok alapján konfigurációja torzult, nem síkalkatú, benne a kettős kötések a szokásosnál hosszabbak (146,4 pm a várt 134 pm helyett).[3]
Pi-elektronrendszere magasabb energiájú, mint nyílt láncú megfelelőjében, az 1,3-butadiénben, ezért nem aromás, hanem antiaromás vegyületnek nevezzük. Elektronállapotait számos számítógépes eljárással vizsgálták.[4] A szingulett alapállapot téglalap alakú. Az első gerjesztett állapot egy négyzetes geometriájú triplett állapot. A téglalap szerkezet összhangban van azzal a megfigyeléssel, hogy két különböző 1,2-dideuterio-1,3-ciklobutadién sztereoizomer létezik. Ez azt mutatja, hogy a pi elektronok lokalizáltak, tehát nem tekinthető aromásnak. A ciklobutadién rendkívül instabil, nagyon reakcióképes és rövid élettartamú vegyület. Diels–Alder-reakció révén 35 K-en dimerizálódik.[forrás?] Monomer formájában magasabb hőmérsékleten nemesgáz mátrixizolációs eljárással tanulmányozták.[forrás?]
Előállítása
Számos próbálkozás után először 1965-ben szintetizálta Rowland Pettit és csoportja, de a kapott anyagot nem sikerült elkülöníteniük. Ciklobutadiént a fémvegyületeinek bontásával, például ciklobutadién-vas-trikarbonilnak ammónium-cérium(IV)-nitrátos reakciójával lehet nyerni. A ciklobutadién-vas-trikarbonil komplexet Fe2(CO)9-ből és cisz-diklórciklobuténből állították elő kettős dehidrohalogénezéssel.[5][6]
A vaskomplexből felszabaduló ciklobutadién reagál elektronban szegény alkinekkel, melynek során Dewar-benzol keletkezik:[7]
A Dewar-benzol 90 °C-on melegítve dimetil-ftaláttá alakul át.
Fordítás
Ez a szócikk részben vagy egészben a Cyclobutadiene című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
