Tropon
| Tropon[1] | |||
 A tropon szerkezete |  A tropon kalottamodellje | ||
| Más nevek | Ciklohepta-2,4,6-triénon | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 539-80-0 | ||
| PubChem | 10881 | ||
| ChemSpider | 10419 | ||
| |||
| |||
| InChIKey | QVWDCTQRORVHHT-UHFFFAOYSA-N | ||
| UNII | CO48X7SUFH | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C7H6O | ||
| Moláris tömeg | 106,12 g/mol | ||
| Sűrűség | 1,094 g/ml | ||
| Forráspont | 113 °C | ||
| Veszélyek | |||
| Lobbanáspont | >113 °C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A tropon (IUPAC-név: ciklohepta-2,4,6-trién-1-on) nem benzoid aromás szerves vegyület.[2] 7 szénatomos gyűrűből áll három konjugált kettős kötéssel és ketocsoporttal. A hasonló tropolon (2-hidroxiciklohepta-2,4,6-trién-1-on) további alkohol (vagy enol) csoporttal rendelkezik a keton mellett. A troponok ritkák a természetes környezetben, kivéve a 2-hidroxiszármazékokat, a tropolonokat.
A tropon 1951 óta ismert, és nevezik cikloheptatrienílium-oxidnak is. A tropolon nevet M. J. S. Dewar alkotta 1945-ben az érzékelt aromásság miatt.[3]
Jellemzők
Dewar 1945-ben feltételezte, hogy a troponok aromásak lehetnek. A karbonilcsoport a triéngyűrű révén jobban polarizált, részleges pozitív töltést adva a szénatomnak és részleges negatívat az oxigénnek (A). Szélsőséges esetben a szén töltése teljes (B), tropíliumiont adva, mely aromás 6 elektronos rendszer (C).
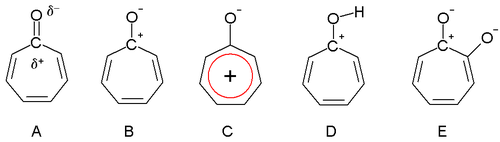
A troponok bázikusak (D) is lehetnek az aromás stabilizáció révén. Ez a savakkal való könnyű sóképződésben is megjelenik. A tropon dipólusmomentuma 4,17 D, szemben a cikloheptanon 3,04 D-ével. A különbség a dipoláris rezonanciaszerkezet stabilizációjával konzisztens.
Szintézis
Számos mód van troponok és troponszármazékok szintézisére. Két gyakori módszer erre a cikloheptatrién szelén-dioxidos oxidációja[4] és a tropinonból Hofmann-eliminációval és brómozással közvetve történő út.[2]
A tropon előállítható továbbá brómbenzolból diazometánnal UV-fényben. Ez brómtropilidént ad, ami brómozással és hidrogén-bromid-eliminációval brómtropílium-bromidot ad, melynek hidrolízisekor tropon keletkezik.[5]

Reakciók
Magas hőmérsékleten kálium-hidroxidban a tropon gyűrűszűkülésen megy át benzoesavat adva. Sok származék szintén a megfelelő arénné szűkül.[2] A tropon elektrofil szubsztitúcióban reagál például brómmal, de ez az 1,2-addíciós terméken megy keresztül, és nem aromás elektrofil szubsztitúció.[2]

A troponszármazékok a nukleofil aromás szubsztitúcióhoz hasonló nukleofil szubsztitúcióban is reagálnak.[2]
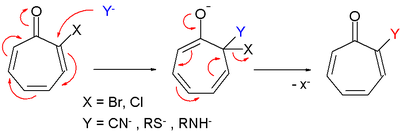
A tropon [8+3]annuláción megy át fahéjaldehiddel.[6]

Diénkarakter
A tropon diénként működik Diels–Alder-reakciókban például maleinsav-anhidriddel.[2] Vas-trikarbonillal a (butadién)vas-trikarbonilhoz hasonló adduktumokat képez.[7]
Származékok
| Név | Szerkezet | Természetes források |
|---|---|---|
| Tropolon |  | Pseudomonas lindbergii, Pseudomonas plantarii[8] |
| Hinokitiol |  | Cupressaceae-fák[9] |
| Stipitatinsav |  | Talaromyces stipitatus[10] |
| Tropoditietinsav |  | Phaeobacter piscinae, Phaeobacter inhibens, Phaeobacter gallaeciensis[11][12] |
| Kolchicin |  | Colchicum autumnale, Gloriosa superba[13] |
További troponszármazékok például a puberulon- és puberulinsav, a rozeobakticidek, a pernambukon, a krototropon és az orobanon.[14][15][16][17][18]
Jegyzetek
Fordítás
Ez a szócikk részben vagy egészben a Tropone című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.