
 | |
 | |
| Називи | |
|---|---|
| IUPAC називs Фосфинска киселина дихидридохидроксидо- оксидофосфор | |
| Идентификација | |
| ECHA InfoCard | 100.026.001 |
| MeSH | Hypophosphorous+acid |
| Својства | |
| H3PO2 | |
| Моларна маса | 66,00 g/mol |
| Густина | 1,274 g/cm³, течност |
| Тачка топљења | 26.5 °C (299,5 K) |
| Тачка кључања | 106 °C (379 K) decomp. |
| помешљива | |
| Киселост (pKa) | 1.2 |
| Структура | |
| Облик молекула (орбитале и хибридизација) | псеудо-тетраедарна |
| Опасности | |
ЕУ класификација (DSD) | not listed |
| Сродна једињења | |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
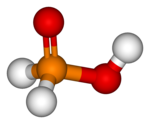
Хипофосфораста киселина је фосфорова кисеонична киселина и врло јако редукционо средство формуле H3PO2. Неоргански хемичари ову киселину зову управо тако (такође „ХПК") иако је IUPAC-ово име дихидридохидроксидооксидофосфор или само фосфинска киселина. Она је безбојно једињење које се брзо топи, раствара у води, диоксану и алкохолима. Формула за хипофосфорасту киселину је обично H3PO2 али мало детаљнији запис би био HOP(O)H2 који показује једнобазни карактер. Соли ове киселине су фосфинати (хипофосфити).[1][2]
HOP(O)H2 постоји заједно са мањим таутомером HP(OH)2. Понекад је тај таутомер тумачен као хипофосфораста киселина а главни као фосфинска киселина.
Иначе, хипофосфорастој киселини припада анхидрид фосфор(III)-оксид. Главна киселина у овој групи је фосфораста киселина.
Индустријски, ова киселина се добија у два корака. Хипофосфити алкалних метала и земноалкалних метала се добијају деловањем фосфора са раствором одређеног хидроксида, нпр. Ca(OH)2.
Чиста киселина се припрема деловањем јаких киселина на хипофосфитне соли.
Алтернативно, H3PO2 се добија оксидацијом фосфина са јодом у води.
Хипофосфораста киселина је обично доступна у облику 50% раствора.
Хипофосфораста киселина се користи у прављењу фармацеутских производа, обезбојавању полимера и у добијању племенитих или негвоздених метала. Главна употреба јој је у неелектроном поплочавању. Другим речима, у избацивању одабраних металних премаза на осетљивим површинама. У органској хемији, H3PO2 је најбоље знана по редукцији диазонијумских соли претварањем ArN2+ у Ar-H.[3][4] Када је у диазотованом концентрованом раствору хипофосфорасте киселине амински супституент, он се може уклонити из арена, углавном алкил-арена.
Разни деривати су познати код два водоникова атома директно везана за фосфор јер могу бити замењени разним органским групама. Ови деривати су познати под називом фосфинских киселина а њихове соли под називом фосфината. На пример, формалдехид и H3PO2 реагују да би дали (HOCH2)2PO2H. Производ реакције је сродан оном код додавања тиола и HCN алдехидима. Слично томе, додаје се на Мајклове примаоце, нпр. са акриламидом даје H(HO)P(O)CH2CH2C(O)NH2.
Пар комплекса метала су настали од H3PO2 а један пример је Ni(O2PH2)2.
Једињења фосфора | |
|---|---|
Једињења водоника | |
|---|---|
H3AsO3 · H3AsO4 · HAt · HSO3F · H3BO3 · HBF4 · HBr · HBrO · HBrO2 · HBrO3 · HBrO4 · HCl · HClO · HClO2 · HClO3 · HClO4 · HCN · HCNO · H2CrO4/H2Cr2O7 · H2CO3 · H2CS3 · HF · HFO · HI · HIO · HIO2 · HIO3 · HIO4 · H2MoO4 · H2MnO4 · HNC · HNCO · HNO · HNO3 · H2N2O2 · HNO5S · H3NSO3 · H2O · H2O2 · H2O3 · H3PO2 · H3PO3 · H3PO4 · H4P2O7 · H5P3O10 · H2PtCl6 · H2S · H2Se · H2SeO3 · H2SeO4 · H4SiO4 · H2SiF6 · H2SO3 · H2SO4 · H2SO5 · H2S2O3 · H2S2O6 · H2S2O7 · H2S2O8 · CF3SO3H · H2Te · H2TeO3 · H6TeO6 · H4TiO4 · H2Po · H3VO4 · HCo(CO)4 |