Линезолид
Линезолид (МНН) — синтетический антибиотик, используемый для лечения тяжёлых инфекционных заболеваний, вызванных грамположительными бактериями, которые устойчивы к другим антибиотикам. Представитель класса оксазолидинонов, линезолид является активным по отношению к большинству грамположительных бактерий, которые вызывают болезни, включая стрептококки, устойчивые к ванкомицину энтерококки и метициллин-резистентный золотистый стафилококк.[1] Основными показаниями линезолида являются инфекционные заболевания кожи, мягких тканей и пневмония (в частности, госпитальная пневмония), хотя становится популярным его использование при различных других инфекционных заболеваниях.
| Линезолид | |
|---|---|
 | |
 | |
| Химическое соединение | |
| ИЮПАК | (S)-N-({3-[3-фторо-4-(морфонил-4-ил)фенил]-2-оксо-1,3-оксазолидин-5-ил}метил)ацетамид |
| Брутто-формула | C16H20FN3O4 |
| Молярная масса | 337.346 г/моль |
| CAS | 165800-03-3 |
| PubChem | 441401 |
| DrugBank | APRD01073 |
| Состав | |
| Классификация | |
| АТХ | J01XX08 |
| Фармакокинетика | |
| Биодоступн. | ~100 % (перорально) |
| Связывание с белками плазмы | низкая (31 %) |
| Метаболизм | в печени (50-70 %, CYP not involved) |
| Период полувывед. | 4.2-5.4 ч (короче у детей) |
| Экскреция | непочечная, почками и с калом |
| Лекарственные формы | |
| гранулы для приготовления суспензии для приёма внутрь; раствор для инфузий; таблетки, покрытые плёночной оболочкой. | |
| Способы введения | |
| внутривенное, пероральное | |
| Другие названия | |
| Зивокс® (Zivox®), Амизолид (Amizolid), Зеникс (Zenix), Линезолид-Тева (Linezolid-Teva) | |
Открытый в 1990-х годах и впервые одобренный для использования в 2000 году, линезолид был первым, и до 2014 года единственным, коммерчески доступным антибиотиком класса оксазолидинона. В 2014 году в США был одобрен к применению следующий антибиотик этого класса — тедизолид. Как ингибитор синтеза белков, линезолид останавливает рост бактерий, нарушая у них биосинтез белка. Хотя многие антибиотики действуют подобным образом, точный механизм действия линезолида представляется уникальным для класса оксазолидинонов. Устойчивость бактерий к линезолиду остаётся очень низкой (первые сообщения были в 1999 году), однако она может возрасти.
При приёме внутрь в течение коротких периодов линезолид относительно безопасен; он может быть использован у пациентов всех возрастов и у людей с заболеваниями печени или почечной недостаточностью. Общие побочные эффекты краткосрочного приёма включают головную боль, диарею и тошноту. Длительное применение, однако, связано с серьёзными побочными эффектами; линезолид может вызвать подавление функции костного мозга и тромбоцитопению, особенно при его использовании более двух недель. Применение линезолида на более длительный период может привести к периферической невропатии (которая может быть необратимой), поражению зрительного нерва и лактатацидозу (накопление молочной кислоты в организме). Всё это возникает, скорее всего, в связи с токсическим поражением митохондрий.
Линезолид является достаточно дорогим препаратом, а курс лечения может стоить до нескольких тысяч долларов США;[2] тем не менее, он представляется более рентабельным, чем сопоставимые антибиотики,[3] главным образом в связи с возможностью перехода от внутривенного на пероральный метод введения, как только состояние пациента стабилизируется, без необходимости коррекции доз.
История
Оксазолидиноны были известны как ингибиторы моноаминоксидазы с конца 1950-х годов. Их антибактериальные свойства были обнаружены исследователями E.I. duPont de Nemours в 1970-х годах.[4] В 1978 году DuPont запатентовала ряд производных оксазолидинона как эффективные в лечении бактериальных и грибковых заболеваний растений, а в 1984 году другой патент описал их эффективность в лечении бактериальных инфекций у млекопитающих.[4][5] В 1987 году учёные DuPont представили подробное описание оксазолидинонов как новый класс антибиотиков с новым механизмом действия.[4][6] Однако обнаружилось, что синтезированные в те времена соединения были токсичны для печени и разработки были прекращены.[7]
Компания Pharmacia & Upjohn (теперь часть Pfizer) начала свою собственную программу исследований оксазолидинона в 1990-х годах. Исследования соединений «структура-активность» привели к разработке нескольких подклассов производных оксазолидинона с различными профилями безопасности и антимикробной активности. Два соединения рассматривались как кандидаты в лекарства: эперезолид (кодовое название PNU-100592) и линезолид (PNU-100766).[8][9] На доклинических стадиях разработок они были схожи по антибактериальной активности и безопасности, поэтому они перешли в фазу I клинических испытаний с целью выявления любых различий в фармакокинетике.[7][10] Было обнаружено, что линезолид имеет фармакокинетические преимущества. Его можно принимать только два раза в день, в то время как эперезолид необходимо принимать 3 раза в день для достижения аналогичного эффекта. Поэтому линезолид был выбран для дальнейших исследований.[8] FDA разрешило применение линезолида 18 апреля 2000 года.[11] В последующим препарат был разрешён в Бразилии (июнь 2000 г.),[12] Великобритании (январь 2001),[9][13] Японии и Канаде (апрель 2001),[14][15][16] Европе (в течение 2001 года),[17] и в других странах Латинской Америки и Азии.[15]
На сегодняшний день (февраль 2019 года) линезолид — один из двух антибиотиков-оксазолидинонов, доступных на фармакологическом рынке (вместе с тедизолидом).[18] Другие представители этого класса в стадии разработки, например посизолид (AZD2563),[19] ранбезолид (RBX 7644),[20] торезолид (TR-701),[18][21] и радезолид (RX-1741).[22]
Спектр активности
Линезолид эффективен против всех клинически значимых грамположительных бактерий, клеточная стенка которых содержит толстый слой пептидогликанов и они не имеют наружной мембраны. К ним относят Enterococcus faecium и Enterococcus faecalis (включая ванкомицин-устойчивые энтерококки), золотистый стафилококк (включая метициллин-устойчивый золотистый стафилококк, англ. MRSA), Streptococcus agalactiae, пневмококк, Streptococcus pyogenes, зеленящие стрептококки, Listeria monocytogenes и Corynebacterium (последние наиболее восприимчивы к линезолиду с минимальной ингибирующей концентрацией обычно ниже 0,5 мг/л).[1][5][23] Линезолид также весьма активен in vitro против некоторых микобактерий.[5] Предполагают, что он очень эффективен против Nocardia, но из-за высокой стоимости и потенциально серьёзных побочных эффектов, авторы рекомендовали комбинировать с другими антибиотиками или применять только как резервный антибиотик в случаях, когда традиционное лечение не эффективно.[24]
Считают, что линезолид обладает бактериостатическим действием против большинства микроорганизмов (то есть, он останавливает их рост и размножение, фактически не убивая их), но также обладает бактерицидным действием в отношении стрептококков.[1][25] Некоторые авторы отмечают, что, несмотря на его бактериостатическое действие in vitro, линезолид «ведёт себя» как бактерицидный антибиотик in vivo, поскольку он ингибирует образование токсинов стафилококков и стрептококков.[8] Он также обладает постантибиотиковым действием на большинство бактерий от одного до четырёх часов, что означает временное подавление роста бактерий даже после прекращения приёма препарата.[26]
Грамотрицательные бактерии
Линезолид не имеет клинически значимого действия на большинство грамотрицательных бактерий. Pseudomonas и энтеробактерии, например, не восприимчивы к его действию.[25] In vitro он активен в отношении Pasteurella multocida,[1][27] фузобактерий, Moraxella catarrhalis, легионелл, бордетелл, Elizabethkingia meningoseptica и умеренно активен (с минимальной подавляющей концентрацией для 90 % штаммов 8 мг/л) в отношении гемофильной инфекции.[25][28] Линезолид также показал хороший эффект как препарат второй линии для лечения инфекций Capnocytophaga.[29][30]
Подобные антибиотики
Спектр активности линезолида в отношении грамположительных бактерий похож на спектр гликопептидного антибиотика ванкомицина, который уже давно входит в стандарт лечения инфекций MRSA и эти 2 препарата часто сравнивают.[26][31] К другим подобным антибиотикам относят тейкопланин, квинупристин/дальфопристин (Synercid, сочетание двух стрептограминов, не активен в отношении Е. faecalis)[7] и даптомицин (Cubicin, липопептид). Также некоторые препараты находятся на стадии разработки, такие как цефтобипрол, далбаванцин и телаванцин. Только линезолид можно применять перорально.[26] В будущем оритаванцин и иклаприм могут стать альтернативой пероральной форме линезолида. Оба препарата находятся на ранней стадии клинических разработок.[26]
Показания
Основное показание линезолида — лечение тяжёлых инфекций, вызванных грамположительными бактериями, устойчивыми к другим антибиотикам. Препарат не должен применяться против бактерий, которые чувствительны к антибиотикам с более узким спектром действия, таким как пенициллины и цефалоспорины. В популярной прессе и научной литературе, линезолид был назван «резервным антибиотиком», который следует использовать с осторожностью как препарат «последней инстанции» в отношении потенциально неразрешимых инфекций.[32][33]
В США, FDA-утверждёнными показаниями для использования линезолида являются: ванкомицин-устойчивые энтерококковые инфекции с или без бактериемии; госпитальные и внегоспитальные пневмонии, вызванные золотистым стафилококком или пневмококком; осложнённые кожные инфекции (англ. cSSSI), вызванные чувствительными бактериями, в том числе инфекции диабетической стопы, если осложняется остеомиелитом, и неосложнённые инфекции кожи и мягких тканей, вызванные S. pyogenes или золотистым стафилококком. Производитель не рекомендует использование линезолида при внегоспитальных пневмониях или неосложнённых инфекциях кожи и мягких тканей, вызванных MRSA.[1] В Великобритании пневмония и cSSSI — единственные показания, отмеченные в маркировке продукции.[13]
Полагают, что линезолид безопасен и эффективен для применения у детей и новорождённых так же, как и у взрослых.[26]
Инфекции кожи и мягких тканей
Крупный мета-анализ рандомизированных контролируемых исследований показал, что линезолид эффективнее гликопептидных антибиотиков (например, ванкомицина и тейкопланина) и бета-лактамных антибиотиков, при лечении инфекций кожи и мягких тканей (англ. SSTIs), вызванных грамположительными бактериями[34]. Также небольшие исследования подтвердили превосходство линезолида над тейкопланином при лечении всех тяжёлых грамположительных инфекций.[35]
При лечении синдрома диабетической стопы, линезолид, как полагают, дешевле и эффективнее ванкомицина.[36] В открытом исследовании 2004 года линезолид был также эффективен, как и ампициллин/сульбактам, ко-амоксиклав и намного эффективнее у пациентов с язвами нижних конечностей и без остеомиелита, но со значительно более высоким уровнем побочных эффектов.[37][38] Однако мета-анализ 2008 года 18 рандомизированных контролируемых исследований показал, что лечение линезолидом бывает неэффективным так же часто, как и лечение другими антибиотиками, независимо от наличия или отсутствия у больного остеомиелита.[39]
Некоторые авторы рекомендуют применение комбинации более дешёвых и более экономически эффективных препаратов (например, ко-тримоксазола с рифампицином или клиндамицином) перед назначением линезолида при лечении SSTI, когда восприимчивость возбудителя это позволяет.[38][40]
Пневмония
Как полагают, нет существенной разницы в отношении эффективности лечения между линезолидом, гликопептидами или соответствующими бета-лактамными антибиотиками при лечении пневмонии.[34] Клинические руководства по лечению внегоспитальной пневмонии, разработанные Американским торакальным обществом и Обществом инфекционных заболеваний Америки, рекомендуют линезолид как резервный антибиотик для случаев, когда MRSA подтверждена как возбудитель или когда предполагается MRSA инфекция на основе клинических проявлений.[41] Руководство Британского торакального общества не рекомендует его для лечения первой линии, а скорее как альтернативу ванкомицину.[42] Линезолид также приемлем как препарат второй линии при лечении внегоспитальной пневмококковой пневмонии, когда существует устойчивость к пенициллину.[41]
Руководства США рекомендуют как линезолид, так и ванкомицин в качестве препарата первой линии для лечения госпитальных (нозокомиальных) пневмоний MRSA.[43] Некоторые исследования показали, что линезолид лучше, чем ванкомицин против внутригоспитальных пневмоний, особенно вентилятор-ассоциированной пневмонии[англ.], вызванной MRSA, возможно потому, что проникновение линезолида в бронхиальную жидкость значительно выше, чем ванкомицина. Однако поднятые несколько вопросов по дизайну исследования ставят под сомнение результаты, которые указывают на превосходство линезолида.[38] Несмотря на это, преимущества линезолида включают высокую биодоступность (так как он позволяет легко переходить на пероральную терапию), а также тот факт, что нарушение функции почек не является препятствием для его использования (в то время как достичь правильной дозировки ванкомицина у больных с почечной недостаточностью очень сложно).[43]
Неутверждённые показания
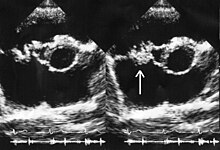
Традиционно считается, что так называемые «глубокие» инфекции, такие как остеомиелит или инфекционный эндокардит, следует лечить бактерицидными антибиотиками, а не бактериостатическими. Тем не менее, доклинические исследования были проведены для оценки эффективности линезолида при этих инфекциях[8] и препарат успешно применяется для их лечения в клинической практике. Полагают, что линезолид является оправданным терапевтическим вариантом для инфекционного эндокардита, вызванного несколькими устойчивыми грамположительными бактериями, несмотря на отсутствие высококачественных доказательств в пользу такого применения.[45][46] Результаты лечения энтерококкового эндокардита варьировали, в некоторых случаях лечение было успешно, а в других ответа на терапию не было.[47][48][49][50][51][52] Доказательства низкого и среднего качества также установили возможность его использования при инфекционных поражениях в костях и суставах, в том числе при хроническом остеомиелите, хотя побочные эффекты вызывают серьёзную озабоченность при длительном применении препарата.[53][54][55][56][57][58]
В сочетании с другими препаратами линезолид был использован для лечения туберкулёза.[59] Оптимальная доза для этой цели не была установлена. У взрослых дозировки 1 и 2 раза в день были использованы с достижением хорошего эффекта. Часто требуется много месяцев лечения и скорость развития побочных эффектов сильно зависит от дозы.[60][61] Недостаточно надёжных доказательств эффективности и безопасности этого показания для постоянного применения.[26]
Линезолид изучен в качестве альтернативы ванкомицину при лечении фебрильной нейтропении у онкологических больных, при подозрении на грамположительную инфекцию.[62] Он также является одним из немногих антибиотиков, которые диффундируют в стекловидное тело и поэтому линезолид может быть эффективен при лечении эндофтальмита, вызванного чувствительными бактериями. Опять же, мало доказательств для его использования при таком состоянии, так как инфекционный эндофтальмит широко и эффективно лечится ванкомицином, который вводится непосредственно в глаз.[38]
Инфекции центральной нервной системы
В исследованиях на животных пневмококкового менингита, было обнаружено, что линезолид хорошо проникает в спинномозговую жидкость, но его эффективность меньше, чем у других антибиотиков.[5][63] Полагают, что не появится достаточное количество доказательств высокого качества в пользу рутинного применения линезолида для лечения бактериального менингита. Тем не менее, линезолид успешно применяется во многих случаях инфекций центральной нервной системы, включая менингит, вызванных чувствительными бактериями, а также он был предложен как оправданный выбор при этих показаниях, когда варианты лечения ограничены или когда другие антибиотики не эффективны.[29][64] Руководство Общества по инфекционным болезням Америки рекомендует линезолид как препарат выбора при менингите VRE и в качестве альтернативы ванкомицину при менингите MRSA.[65] Считают, что линезолид превосходит ванкомицин при лечении внегоспитальной MRSA инфекции центральной нервной системы, хотя и очень мало сообщений было опубликовано о случаях таких инфекций (по состоянию на 2009 год).[66]
Катетер-ассоциированные инфекции
В марте 2007 года, FDA сообщил о результатах рандомизированного открытого клинического испытания в III фазе, где сравнивался линезолид с ванкомицином при лечении катетер-ассоциированных инфекций крови. Пациентам получаемое лечение ванкомицином может быть заменено на оксациллин или диклоксациллин, если бактерии, вызывающие инфекцию, восприимчивы, а пациенты в обеих группах (линезолида и ванкомицина) при необходимости могут получать специфическое лечение в отношении грамотрицательных бактерий.[67] Само исследование было опубликовано в январе 2009 года.[68]
Линезолид ассоциировался с большей смертностью, чем сравниваемые с ним антибиотики. Когда были собраны данные по всем участникам, исследование показало, что 21,5 % из тех, кто получал линезолид, умерли по сравнению с 16 % умерших в группе, где его не получали. Такая разница объясняется недостаточной эффективностью линезолида в лечении только грамотрицательных инфекций или смешанной грамположительной/грамотрицательной инфекции. Только в группе участников с грамположительной инфекцией безопасность и эффективность линезолида и ванкомицина оказались одинаковы.[67][68] В свете этих результатов, FDA издало предупреждение для работников здравоохранения, что линезолид не одобрен для лечения катетер-ассоциированных инфекций или инфекций, вызванных грамотрицательными бактериями.[67]
Побочные эффекты
При использовании в течение короткого периода линезолид является относительно безопасным препаратом.[31] Общие побочные эффекты линезолида (возникающие у более чем 1 % людей, принимающих линезолид) включают диарею (по сведениям, у 3-11 % участников клинических испытаний), головную боль (1-11 %), тошноту (3-10 %), рвоту (1-4 %), сыпь (2 %), запор (2 %), изменение восприятия вкуса (1-2 %) и изменение цвета языка (0.2-1 %).[2] Могут возникать грибковые инфекции, такие как оральный и вагинальный кандидоз, так как линезолид подавляет бактериальную флору в организме и открывает нишу для грибов (так называемый антибиотиковый кандидоз).[2] Менее распространённые (и потенциально более серьёзные) побочные эффекты — аллергические реакции, панкреатит и повышение уровня трансаминаз, что может быть признаком поражения печени.[2][9] В отличие от некоторых антибиотиков, таких как эритромицин, и хинолонов, линезолид не влияет на интервал QT на ЭКГ, который показывает электрическую проводимость сердца.[9][69] У детей побочные эффекты такие, как и у взрослых.[69]
Как почти все антибиотики, линезолид ассоциирован с возникновением Clostridium difficile-ассоциированной диареи (CDAD) и псевдомембранозного колита, хотя последний редок, возникая у одного из двух тысяч пациентов в клинических испытаниях.[2][9][69][70] C. difficile , как полагают, восприимчив к линезолиду in vitro и препарат даже рассматривают для возможного лечения CDAD.[71]
Длительное применение
Подавление функции костного мозга, проявляющееся в частности тромбоцитопенией (уменьшение количества тромбоцитов), может возникнуть при лечении линезолидом; полагают, что это единственный побочный эффект, который возникает значительно чаще при использовании линезолида, чем при применении гликопептидов или бета-лактамов.[34] Он редко возникает у больных, получающих препарат в течение 14 дней или меньше, но встречается гораздо чаще у пациентов, которые получают линезолид более длительным курсом или у которых есть почечная недостаточность.[9][72]
Длительное использование линезолида также ассоциировано с периферической невропатией и оптической невропатией, которые является наиболее распространёнными после нескольких месяцев лечения и могут быть необратимыми.[73][74][75][76] Хотя механизм повреждения всё ещё не совсем понятен, токсическое повреждение митохондрий предполагают в качестве причины;[77][78] линезолид является токсичным для митохондрий, вероятно, из-за сходства митохондриальной и бактериальной рибосом.[79]Лактатацидоз, потенциально опасное для жизни накопление молочной кислоты в организме, может также возникать в связи с митохондриальной токсичностью.[77] Из-за этих эффектов длительного лечения, производитель рекомендует еженедельно проводить клинический анализ крови во время терапии линезолидом для контроля за возможным подавлением функции костного мозга и рекомендует проводить лечение не более 28 дней.[1][9] Протокол более интенсивного мониторинга для раннего выявления токсичности у тяжелобольных пациентов, получающих линезолид, был разработан и предложен группой исследователей в Мельбурне, Австралия. Протокол включает проведение два раза в неделю анализов крови и функциональных проб печени; измерение уровня лактата в сыворотке крови для раннего обнаружения лактатацидоза; оценка всех лекарств принимаемых пациентом, отменяя назначение тех, которые могут взаимодействовать с линезолидом и периодические осмотры глаз и оценка неврологического статуса у пациентов, которые должны получать линезолид более четырёх недель.[80]
Побочные эффекты длительного применения линезолида были впервые выявлены в ходе постмаркетингового наблюдения. Подавление функции костного мозга не было выявлено в ходе III фазы исследований, в которых лечение не превышало 21 дней. Хотя у некоторых участников ранних исследований возникала тромбоцитопения, она оказалась обратимой и не возникала значительно чаще, чем в контрольной группе (где участники не принимали линезолид).[5] Были также постмаркетинговые сообщения о судорогах и, по состоянию на июль 2009 года, одиночные случаи паралича Белла (паралич лицевого нерва) и токсичном поражении почек.[69]
Химия
При физиологическом рН, линезолид существует в незаряженном состоянии. Он умеренно растворим в воде (приблизительно 3 мг/мл), с log Р 0,55.[26]
Фармакокинетика

Одним из преимуществ линезолид является его высокая биодоступность (около 100 %) при пероральном применении. Это означает, что пациенты, получающие линезолид внутривенно, могут начать принимать препарат перорально, как только их состояние позволяет, в то время как схожие антибиотики (например, ванкомицин и квинупристин/дальфопристин) могут назначаться только внутривенно.[81]При приёме линезолида с пищей возможно некоторое замедление его абсорбции, но площадь под кривой не изменяется.[26]
Линезолид обладает низкой способностью связывания с белками плазмы (примерно 31 %, но значения сильно варьируют) и кажущийся объём распределения в равновесном состоянии составляет около 40-50 литров.[2] Пик концентрации в сыворотке крови (С макс) достигается через 1-2 часа после введения препарата. Линезолид хорошо распределяется во всех тканях в организме, кроме костного матрикса и белой жировой ткани.[8] Примечательно, что концентрация линезолида в жидкости эпителия слизистой оболочки нижних дыхательных путей по крайней мере одинакова, а зачастую и выше, чем таковая в сыворотке крови (некоторые авторы сообщают, что концентрация в бронхиальной жидкости в четыре раза выше, чем в сыворотке крови), чем можно объяснить его эффективность при лечении пневмонии. Концентрация в спинномозговой жидкости варьирует; пик концентрации в СМЖ ниже, чем сыворотки крови из-за медленной диффузии через гемато-энцефалический барьер и корыта концентрации в СМЖ выше по той же причине.[26] Средний период полураспада составляет три часа у детей, четыре часа у подростков и пять часов у взрослых.[1]
Линезолид метаболизируется в печени путём окисления морфолинового кольца без участия системы цитохрома Р450. Этот метаболический путь приводит к образованию двух крупных неактивных метаболитов (что каждый приходится около 45 % и 10 % дозы выделяется в устойчивом состоянии), одного малого метаболита и нескольких следовых метаболитов, ни один из которых приходится более 1 % выделяется дозы.[82] Клиренс линезолида зависит от возраста и пола; он самый быстрый у детей (на долю которого приходится более короткий период полураспада) и, вероятно, на 20 % ниже у женщин, чем у мужчин.[1][82][83]
Применение в особых группах населения
Взрослым и детям старше 12 лет линезолид обычно назначается каждые 12 часов перорально или внутривенно.[5][81] Детям младшего возраста и младенцам препарат назначается каждые 8 часов.[84] Нет точной дозировки для лиц пожилого возраста, людей с лёгкой или умеренной печёночной недостаточностью или для пациентов с нарушениями функции почек.[2] Люди, нуждающихся в гемодиализе, должны получать линезолид после процедуры, так как диализ удаляет 30-40 % дозы из организма, нет точной дозировки для пациентов, которые находятся на непрерывной гемофильтрации[2], хотя и более частое введение может быть оправдано в некоторых случаях.[26] По данным одного исследования, вводить линезолид, возможно, требуется чаще у пациентов с ожогами, которые поражают более 20 % площади тела, когда увеличивается непочечный клиренс препарата.[85]
Линезолид в США имеет класс С для беременных, то есть не было никаких достаточных исследований его безопасности при использовании у беременных и хотя исследования на животных показали умеренную токсичность для плода, преимущество использования препарата может превышать риск.[1] Он также проникает в грудное молоко, хотя клиническое значение этого неизвестно.[28]
Механизм действия

Оксазолидиноны являются ингибиторами синтеза белка: они останавливают рост и размножение бактерий, нарушая трансляцию белков на рибосомах. Хотя механизм действия полностью не понятен,[86] линезолид, вероятно, действует на первом этапе синтеза белков — инициации — в отличие от большинства других ингибиторов синтеза белка, которые препятствуют элонгации.[81][87]
Препарат делает это путём предотвращения образования инициирующего комплекса, состоящего из 30S и 50S субъединиц рибосомы, тРНК и мРНК. Линезолид связывается с 23S частью 50S субъединицы (центр действия пептидилтрансферазы),[88] рядом с областью связывания хлорамфеникола, линкомицина и других антибиотиков. В связи с этим уникальным механизмом действия, перекрёстная резистентность между линезолидом и другими ингибиторами синтеза белка возникает очень редко или вовсе отсутствует.[5][26]
В 2008 году кристаллическая структура линезолида, связанная с 50S субъединицей рибосомы архея Haloarcula marismortui, была выделена группой учёных из Йельского университета и хранится в Protein Data Bank.[89] Другая группа учёных в 2008 году определила структура линезолида, связанного с 50S субъединицей Deinococcus radiodurans. Авторы предложили уточнённую модель механизма действия оксазолидинонов, установив, что линезолид занимает А область 50S рибосомной субъединицы, вызывая конформационные изменения, что предотвращает попадание тРНК и, в итоге, заставляя тРНК отделиться от рибосомы.[90]
Устойчивость
О приобретённой устойчивости к линезолиду сообщалось ещё в 1999 году, у двух пациентов с тяжёлой инфекцией Энтерококкус фэциум со множественной лекарственной устойчивостью.[25] Линезолид-устойчивый золотистый стафилококк был впервые обнаружен в 2001 году.[91]
В США устойчивость к линезолиду мониторируется и отслеживается с 2004 года в рамках программы под названием LEADER. Устойчивость остаётся стабильной и чрезвычайно низкой.[92] Похожая международная программа — Zyvox Annual Appraisal of Potency and Spectrum Study или ZAAPS — действует с 2002 года. В 2007 году общая устойчивость к линезолиду в 23 странах была меньше чем 0,2 % и не существовала среди стрептококков. Устойчивость была выявлена только в Бразилии, Китае, Ирландии и Италии, среди коагулазонегативных стафилококков (0,28 % проб устойчивости), энтерококков (0,11 %) и золотистых стрептококков (0,03 %).[93]
Механизм устойчивости
Собственная устойчивость большинства грамотрицательных бактерий к линезолиду связана с активностью истечения насосов, которые активно «выкачивают» линезолид из клетки быстрее, чем он накапливается.[8][94]
У грамположительных бактерий обычно развивается устойчивость к линезолиду в результате точечной мутации, известной как G2576T , при которой основание гуанина заменяется тимином в аллели 2576 генов, кодирующих 23S рибосомальную РНК.[95][96] Это наиболее распространённый механизм устойчивости стафилококков.[97] Другие механизмы были обнаружены у пневмококков (в том числе мутации в РНК метилтрансферазе, который метилирует G2445 из 23S рРНК, и мутации вызывают повышение экспрессии гена транспортёра ABC)[98] и у эпидермального стафилококка.[99][100]
Взаимодействия с другими лекарственными средствами
Линезолид является слабым ингибитором моноаминоксидазы (ИМАО) и не должен применяться одновременно с другими ИМАО, с продуктами, содержащими большое количество тирамина (такие как свинина, сыры, алкогольные напитки, копчёные и солёные продукты) и с серотонинергическими препаратами. Существуют постмаркетинговые сообщения о возникновении серотонинового синдрома, когда линезолид принимался одновременно или вскоре после отмены серотонинергических препаратов, особенно селективных ингибиторов обратного захвата серотонина, таких как пароксетин и сертралин.[9][101][102][103] Он может также усиливать гипертензивный эффект симпатомиметических препаратов, таких как псевдоэфедрин или фенилпропаноламин.[5][104] Линезолид также не должен сочетаться с петидином (меперидином) ни при каких обстоятельствах из-за риска серотонинового синдрома.
Линезолид не влияет на систему цитохрома P450 (CYP), которая отвечает за метаболизм многих лекарств и, следовательно, не имеет CYP связанных взаимодействий.[1]
Фармакоэкономика
Линезолид довольно дорогой препарат: курс лечения может стоить несколько тысяч долларов США, не учитывая другие расходы (например само пребывание в стационаре). Однако внутривенное введение линезолида может быть заменено на пероральный приём без ущерба для эффективности, пациенты могут быть выписаны из больницы относительно рано и продолжать лечение на дому, в то время как домашнее лечение инъекционными антибиотиками может быть нецелесообразным.[3] Сокращение продолжительности пребывания в стационаре снижает общую стоимость лечения, хотя линезолид может быть более дорогим, чем похожие антибиотики.
Были проведены исследования в ряде стран с различными моделями системы здравоохранения для оценки экономической эффективности линезолида по сравнению с гликопептидами, такими как ванкомицин или тейкопланин. В большинстве стран, линезолид был более рентабельным, чем сопоставимые антибиотики для лечения госпитальной пневмонии и инфекций кожи либо из-за более эффективного лечения и лучшей выживаемости либо за счёт снижения общих затрат на лечение.[3]