Малярия
Маляри́я (итал. mala aria — «плохой воздух»[2][3], ранее известная как «болотная лихорадка»[4]) — группа трансмиссивных инфекционных заболеваний, передаваемых человеку при укусах самками комаров рода Anopheles («малярийных комаров»), вызывается паразитическими протистами рода Plasmodium, преимущественно Plasmodium falciparum[5].
| Малярия | |
|---|---|
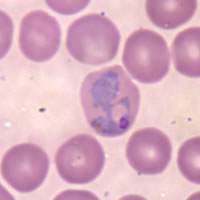 Эритроциты, заражённые P.vivax | |
| МКБ-10 | B50B51B52 B53 B54 |
| МКБ-10-КМ | B54 |
| МКБ-9 | 084 |
| МКБ-9-КМ | 084[1] и 084.6[1] |
| OMIM | 248310 |
| DiseasesDB | 7728 |
| MedlinePlus | 000621 |
| eMedicine | med/1385 emerg/305 ped/1357 |
| MeSH | D008288 |
Малярия сопровождается лихорадкой, ознобами, спленомегалией (увеличением размеров селезёнки), гепатомегалией (увеличением размеров печени), анемией. Характеризуется хроническим рецидивирующим течением.
На начало XXI века заболеваемость составляла 350—500 миллионов случаев в год, из них 1,3—3 миллиона заканчивались смертью[6]. Ожидалось, что смертность вырастет вдвое на протяжении следующих 20 лет,[7] однако данный прогноз оказался неверным. Согласно World Malaria Report 2021 от ВОЗ смертность от малярии не выросла вдвое с 2006 г в течение последующих 20 лет. С 896 000 в 2000 количество смертей снизилось до 562 000 в 2015 и до 558 000 в 2019[8]. Также по оценкам ВОЗ, в год происходит от 124 до 283 миллионов случаев заражения малярийными плазмодиями и от 367 до 755 тысяч смертей от заболевания. С 2000 года по 2013 год глобальные показатели смертности от малярии снизились на 47 %, в Африканском регионе ВОЗ — на 54 %.[9] 85—90 % случаев заражения приходится на районы Африки южнее Сахары[10], в подавляющем большинстве инфицируются дети в возрасте до 5 лет[11].
На 2019 год эффективность существующей вакцины против малярийного плазмодия низка (31—56 %). Тестируется новая предположительно высокоэффективная (90 % и более) вакцина[12][13].
Для некоторых групп населения риск заражения малярией, а также развитие более тяжелой формы болезни выше. Это младенцы, дети до пяти лет, а также беременные женщины. Кроме того, люди с ВИЧ/СПИДом, мигранты, у которых нет иммунитета, путешественники и мобильные группы населения находятся в зоне риска.[14]
История
Считается, что родиной малярии является Западная Африка (P. falciparum) и Центральная Африка (P. vivax). Молекулярно-генетические данные свидетельствуют, что предпаразитический предок плазмодия был свободноживущим простейшим, способным к фотосинтезу, который приспособился жить в кишечнике водных беспозвоночных. Также он мог жить в личинках первых кровососущих насекомых отряда Diptera, которые появились 150—200 миллионов лет назад, быстро приобретя возможность иметь двух хозяев. Древнейшие найденные окаменелости комаров с остатками малярийных паразитов имеют возраст 30 миллионов лет. С появлением человека развились малярийные паразиты, способные к смене хозяина между человеком и комарами рода Anopheles.
Около 2—3 млн лет назад, в популяции гоминин произошла мутация, блокирующая производство одной из разновидностей сиаловой кислоты — Neu5Gc, используемой малярийным паразитом для прикрепления к хозяйской клетке. Вероятно, вызываемое мутацией повышение устойчивости к малярии способствовало позднейшему её закреплению в популяции, несмотря на то, что одновременно её эффектом могло стать понижение фертильности. Предположительно, это привело к созданию барьера фертильности между носителями мутации и остальной популяцией и, в конечном счёте, к появлению предковой для современных людей линии гоминин[15][16][17].
Имеется археологическая находка датировкой 145 тыс. лет с диагностированной малярией — череп одного из видов Homo, обнаруженный в местечке Синга у города Сеннар в Судане[18].
По другим оценкам, люди болеют малярией в течение по крайней мере 50 тысяч лет[19]. 60—40 тысяч лет назад в организме гориллы, заражённой двумя линиями плазмодиев, произошёл обмен генетическим материалом между ними, в результате чего паразит, получивший определённый вариант гена rh5, приобрёл способность заражать человека[20]. Время до последнего общего предка (TMRCA) по всем гаплотипам устойчивого к малярии аллеля FY*O, который возник в Африке, — 42 тыс. лет назад (95 % доверительный интервал: 34—49 тыс. лет назад), TMRCA FY*A у неафриканцев — в 57 тыс. лет назад (95 % доверительный интервал: 48—65 тыс. лет назад). В современных популяциях к югу от Сахары аллель FY*O достигает частоты 86 %. Аллели FY*B и FY*A обычны для Европы и Азии, но имеются и в Африке[21][22].
Первые летописные свидетельства лихорадки, вызванной малярией, были обнаружены в Китае. Они датируются приблизительно 2700 годом до н. э., временем правления династии Ся[23].
Выяснение причины заболевания
В 1880 году французский военный врач Шарль Луи Альфонс Лаверан, работавший в Алжире, обнаружил в кровяных шариках больного малярией живой одноклеточный организм. Спустя год ученый опубликовал в медицинской печати статью «Паразитарный характер заболевания малярией: описание нового паразита, найденного в крови больных малярией». Это был первый случай, когда простейшие были идентифицированы как причина болезни[24]. За это и другие открытия он был награждён Нобелевской премией по физиологии и медицине 1907 года. Название рода паразита Plasmodium было предложено в 1895 году итальянскими учёными Этторе Маркиафава и Анджело Челли (итал. Angelo Celli)[25]. В 1894 году паразитолог Патрик Мэнсон впервые предположил, что малярия может передаваться человеку комарами. В 1896 году кубинский врач Карлос Финлей, который лечил больных жёлтой лихорадкой в Гаване, высказал ту же гипотезу. Англичанин сэр Рональд Росс, работавший в Индии, показал в 1898 году, что определённые разновидности комаров передают малярию птицам, и выделил паразитов из слюнных желез комара. Ему также удалось найти паразитов в кишечнике комаров, питавшихся кровью больных людей, но не удалось проследить передачу паразитов от комаров к человеку. Джованни Батиста Грасси в 1898 году удалось осуществить экспериментальное заражение человека малярией через укус комара (он ставил опыты на добровольцах, в том числе и на себе). Он доказал также, что только комары рода Anopheles являются переносчиками малярии в Италии, разработал и внедрил меры профилактики малярии. Однако в 1902 году Нобелевскую премию по медицине за описание жизненного цикла малярийного паразита получил только Рональд Росс. Данные, полученные Финлеем и Россом, в 1900 году были подтверждены медицинским советом, который возглавлял Уолтер Рид. Рекомендации этого совета были использованы Уильямом Кроуфордом Горгасом* для оздоровительных мероприятий, осуществлённых на строительстве Панамского канала.
Пути передачи
Для малярии существуют три следующих механизма передачи инфекции: трансмиссивный, через укусы комаров — комар кусает больного, затем кусает здорового человека и заражает его — наиболее распространенный путь; гемоконтактный, напрямую через кровь — при переливании крови, трансплантации органов или совместном использовании шприцев; трансплацентарный — от матери плоду во время беременности («врожденная» малярия), т. н. вертикальный путь.
Поиск лекарственных средств
Первым известным лекарством против малярии является растение полынь однолетняя, лат. Artemisia annua. Оно известно в Китае под названием кинхао и впервые упоминается в трактате «52 рецепта» (датируется династией Хань, две тысячи лет назад, обнаружен в мавандуйских погребениях). Другой рецепт, с применением этого растения именно для лечения малярии, содержится в работе китайского учёного Гэ Хуна IV века «Чжоуху Бэйцзи Фан» (Книга рецептов для оказания неотложной помощи, 340 г.)[26][27]
В 1596 году китайский врач Ли Шичжэнь применял экстракт полыни для лечения заболеваний, схожих по симптомам с малярией[5].
С открытием Нового Света появилось новое средство, кора хинного дерева, которая веками использовалась индейцами как жаропонижающее.Выдающийся испанский историк-натуралист Бернабе Кобо, иезуитский миссионер и писатель, сыграл значительную роль в истории хинина — иезуитской коры, как её поначалу называли — дав её первое описание; в 1632 году он же первым привез её в Европу.[28]
Его название пошло от первого известного европейца, которого им вылечили. Этим больным была графиня Чинчон, жена вице-короля Перу. Она получила заражение в долине Ланавара на побережье Тихого Океана. Излечилась она принятием коры хинного дерева, растертой в порошок. Саму кору вице-королю доставил Диего де Торрес Васкес, коррехидор долины Лоха (Loja) возле провинции Кито (Эквадор), которому её добыли подчинённые ему индейцы — потомки инков из Уритусинга[29], знавшие о свойствах коры, как лекарства (сама болезнь «перемежающаяся лихорадка» у индейцев кечуа называлась Chucchuni chucchuhuanmi chucchum hapihuan chucchuymanchayani; любое лекарство называлось — Hamppi, согласно словарю Диего Гонсалеса Ольгина, 1608). Сам граф широко раструбил об излечении своей жены, а графиня, вернувшись в Испанию, раздавала порошок из коры своим подругам и знакомым, и лекарство стало известным, как «порошок графини». Спустя несколько лет иезуиты, действовавшие в Перу, переправили кору в Рим, где её применяли в качестве лекарства от малярии, и благодаря им она стала известна по всей Италии.[30]
Так, Кардинал Хуан де Луго получил поручение от папы Иннокентия X собрать информацию о целебной коре quinquina (хинин — иезуитская кора). Затем её изучил папский придворный лекарь Габриель Фонсека, которого весьма заинтересовали свойства порошка. После этого кардинал де Луго развернул широкую кампанию за применение хинина.[31] В результате лекарство прозвали «иезуитским», или «кардинальским» порошком, люди в Риме какое-то время называли его «порошком де Луго».
В 1640-х годах начали вводить это средство в употребление в Европе, где оно вскоре было принято[32]. Однако активный ингредиент, хинин, был выделен из коры лишь в 1820 году французскими химиками Пьером Пеллетье и Жозефом Каванту.[33]
В 1709 году был опубликован трактат итальянского врача Ф. Торти (1658—1741) о применении коры хинного дерева при малярии[34].
В начале XX века, до открытия антибиотиков, практиковалось умышленное заражение малярией пациентов, больных сифилисом. Малярия обеспечивала повышенную температуру тела (до 40—41 °C), что значительно тормозило размножение возбудителя сифилиса бледной трепонемы и частично его убивало. В результате сифилис если и не проходил полностью, то во всяком случае снижал свою активность и переходил в латентную стадию. Контролируя течение лихорадки с помощью хинина, врачи таким образом пытались минимизировать негативные эффекты сифилиса. Несмотря на то, что некоторые пациенты умирали, это считалось предпочтительнее неизбежной смерти от сифилитической инфекции.[35]
Китайская учёная Ту Юю с 1965 по 1978 г. работала с архивами Китайской академии традиционной медицины, изучая старинные трактаты, и с 1969 года вела там поиск лекарства против малярии. К 1972 г. её группа изучила и проверила около 2000 старинных рецептов. Проверка показала эффективность отвара полыни Artemisia annua, из которой учёные выделили действующее вещество цинхаосу (от «цинхао» — полынь и «су» — основной элемент, в западной фармакопее вещество получило название артемизинин), представлящее собой сесквитерпеновый лактон (органическое вещество класса терпенов). Артемизинин убивает протисты на ранних стадиях их развития. Позже группа Юю Ту синтезировала более эффективные против плазмодия малярии производные артемизинина: дигидроартемизинин (восстановленный артемизинин), артеметер (жирорастворимый метиловый эфир артемизинина) и артесунат (водорастворимый гемисукцинат дигидроартемизинина). В 1979 г. завершились клинические испытания, подтвердившие эффективность и безопасность препаратов. Они были внедрены в клиническую практику, что ежегодно спасло около 2 миллионов жизней[5][36].
В 2006 году Всемирная организация здравоохранения рекомендовала отказаться от монопрепаратов артеминизина и использовать комбинированные лекарства, чтобы предотвратить появление устойчивых к артеминизину вариантов возбудителя малярии. В настоящий момент наиболее эффективной считается терапия комбинированными лекарствами, совмещающих артемизинин с другим противомалярийным веществом[5].
За разработку артемизинина группа Ту Юю получила премию Ласкера в 2011 и Нобелевскую премию в 2015 году[5].
Открытие покоящейся стадии паразита
Хотя стадии жизненного цикла паразита, проходящие в кровяном русле человека и в теле комара, были описаны ещё в конце XIX — начале XX века, только в 1980-е годы стало известно о существовании покоящейся стадии.[37][38] Открытие этой формы паразита окончательно объяснило, как люди, вылечившиеся от малярии, могли вновь заболевать спустя годы после исчезновения клеток плазмодия из кровяного русла.
Ареал

Малярийные комары живут почти во всех климатических зонах, за исключением субарктического, арктического поясов и пустынь.
Однако для того, чтобы существовал риск заражения малярией, требуются, помимо малярийных комаров, условия для их быстрого размножения и переноса малярийного плазмодия. Такие условия достигаются в тех районах, где не бывает низких температур, имеются болота и выпадает много осадков. Поэтому малярия шире всего распространена в экваториальной и субэкваториальной зонах, и относительно широко распространена во влажном субтропическом поясе.
В России малярийные комары обитают на всей европейской территории страны и в Западной Сибири, кроме полярных и приполярных широт. В Восточной Сибири зимы слишком суровые, и комары там не выживают.
В России и СССР
Ареал комаров-переносчиков, таких как Anopheles maculipennis, Anopheles messeae, Anopheles beklemishevi и Anopheles claviger[39], простирается в России весьма широко, захватывая умеренные широты почти до Полярного круга. По этой причине передача малярии возможна почти на всей территории Европейской части России, где имеются пригодные для размножения комаров заболоченные места, но ограничена теплым временем года.
В районе влажных субтропиков Кавказа (Сочи, Абхазия) малярия в начале XX века была большой проблемой до принятия С. Ю. Соколовым мер по осушению заболоченной местности, в том числе путём создания посадок эвкалипта и платана[40], нефтеванию водоёмов, разведению и выпуску в местные водоёмы и реки гамбузии и проведению других мероприятий, приведших в итоге к уничтожению как мест размножения так и самих малярийных комаров в курортной зоне[41][42].
В России и в СССР до начала 1950-х годов заболеваемость малярией была массовой, причем не только на Кавказе, в Закавказье и в Средней Азии, но и средней полосе европейской части (Поволжье и другие районы). Пик абсолютного числа заболевших пришелся на 1934—1935 годы, когда было зарегистрировано более 9 млн случаев малярии[43].
В дальнейшем малярия была практически ликвидирована в СССР к 1960 году, но единичные случаи (несколько десятков в год) случались и были связаны с перелётом комаров через пограничные с Афганистаном Амударью и Пяндж. Война в Афганистане привела к увеличению числа случаев малярии в СССР — в 1986—1990 годах было зафиксировано 1314 случаев (из них 136 завозных). Гражданская война в Таджикистане привела к эпидемии малярии в этой республике: в 1997 году было зафиксировано 29 794 случая[источник не указан 2133 дня]. В дальнейшем в Таджикистане ситуация нормализовалась и в 2011 году было отмечено лишь 78 случаев, а в 2013 году только 14 случаев (из них лишь 3 местных)[44].
Массовый завоз инфекции из южных стран СНГ привёл к случаям её распространения в некоторых регионах России, в основном в Москве, Московской области; а также крупных городах (трёхдневная малярия). Большинство случаев (до 500 ежегодно) возникает из-за приезда больных и не вылеченных мигрантов из закавказских и азиатских стран СНГ. По оценкам экспертов, в Москве и области с мая по сентябрь находилось порядка 2 млн мигрантов из Азербайджана и Таджикистана. В 2001 и 2003 гг. из-за эпидемии в Таджикистане большая часть случаев завоза инфекции была из этой страны[45].
Завоз заражённых комаров на транспортных средствах в РФ зафиксирован всего 1 раз: в 1999 г. около аэропорта «Шереметьево» (заразилось 4 человека)[45]. По информации Роспотребнадзора в 2018 г. заболеваемость малярией в РФ по сравнению с предыдущим годом возросла на 66,7 %. Всего было зарегистрировано 148 случаев. Столь значительное увеличение числа завозных случаев малярии в 2018 г. связано с проведением ХХI чемпионата мира по футболу в июне — июле 2018 г. в 11 городах Российской Федерации[46][47].
Трудности определения инфекции во время пандемии COVID-19
22 ноября 2020 года приблизительно в 20:50 в Вологде в возрасте 15 лет скончалась Дарья Мухина, ранее 11 ноября вместе с матерью вернувшаяся из Танзании. Тест на коронавирус показал отрицательный результат. Уже днём, после возвращения в Вологду, девушка почувствовала себя плохо, у неё поднялась температура до 42 градусов. Мать Дарьи вызывала скорую помощь четыре раза. Первая бригада скорой помощи выписала лечение противовирусными препаратами, вторая поставила предположительный диагноз: пневмония и гастроэнтерит. Школьница была доставлена в моногоспиталь на Советском проспекте, который был самым крупным и вторым открывшимся моногоспиталем в Вологодской области, после череповецкого, и специализировался на лечении больных с коронавирусной инфекцией[48]. 20 ноября врачи изменили диагноз на ротавирус, но отказались класть Дарью на лечение в инфекционную больницу без свежего теста на COVID-19. На следующий день её всё же взяли в больницу без теста. Анализ крови показал, что девушка умерла из-за тропической малярии, которую врачи изначально приняли за коронавирус. Новость вызвала большой общественный резонанс и была освещена в федеральных СМИ. Ситуация, сложившаяся во время пандемии, показала, что нагрузка ослабила систему здравоохранения, и врачи не всегда были способны поставить верный диагноз, когда пациенты заражались инфекцией, схожей по симптоматике с коронавирусной[49][50][51][52]. Позднее родители Дарьи обратились с заявлением в следственный комитет с просьбой проверить действия медиков[53].
Этиология и патогенез
Возбудители малярии — простейшие рода Plasmodium (плазмодии). Для человека патогенны четыре вида этого рода: P.vivax, P.ovale, P.malariae и P.falciparum[54]. В последние годы установлено, что малярию у человека в Юго-Восточной Азии вызывает также пятый вид — Plasmodium knowlesi[55][56][57]. Человек заражается ими в момент инокуляции (впрыскивания) самкой малярийного комара одной из стадий жизненного цикла возбудителя (так называемых спорозоитов) в кровь или лимфатическую систему, которое происходит при кровососании.
После кратковременного пребывания в крови спорозоиты малярийного плазмодия проникают в гепатоциты печени, давая тем самым начало доклинической печёночной (экзоэритроцитарной) стадии заболевания. В процессе бесполого размножения, называемого шизогонией, из одного бывшего спорозоита, который в клетке печени превращается в шизонта, в итоге образуется от 2000 до 40 000 печёночных мерозоитов. В большинстве случаев эти дочерние мерозоиты через 1—6 недель снова попадают в кровь. При инфекциях, вызываемых некоторыми североафриканскими штаммами P.vivax, первичный выход в кровь мерозоитов из печени происходит примерно через 10 месяцев от момента заражения, в сроки, совпадающие с кратковременным периодом массового выплода комаров в следующем году.
При инфекциях, вызываемых P.falciparum и P.malariae, печёночная стадия развития паразитов на этом и заканчивается. При инфекциях, вызванных другими видами малярийного плазмодия, «спящие» печёночные стадии (так называемые гипнозоиты) остаются и длительно персистируют в печени, они могут вызывать спустя месяцы и годы после заражения новые рецидивы заболевания и новые эпизоды выхода паразитов в кровь (паразитемии).
Эритроцитарная, или клиническая стадия малярии начинается с прикрепления попавших в кровь мерозоитов к специфическим рецепторам на поверхности мембраны эритроцитов. Эти рецепторы, служащие мишенями для заражения, по-видимому, различны для разных видов малярийных плазмодиев.
Плазмодии, попадая в жертву, стимулируют её выделять вещества, привлекающие комаров. К такому выводу пришли исследователи, когда провели серию экспериментов на мышах. Малярийные паразиты изменяли запах тела мышей, и особенно «привлекательным» этот запах становился в период полного созревания паразитов.[58]
Симптомы и диагностика
Симптомы малярии обычно следующие: лихорадка, ознобы, артралгия (боль в суставах), рвота, гемолитическая анемия, гемоглобинурия, судороги. Возможно также ощущение покалывания в коже, особенно в случае малярии, вызванной P. falciparum. Также могут наблюдаться спленомегалия (увеличенная селезёнка), нестерпимая головная боль, ишемия головного мозга. Малярийная инфекция смертельно опасна, особенно для детей и беременных женщин.
Диагноз устанавливается на основе выявления паразитов в мазках крови. Традиционно используют два типа мазков — тонкий и толстый (или так называемую «толстую каплю»). Тонкий мазок позволяет с большей надёжностью определить разновидность малярийного плазмодия, поскольку внешний вид паразита (форма его клеток) при данном типе исследования лучше сохраняется. Толстый мазок позволяет микроскописту просмотреть больший объём крови, поэтому этот метод чувствительнее, но внешний вид плазмодия при этом изменяется, что не позволяет легко различать разновидности плазмодия. Поставить диагноз на основе микроскопического исследования зачастую бывает затруднительно, так как незрелые трофозоиты разных видов малярийного плазмодия плохо различимы, и обычно необходимо несколько плазмодиев, находящихся на разных стадиях созревания, для надёжной дифференциальной диагностики.
В настоящее время используются также быстрые диагностические тесты (RDT, Rapid Diagnostic Tests) с использованием иммунохимических наборов (более дорогие, но дающие результат через 5—15 минут и не требующие использования микроскопа) и тесты с помощью ПЦР (наиболее дорогие, но наиболее надежные)[59]
Виды (формы) малярии
Симптоматика, течение и прогноз заболевания отчасти зависят от вида плазмодия, который является возбудителем данной формы болезни.
- Возбудитель тропической малярии — Plasmodium falciparum. Вызывает наиболее опасную форму, часто протекающую с осложнениями и имеющую высокую смертность. Эта же форма наиболее широко распространена (91 % всех случаев малярии в 2006 г.).
- Возбудитель четырехдневной малярии — Plasmodium malariae. Приступы происходят обычно через 72 часа.
- Возбудители трехдневной малярии и похожей на неё овале-малярии — соответственно, Plasmodium vivax и Plasmodium ovale. Приступы происходят через каждые 40—48 часов.
Эти формы малярии различаются также по длительности инкубационного периода, продолжительности разных стадий жизненного цикла плазмодиев, симптоматике и течению[60].
Таблица 1. Дифференциально-диагностические критерии малярии в зависимости от этиологии
| Клинические признаки | Виды малярии | |||
| Трехдневная Вивакс-малярия | Трехдневная овале-малярия | Четырехдневная | Тропическая | |
| Типовые (эндемичные) страны | Турция, Ирак, Сирия, Азербайджан | страны тропической Африки, Новой Гвинеи, Филиппины, Индокитай, Афганистан. | страны тропической Африки, юго-восточная Азия, ближний и Средний Восток | страны тропической Африки, Юго-Восточной Азии и Южной Америки (минимальная температура развития паразита в теле комара +18°С) |
| Инкубационный период | 10-14 дней (короткая инкубация) или 7-36 мес. (длительная инкубация) | 3-6 недель | 8-16 дней | |
| Продромальный период | есть | редко | редко | есть |
| Лихорадка: Выраженность | 40-41ºС | 38-39ºС | 39-40ºС | 38-39ºС |
| Лихорадка: Начало пароксизма | Утро | Вечер | Полдень | Вторая половина дня |
| Лихорадка: Длительность | 6-10 часов | 6-10 часов | 13 часов | 3-7 дней |
| Характер лихорадки | интермиттирующий | интермиттирующий | интермиттирующий | ремиттирующий, неправильный, постоянный |
| Лихорадка: Период апирексии | 1 день | 1 день | 2 дня | Нет |
| Интоксикация | выражена | слабо выраженная | слабо выраженная | выражена |
| Увеличение печени и селезенки | конец 1 недели | конец 1 недели | через 2 нед. | 2-3 день болезни |
| Анемия | Со 2-й недели | Со 2-й недели | Слабо выражена | Выражена при тяжелом течении |
| Гипогликемия | Слабо выражена | Не выражена | Не выражена | Часто. Выражена |
| Нервно-психические нарушения | Слабо или умеренно выражены во время пароксизма | Слабо выражены во время пароксизма | Слабо выражены во время пароксизма | Часто. Выражены вплоть до коматозного состояния |
| Продолжительность болезни без лечения | 1,5-3 года | 1,5-3 года | 3-50 лет | До 1 года |
| Осложнения | редко | редко | есть | есть |
| Возможность ранних рецидивов | есть | есть | есть | есть |
| Возможность поздних рецидивов | есть | есть | нет | нет |
| Выявление в периферической крови | все стадии паразитов | все стадии паразитов | все стадии паразитов | чаще — юные: трофозоит, кольца и гаметоциты полулунной формы. Зрелые трофозоиты и шизонты — неблагоприятный прогноз. Выявление только колец — ранний период, гаметоцитов — длительность болезни более 10 дней. |
Противомалярийный иммунитет
Иммунный ответ против малярийной инфекции развивается медленно. Он характеризуется малой эффективностью и практически не защищает от повторного инфицирования. Приобретённый иммунитет развивается после нескольких заболеваний малярией за несколько лет. Этот иммунитет специфичен к стадии заболевания, к виду и даже к конкретному штамму малярийного плазмодия. Но клинические проявления и симптомы уменьшаются с развитием специфического противомалярийного иммунитета.[источник не указан 956 дней]
Среди возможных объяснений такого слабого иммунного ответа называют нахождение малярийного плазмодия в клетках на протяжении большей части его жизненного цикла, общее угнетение иммунной системы, присутствие антигенов, которые не опознаются T-клетками, подавление пролиферации B-клеток, значительный полиморфизм малярийного плазмодия и быстрая смена потенциальных антигенов на его поверхности.[источник не указан 956 дней]
У людей существует мутация, вызывающая серповидноклеточную анемию, которая способствует выживанию при заражении малярийным плазмодием носителей этой мутации: в случае, когда один из двух аллелей продуцирует нормальный гемоглобин, а второй — аномальный гемоглобин S, такой носитель мутации c большей вероятностью выживает при заражении тропической малярией, и в то же время на равнине, при нормальном парциальном давлении кислорода, не страдает от анемии. Зато человек без серповидноклеточной анемии во время приступа малярии погибнет с большей вероятностью. Это способствовало сохранению такой мутации на территориях, эндемичных для тропической малярии. Однако в последние годы была обнаружена мутация малярийного плазмодия, которая позволяет ему проникать в серповидные эритроциты, в результате чего носитель серповидноклеточной анемии беззащитен при инвазии такого мутировавшего плазмодия[18].
- Cм. также: Антигенная система Даффи (англ. Duffy antigen system)
Лечение
Самым распространённым медикаментом для лечения малярии сегодня, как и раньше, является хинин. На некоторое время он был заменен хлорохином, но ныне снова приобрел популярность. Причиной этому стало появление в Азии и затем распространение по Африке и другим частям света Plasmodium falciparum с мутацией устойчивости к хлорохину.
Также существует несколько других веществ, которые используются для лечения и иногда для профилактики малярии. Многие из них могут использоваться для обеих целей. Их использование преимущественно зависит от устойчивости к ним паразитов в области, где используется тот или другой препарат.
В настоящее время наиболее эффективны комбинированные лекарственные средства с артемезинином[61]. Резолюция ВОЗ WHA60.18 (май 2007) настаивает на использовании этих препаратов, однако в России они до сих пор не зарегистрированы и не применяются.
| Препарат | Англ. название | Профилактика | Лечение | Примечания |
|---|---|---|---|---|
| Артеметер/люмефантрин | Artemether/lumefantrine | - | + | коммерческое название Коартем (в некоторых странах - Риамет) |
| Артезунат/амодиахин | Artesunate/amodiaquine | + | - | |
| Атовакуон/прогуанил | Atovaquone/proguanil | + | + | коммерческое название Маларон (в некоторых странах - Маланил) |
| Хинин | Quinine | - | + | |
| Хлорохин | Chloroquine | + | + | после появления резистентности использование ограничено коммерческое название Делагил |
| Котрифазид | Cotrifazid | + | + | |
| Доксициклин | Doxycycline | + | + | |
| Мефлохин | Mefloquine | + | + | коммерческое название Лариам |
| Прогуанил | Proguanil | - | + | коммерческое название Саварин |
| Примахин | Primaquine | + | - | |
| Сульфадоксин/пириметамин | Sulfadoxine/pyrimethamine | + | + | коммерческое название Фансидар |
Экстракты растения Artemisia annua (Полынь однолетняя), которые содержат вещество артемизинин и его синтетические аналоги, имеют высокую эффективность, но их производство дорого. В настоящее время (2006) изучаются клинические эффекты и возможность производства новых препаратов на основе артемизинина.[62] Другая работа команды французских и южноафриканских исследователей разработала группу новых препаратов, известных как G25 и TE3, успешно испытанных на приматах.[63][64]
Хотя противомалярийные лекарства присутствуют на рынке, болезнь представляет угрозу для людей, которые живут в эндемичных областях, где нет надлежащего доступа к эффективным препаратам. Согласно данным организации «Врачи без границ», средние затраты на лечение человека, заражённого малярией, в некоторых африканских странах составляют всего 0,25—2,40 $.[65]
Экспериментальные средства
С 2015 года ведутся испытания нового препарата от малярии — DSM265. Лекарство было разработано в Северо-западном медицинском центре Техасского университета совместно со специалистами Института фармакологии Университета Монаша, Вашингтонского университета и фонда Medicines for Malaria Venture (MMV). Препарат препятствует синтезу предшественников нуклеотидов, которые необходимы для дальнейшего синтеза ДНК и РНК, в организме малярийного плазмодия. В результате лекарство способно поражать возбудителя малярии и в крови, и в печени человека. Это первый противомалярийный препарат, рассчитанный на однократный приём. Также данное лекарственное средство можно будет принимать в профилактических целях.[66]
Другие препараты: ганаплацид.[источник не указан 204 дня]
По состоянию на 2017 г. для лечения малярии может использоваться новая (проходящая клинические испытания) вакцина PfSPZ в сочетании с хлорохином, препятствующим выходу плазмодиев из печени в кровь[67].
Профилактика
Методы, которые используются для предотвращения распространения болезни или для защиты в областях, эндемичных для малярии, включают профилактические лекарственные средства, уничтожение комаров, средства для предотвращения укусов комаров и вакцинацию[13][12].
Профилактические лекарственные средства
Ряд препаратов, используемых для лечения малярии, могут также применяться и для профилактики. Обычно эти лекарственные препараты принимают ежедневно или еженедельно в меньшей дозе, чем для лечения. Профилактические лекарственные средства обычно используются людьми, посещающими области с риском заражения малярией, и практически не используются местным населением из-за их высокой стоимости и побочных эффектов. Важно помнить, что лекарство для профилактики, на фоне приёма которого развилась малярия, не может применяться в последующем для её лечения. Препараты выбора для лечения малярии (комбинированные препараты с артемизинином) не используется в качестве профилактических.
С начала XVII века для профилактики используют хинин. Синтез в XX веке более эффективных альтернативных веществ (хинакрин (акрихин), хлорохин, примахин), сократило использование хинина. С появлением штамма Plasmodium falciparum, резистентного к хлорохину, хинин вернулся в качестве средства для лечения, но не для профилактики.
Современные лекарственные средства для профилактики включают мефлохин (Лариам), доксициклин и атовакуон-прогуанил гидрохлорид (бигумаль, Маларон). Выбор препарата обычно зависит от резистентности паразитов в области и от побочных эффектов. Профилактический эффект не начинается немедленно, поэтому следует начинать принимать профилактические препараты за 1—2 недели до прибытия в опасную зону и продолжать приём 1—4 недели после возвращения.
Выбор препарата для профилактики среди граждан, выезжающих в жаркие страны, рекомендуется только в зонах тропической малярии, зависит от того, куда планируется поездка. Мефлохин, хлорохин с прогуанилом и доксициклин не гарантируют защиту от малярии. Длительность приёма мефлохина и доксициклина ограничена (4 и 1 месяц соответственно)[45].
Уничтожение комаров
Усилия по борьбе с малярией путём уничтожения комаров достигли успеха в некоторых областях. Когда-то малярия была распространена в США и Южной Европе. После осушения болот и улучшения санитарных условий, вместе с контролем и лечением заражённых людей, эти области стали безопасными. Например, в 2002 году в США было зарегистрировано 1059 случаев малярии, в том числе 8 смертей. С другой стороны, не удается искоренить малярию во многих частях света, в первую очередь в развивающихся странах — проблема наиболее распространена в Африке.[источник не указан 943 дня]
В круглогодичном тёплом климате уничтожение комаров могло проводиться комбинированными биологическими методами. В частности, в Советском Союзе значительный успех в борьбе с яйцами и личинками малярийного комара в Сочи и Абхазии был достигнут при помощи разведения и выпуска в местные водоёмы и реки активного ларвифага гамбузии, а также путем осушения болот ирригационными работами и при помощи посадок эвкалипта и платана[42][40].
Эффективным химическим препаратом против комаров зарекомендовал себя ДДТ. Он был разработан во время Второй мировой войны как первый современный инсектицид. Сначала его использовали для борьбы против малярии, а затем он распространился и на сельское хозяйство. Со временем контроль за численностью сельскохозяйственных вредителей, вместо уничтожения комаров, стал преобладать в использовании ДДТ, особенно в развивающихся странах. На протяжении 1960-х количество свидетельств негативных последствий его неправильного применения увеличилось, что в конце концов привело к запрету ДДТ во многих странах в 1970-х. До этого времени его широкое использование уже привело к появлению стойких к воздействию ДДТ популяций комаров во многих областях. Но сейчас есть перспектива возможного возврата ДДТ. ВОЗ сегодня рекомендует использовать ДДТ против малярии в эндемичных областях. Наряду с этим, предлагается применять альтернативные инсектициды в областях, где комары устойчивы к ДДТ, чтобы контролировать эволюцию резистентности[68].
Тестируется антимоскитный лазер, убивающий комаров сфокусированным оптическим пучком[69].
Противокомариные сетки и репелленты

Противокомариные сетки помогают оградить людей от комаров и тем самым значительно уменьшить количество инфицирований и передачу малярии. Сетки — не идеальный барьер, поэтому они часто используются вместе с инсектицидом, который распыляется, чтобы убить комаров перед тем, как они найдут путь через сетку. Поэтому сетки, пропитанные инсектицидами, намного более эффективны.[7]
Для персональной защиты также эффективны закрытая одежда и репелленты. Репелленты подразделяются на две категории: натуральные и синтетические. Распространённые натуральные репелленты — эфирные масла некоторых растений.
Примеры синтетических репеллентов:
- Диэтилтолуамид
- IR3535 — этилбутилацетиламинопропионат
- Икаридин — гидроксиэтилизобутилпиперидинкарбоксилат
На острове Биоко за 15 лет (с 2003 до 2019 года) такими традиционными средствами, как противомоскитные сетки и распыление в помещениях инсектицидов, удалось снизить число больных малярией с 45 % лишь до 12,5 %. В других регионах центральной Африки результаты ещё хуже[13].
Трансгенные комары
Лесли Воссхолл (англ. Leslie Birgit Vosshall) — руководительница коллектива, в 2019 году опубликовавшего работу в журнале Cell, сотрудница Медицинского института Говарда Хьюза и руководительница лаборатории нейрогенетики и поведения при Университете Рокфеллера высказала идею о создании трансгенных кровососущих насекомых в целях борьбы с переносимыми ими заболеваниями: «У научного сообщества заканчиваются идеи о способах борьбы с насекомыми, которые распространяют болезни, и это совершенно новый способ думать в данном направлении. Инсектициды терпят неудачу из-за резистентности, у нас нет способа создать лучшие репелленты и пока нет вакцин против большинства болезней, распространяемых комарами, которые бы действовали достаточно хорошо, чтобы приносить существенную пользу». Учёные этой группы считают, что в борьбе с малярией необходимо акцентироваться на генной инженерии насекомых-переносчиков[70].
Учёные рассматривают несколько вариантов генетических модификаций генома комара. Один из потенциальных методов контроля численности комаров — метод выращивания бесплодных особей. Сейчас достигнут значительный прогресс в получении трансгенных или генетически изменённых комаров, не переносящих малярию. Уже в 2002 году две группы исследователей объявили о разработке первых линий подобных комаров[71][72].
В 2007 году в журнале PNAS была опубликована статья «Transgenic malaria-resistant mosquitoes have a fitness advantage when feeding on "Plasmodium"-infected blood». Группа специалистов с кафедры молекулярной биологии и иммунологии Института исследования малярии при Университете Джонса Хопкинса в Балтиморе (США) провела эксперименты, показывающие, как трансгенные малярийные комары могут конкурировать с обычными малярийными комарами. Ученые воспользовались ранее полученными сведениями, что приспособленность трансгенных малярийных комаров можно повысить: они оказывались более жизнеспособными, если их кормили кровью мышей, зараженных малярией. Ими были проведены эксперименты, в которых исследователи сравнивали, как меняется от поколения к поколению соотношение посаженных вместе трансгенных и диких комаров, которых кормили кровью зараженных малярией мышей. Через 9 поколений трансгенных комаров оказалось около 70 % от общего числа, и в дальнейшем это соотношение оставалось примерно постоянным. Если комаров в какой-то момент переводили на незараженную мышиную кровь, то трансгены всё равно удерживали первенство, хотя и не такое явное — на уровне около 60 %[73].
В 2019 году в журнале Science была опубликована статья «Transgenic "Metarhizium" rapidly kills mosquitoes in a malaria-endemic region of Burkina Faso». Сконструирован штамм энтомопатогенного грибка Metarhizium pingshaense, выделяющий инсектицид в гемолимфу малярийного комара. Проведенный в полуполевых условиях эксперимент показал, что применение трансгенного M. pingshaense сокращает популяцию комаров более чем на 90 %[74]
Вакцины
Ведутся разработки и клинические испытания различных вакцин от малярии[75].
В июле 2015 года Европейское агентство лекарственных средств выпустило позитивное мнение на вакцину «RTS,S» (Mosquirix), защищающую от Plasmodium falciparum, разработанную британской фармацевтической компанией GlaxoSmithKline[76]. Эта вакцина была проверена на более чем на 15 тысячах детей и показала эффективность около 30–40 % при четырёхкратном введении (протокол введения: 0, 1, 2 и 20 месяцев)[77]. На 2015 год публикация европейского агентства должна была способствать получению разрешений на применение этой вакцины в африканских странах, а Всемирная организация здравоохранения планировала изучить, насколько безопасно использование вакцины детьми — они наиболее подвержены малярии[76][78], применение вакцины в отдельных государствах ожидалось в 2017 году[79].
На 2019 год существовала единственная противомалярийная вакцина с эффективностью 31−56 % — RTS,S[12].
30 апреля 2019 года в Гане стартовала пилотная иммунизация населения вакциной RTS,S[80].
В 2021 году вакцина RTS,S (Mosquirix) допущена ВОЗ к широкому применению[81].
С 2003 года ведётся разработка вакцины PfSPZ (название происходит от англ. Plasmodium falciparum sporozoites) из ослабленных живых спорозоитов малярийного плазмодия. На первой стадии испытаний на малом количестве добровольцев эта вакцина показала 90 % эффективность, а в сочетании с хлорохином — 100 %, результаты КИ были опубликованы в 2017 году[67][82].На 2020 год были запланированы клинические испытания этой вакцины с участием нескольких тысяч жителей острова Биоко в Гвинейском заливе, 12,5 % населения которого болеют малярией[12][13].
В 2023 году Всемирная организация здравоохранения рекомендовала к использованию новую вакцину от малярии — R21[81][83], разработанную в Оксфордском университете. Это вторая вышедшая в оборот в мире вакцина, предназначенная для защиты от малярии, причём она недорогая в сравнении с первой (вдвое дешевле, чем RTS,S) и пригодна к массовому производству, что является её ключевым отличием от RTS,S[81].
Эксперты ВОЗ подчеркнули, что по эффективности обе вакцины близки. Однако выпуск ранее созданной вакцины RTS,S невелик, к октябрю 2023 года в мире имеется только 18 миллионов её доз, тогда как для выпуска новой вакцины в мире существует значительно больше производственных мощностей. В частности, Индийский институт сыворотки крови, крупнейший в мире производитель вакцин, готов выпускать ежегодно более 100 миллионов доз R21 и планирует увеличить производственные мощности до 200 миллионов доз в год[81].
Значение

Малярия всегда была и остается одной из опаснейших болезней человека. К известным личностям, которые возможно умерли от малярии, принадлежат: Александр Македонский, Аларих (король вестготов), Чингисхан, святой Августин, как минимум 5 римских пап, итальянский поэт Данте, император Священной Римской империи Карл V, Христофор Колумб, Оливер Кромвель, Микеланджело Меризи Караваджо, лорд Байрон и многие другие[84].
На 2019 год малярия является наиболее частой причиной смерти в тропиках[18].
- Сведения о малярии
- На 2006 год малярия была распространена более чем в 100 странах, где проживало более 40 % населения мира[85]. На 2011 год — 106 стран и больше половины мирового населения[86].
- По данным ВОЗ в 2017 г. выявлено 219 млн случаев малярии[87], в 2013 г. — 197 лабораторно подтверждённых случаев. В начале XXI века это число ежегодно возрастало на 16 %, число заболевших увеличивалось в 2000—2005 годах и снижалось между 2005—2010[88].
- Подавляющее большинство случаев регистрируется в Африке, другие очаги массового заболевания — Индия, Бразилия, Шри-Ланка, Вьетнам и Колумбия.
- Малярия находится на пятом месте по числу смертельных случаев за год среди инфекционных заболеваний. С точки зрения ВОЗ, малярия — самое приоритетное тропическое заболевание.
- Ежегодно до миллиона человек умирает от малярии (781 000 в 2009 и 655 000 в 2010).
В 2017 г. от малярии умерли 435 тыс. чел.[87] - По состоянию на 2008—2009 годы на одну смерть от малярии приходится 2200 $ на лечение и исследования в мире. Для сравнения, на одну смерть от ВИЧ/СПИД приходится 6800 $[источник не указан 1176 дней].
- Каждый год около 30 000 человек, посещающих опасные районы, заболевают малярией.
См. также
Примечания
Литература
- Тареев, Е. М. Клиника малярии. — 2-е изд. — М. : Медгиз, 1946. — 288 с.
- Мошковский, Ш. Д. Основные закономерности эпидемиологии малярии. — М. : Изд-во Акад. мед. наук СССР, 1950. — 324 с.
- Лысенко, А. Я. Малярия : паразитология, эпидемиология, профилактика и иммунитет : Центр. ин-т усоверш. врачей : лекция / А. Я. Лысенко, А. Е. Беляев. — М. : ЦОЛИУВ, 1981. — 42 с.
- Поль де Крюи. Гл. 10. Росс против Грасси. Малярия // Охотники за микробами = Paul de Cruif. Microbe Hunters. Houghton Mifflin Harcout Publishing Company, 1996. / Пер. с англ. О. Колесникова. — AST Publishers, 2017. — 480 с. — (Эксклюзивная классика). — ISBN 978-5-17-105544-8.
- Токаревич, К. Н. Трясучая хворь // По следам минувших эпидемий / К. Н. Токаревич, Т. И. Грекова. — Л. : Лениздат, 1986.
- Михель, Д. В. Болезнь и всемирная история : уч. пос. для студ. и аспир.. — Саратов : Научная книга, 2009. — 196 с. — ISBN 978-5-903357-18-5.
- Mordmüller, Benjamin. Sterile protection against human malaria by chemoattenuated PfSPZ vaccine / Benjamin Mordmüller, Güzin Surat, Heimo Lagler … [и др.] // Nature. — 2017. — Vol. 542 (15 февраля). — doi:10.1038/nature21060.
- Roestenberg, Meta. Protection against a Malaria Challenge by Sporozoite Inoculation / Meta Roestenberg, Matthew McCall, Joost Hopman … [и др.] // New Englang Journal of Medicine. — 2009. — Vol. 361 (30 июля). — P. 468−477. — doi:10.1056/NEJMoa0805832. — PMID 19641203.
Study to Investigate the Induction of an Protective Immune Response to Malaria. ClinicalTrials.gov (16 августа 2007). — NCT00442377. - Luke, Thomas C. Rationale and plans for developing a non-replicating, metabolically active, radiation-attenuated Plasmodium falciparum sporozoite vaccine / Thomas C. Luke, Stephen L. Hoffman // Journal of Experimental Biology. — 2003. — Vol. 206. — doi:10.1242/jeb.00644.
- Butler, Declan. Promising malaria vaccine to be tested in first large field trial : The vaccine can confer up to 100% protection and will be tested in 2,100 people on the west African island of Bioko. // Nature. — 2019. — 16 апреля. — doi:10.1038/d41586-019-01232-4.
- Рухадзе, Н. П. Материалы по изучению малярии в Абхазии / Нар. ком. здрав. С. С. Р. Абхазии. — Сухум : ВСНХ Абхазии, 1929. — 68 с. — 500 экз.
- Николаев, В. Ф. Использование и разведение эвкалиптов. — Сухум : АБГИЗ, 1933. — С. 6. — 20 с. — 1000 экз.
Ссылки
- Малярия у детей: симптомы, диагностика, лечение и профилактика. infectologia.ru. Дата обращения: 18 апреля 2019. Архивировано из оригинала 2 июня 2012 года.
- Екатерина Русакова. Вакцину от малярии со стопроцентной эффективностью испытают на выборке из 2100 человек. N+1 (17 апреля 2019). Дата обращения: 18 апреля 2019.
- Софья Долотовская. Вакцинация живыми плазмодиями обеспечила 100-процентную защиту от малярии. N+1 (16 февраля 2017).
- Даниил Кузнецов. Борцы с паразитами. В Стокгольме вручили Нобелевские премии по физиологии и медицине. N+1 (5 октября 2015).