Danh sách phân tử trong môi trường liên sao
Dưới đây là danh sách phân tử đã được phát hiện trong môi trường liên sao và vùng quanh sao, được nhóm lại theo số lượng nguyên tử thành phần. Công thức hoá học được liệt kê cho mỗi hợp chất được phát hiện, cùng với các dạng ion hoá đã được quan sát thấy.

Tổng quan
Các phân tử được liệt kê dưới đây được phát hiện thông qua phổ học thiên văn. Các đặc điểm phổ học của chúng phát sinh do các phân tử hấp thụ hoặc phát ra một photon ánh sáng khi chúng chuyển tiếp giữa hai mức năng lượng phân tử. Năng lượng (và do đó là bước sóng) của photon phù hợp với sự chênh lệch năng lượng giữa các mức liên quan. Chuyển đổi điện tử phân tử xảy ra khi một trong các electron của phân tử di chuyển giữa các orbital phân tử, tạo ra một vạch quang phổ trong các phần tử ngoại, ánh sáng hoặc hồng ngoại gần của phổ điện từ. Ngoài ra, quá trình chuyển đổi rung động cấp phân tử truyền năng lượng lượng tử tới (hoặc từ) các dao động của các liên kết phân tử, tạo ra các vết ấn trong vùng hồng ngoại trung hoặc xa. Các phân tử ở pha khí cũng có các mức chuyển đổi quay, gây ra sự chuyển tiếp ở bước sóng vi ba hoặc vô tuyến.[1]
Đôi khi một quá trình chuyển đổi có thể liên quan đến nhiều hơn một trong các loại mức năng lượng này, ví dụ như quang phổ rung động quay thay đổi cả mức năng lượng quay và rung động. Đôi khi cả ba xảy ra cùng nhau, như trong dải Phillips của C2 (dicarbon), khi quá trình chuyển đổi điện tử tạo ra một vạch trong vùng hồng ngoại gần. Nó sau đó được chia thành nhiều dải rung do sự thay đổi đồng thời về mức độ rung động, và từng dải lần lượt lại được chia thành các nhánh quay.[2]
Quang phổ của một phân tử cụ thể bị chi phối bởi các quy tắc chọn lọc của hóa học lượng tử và bởi tính đối xứng phân tử của nó. Một số phân tử có quang phổ đơn giản dễ xác định, trong khi những phân tử khác (thậm chí một số phân tử nhỏ) có quang phổ cực kỳ phức tạp với dòng trải rộng giữa nhiều vạch khác nhau, khiến chúng khó phát hiện hơn nhiều.[3] Tương tác giữa hạt nhân nguyên tử và electron đôi khi gây ra cấu trúc siêu mịn hơn nữa của các vạch quang phổ. Nếu phân tử tồn tại ở nhiều dạng isotopologues (các đồng vị phân tử), quang phổ sẽ phức tạp hơn do dịch chuyển đồng vị.
Việc phát hiện một phân tử giữa môi trường liên sao hoặc vùng quanh các sao đòi hỏi phải xác định một thiên thể có phù hợp nơi nó có khả năng hiện diện hay không, sau đó quan sát nó bằng kính viễn vọng được trang bị máy quang phổ hoạt động với bước sóng, độ phân giải phổ học và độ nhạy cần thiết. Phân tử đầu tiên được phát hiện trong môi trường liên sao là gốc methylidyne (CH•) vào năm 1937, thông qua quá trình chuyển đổi điện tử mạnh mẽ của nó ở 4300 ångström (trong quang học).[4] Những tiến bộ trong thiết bị thiên văn đã dẫn đến số lượng loại phân tử phát hiện mới ngày càng tăng. Từ những năm 1950 trở đi, thiên văn vô tuyến bắt đầu thống trị công cuộc phát hiện mới, với thiên văn học dưới milimet cũng trở nên quan trọng từ thập niên 1990.[3]
Việc kiểm kê các phân tử được phát hiện thường thiên về một số loại dễ phát hiện hơn: ví dụ: thiên văn học vô tuyến nhạy cảm nhất với các phân tử tuyến tính nhỏ có mức lưỡng cực phân tử cao.[3] Phân tử phổ biến nhất trong vũ trụ, H2 (hydro phân tử) hoàn toàn vô hình đối với kính viễn vọng vô tuyến vì nó không có lưỡng cực;[3] quá trình chuyển đổi điện tử của nó có mức năng lượng quá cao đối với kính viễn vọng quang học, vì vậy để phát hiện H2 thì cần quan sát cực tím bằng tên lửa nghiên cứu.[5] Các dải dao động thường không đặc trưng cho một phân tử riêng lẻ, nên chỉ có thể xác định loại chung. Ví dụ: các đường dao động của hydrocarbon thơm đa vòng (PAH) đã được xác định vào năm 1984,[6] cho thấy loại phân tử này rất phổ biến trong không gian,[7] nhưng phải đến năm 2021 mới xác định được các PAH cụ thể thông qua các dải quay của chúng.[8][9]
Một trong những nguồn phong phú nhất để phát hiện các phân tử liên sao là Sagittarius B2 (Sgr B2), một đám mây phân tử khổng lồ gần trung tâm Dải Ngân Hà. Khoảng một nửa số phân tử được liệt kê dưới đây lần đầu tiên được tìm thấy trong Sgr B2, và nhiều phân tử khác sau đó đã được phát hiện có ở đám mây này.[10] Một nguồn phân tử ngoại vi phong phú là CW Leonis (còn được gọi là IRC +10216), một ngôi sao carbon gần đó, là nơi có khoảng 50 loại phân tử đã được xác định.[11] Không có ranh giới rõ ràng giữa môi trường liên sao và môi trường xung quanh sao, vì vậy cả hai đều được gộp chung trong các bảng bên dưới.
Lĩnh vực hóa học thiên thể bao gồm việc hiểu cách các phân tử này hình thành và giải thích sự phong phú của chúng. Mật độ cực thấp của môi trường liên sao không có lợi cho sự hình thành các phân tử, làm cho các phản ứng pha khí thông thường giữa các vật chất trung hòa (nguyên tử hoặc phân tử) không hiệu quả. Nhiều khu vực cũng có nhiệt độ rất thấp (thường là 10 kelvin bên trong đám mây phân tử), làm giảm tốc độ phản ứng hoặc trường bức xạ cực tím cao, phá hủy các phân tử thông qua quá trình quang hóa.[12] Việc giải thích sự phong phú quan sát được của các phân tử liên sao đòi hỏi phải tính toán sự cân bằng giữa tốc độ hình thành và phá hủy bằng cách sử dụng hóa học ion pha khí (thường do các tia vũ trụ kiểm soát), hóa học bề mặt trên bụi vũ trụ, sự truyền xạ bao gồm sụp đổ liên sao và mạng lưới phản ứng phức tạp.[13] Việc sử dụng các vạch phân tử để xác định tính chất vật lý của các thiên thể được gọi là vật lý thiên văn phân tử.
Danh sách phân tử
Bảng dưới đây liệt kê các phân tử được phát hiện trong môi trường liên sao hoặc vật chất bao quanh sao, được nhóm lại theo số lượng nguyên tử thành phần. Các phân tử trung tính cùng các ion phân tử của chúng được liệt kê trong các cột riêng biệt; nếu không có mục nào trong cột phân tử, thì chỉ có dạng ion hóa được phát hiện. Tên gọi ở đây (tên của các phân tử) là những danh pháp được sử dụng trong tài liệu khoa học mô tả quá trình phát hiện; nếu không có tên thì ô đó để trống. Khối lượng được liệt kê với đơn vị khối lượng nguyên tử. Các phân tử deuteri, chứa ít nhất một nguyên tử deuteri (2H), có khối lượng hơi khác nhau và được liệt kê trong một bảng riêng. Tổng số loại phân tử của mỗi mục, bao gồm các trạng thái ion hóa riêng biệt, được ghi trong mỗi tiêu đề phần.
Hầu hết các phân tử được phát hiện cho đến nay là hữu cơ. Phân tử vô cơ duy nhất có năm nguyên tử trở lên được phát hiện là SiH4.[14] Các phân tử có số nguyên tử lớn hơn thế đều có ít nhất một nguyên tử carbon, không có liên kết N−N hoặc O−O.[14]
Hai nguyên tử (43)

| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| AlCl | Nhôm(I) chloride[16][17] | 62,5 | — |
| AlF | Nhôm(I) fluoride[16][18] | 46 | — |
| AlO | Nhôm(II) oxide[19] | 43 | — |
| — | Nguyên tử argon[20][21] | 37[note 1] | ArH+ |
| — | Cation carbon / Cation methyl | 12 | C+[22][23] |
| C2 | Dicarbon[24][25] | 24 | — |
| — | Fluoromethylidyni | 31 | CF+[26] |
| CH | Gốc methylidyn[27][28] | 13 | CH+[29] |
| CN | Gốc cyanide[16][28][30][31] | 26 | CN+,[32] CN−[33] |
| CO | Carbon monoxide[16][34][35] | 28 | CO+[36] |
| CP | Carbon monophosphide[31] | 43 | — |
| CS | Carbon monosulfide[16] | 44 | — |
| FeO | Sắt(II) oxide[37] | 82 | — |
| — | Cation heli hydride[38][39] | 5 | HeH+ |
| H2 | Hydro phân tử[5] | 2 | — |
| HCl | Hydro chloride[40] | 36,5 | HCl+[41] |
| HF | Hydro fluoride[42] | 20 | — |
| HO | Gốc hydroxyl[16] | 17 | OH+[43] |
| KCl | Kali chloride[16][17] | 75,5 | — |
| NH | Gốc imidogen[44][45] | 15 | — |
| N2 | Nitơ phân tử[46][47] | 28 | — |
| NO | Nitơ monoxide[48] | 30 | NO+[32] |
| NS | Lưu huỳnh mononitrit[16] | 46 | — |
| NaCl | Natri chloride[16][17] | 58,5 | — |
| — | Cation magnesi monohydride | 25,3 | MgH+[32] |
| O2 | Oxy phân tử[49] | 32 | — |
| PN | Phosphor nitride[50][51] | 45 | — |
| PO | Phosphor monoxide[52] | 47 | — |
| SH | Lưu huỳnh monohydride[53] | 33 | SH+[54] |
| SO | Lưu huỳnh monoxide[16] | 48 | SO+[29] |
| SiC | Carborundum[16][55] | 40 | — |
| SiN | –[56] | 42 | — |
| SiO | Silic monoxide[16] | 44 | — |
| SiS | Silic monosulfide[16] | 60 | — |
| TiO | Titani(II) oxide[57] | 63,9 | — |
Ba nguyên tử (44)

3 là một trong những ion phong phú nhất trong vũ trụ. Nó được phát hiện lần đầu tiên vào năm 1993.[58][59]
| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| AlNC | Nhôm isocyanide[16] | 53 | — |
| AlOH | Nhôm(I) hydroxide[60] | 44 | — |
| C3 | Tricarbon[61][62] | 36 | — |
| C2H | Gốc ethynyl[16][30] | 25 | — |
| CCN | Cyanomethylidyn[63] | 38 | — |
| C2O | Dicarbon monoxide[64] | 40 | — |
| C2S | Thioxoethenyliden[65] | 56 | — |
| C2P | —[66] | 55 | — |
| CO2 | Carbon dioxide[67] | 44 | — |
| CaNC | Calci isocyanide[68] | 92 | — |
| FeCN | Sắt cyanide[69] | 82 | — |
| — | Hydro proton hóa phân tử | 3 | H+ 3[58][59] |
| H2C | Gốc methylen[70] | 14 | — |
| — | Ion chloroni | 37,5 | H2Cl+[71] |
| H2O | Nước[72] | 18 | H2O+[73] |
| HO2 | Hydroperoxyl[74] | 33 | — |
| H2S | Hydro sulfide[16] | 34 | — |
| HCN | Hydro cyanide[16][30][75] | 27 | — |
| HNC | Hydro isocyanide[76][77] | 27 | — |
| HCO | Gốc formyl[78] | 29 | HCO+[29][78][79] |
| HCP | Phosphaethyn[80] | 44 | — |
| HCS | Thioformyl[81] | 45 | HCS+[29][79] |
| — | Diazenyli[29][79][82] | 29 | HN+ 2 |
| HNO | Nitroxyl[83] | 31 | — |
| — | Isoformyl | 29 | HOC+[30] |
| HSC | Isothioformyl[81] | 45 | — |
| KCN | Kali cyanide[16] | 65 | — |
| MgCN | Magnesi cyanide[16] | 50 | — |
| MgNC | Magnesi isocyanide[16] | 50 | — |
| NH2 | Gốc amin[84] | 16 | — |
| N2O | Dinitơ oxide[85] | 44 | — |
| NaCN | Natri cyanide[16] | 49 | — |
| NaOH | Natri hydroxide[86] | 40 | — |
| OCS | Carbonyl sulfide[87] | 60 | — |
| O3 | Ozon[88] | 48 | — |
| SO2 | Lưu huỳnh dioxide[16][89] | 64 | — |
| c-SiC2 | c-Silic dicarbide[16][55] | 52 | — |
| SiCSi | Disilic carbide[90] | 68 | — |
| SiCN | Silic carbonitride[91] | 54 | — |
| SiNC | —[92] | 54 | — |
| TiO2 | Titani(IV) oxide[57] | 79,9 | — |
Bốn nguyên tử (30)

| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| — | Cation methyl / Cation carbon | 15 | CH3+[22][23] |
| CH3 | Gốc methyl[94] | 15 | — |
| l-C3H | Propynylidyn[16][95] | 37 | l-C3H+[96] |
| c-C3H | Cyclopropynylidyn[97] | 37 | — |
| C3N | Cyanoethynyl[98] | 50 | C3N−[99] |
| C3O | Tricarbon monoxide[95] | 52 | — |
| C3S | Tricarbon sulfide[16][65] | 68 | — |
| — | Hydroni | 19 | H3O+[100] |
| C2H2 | Acetylen[101] | 26 | — |
| H2CN | Methylen amidogen[102] | 28 | H2CN+[29] |
| H2NC | Aminocarbyn[103] | 28 | — |
| H2CO | Formaldehyde[93] | 30 | — |
| H2CS | Thioformaldehyde[104] | 46 | — |
| HCCN | —[105] | 39 | — |
| HCCO | Ketenyl[106] | 41 | — |
| — | Hydro cyanide proton hóa | 28 | HCNH+[79] |
| — | Carbon dioxide proton hóa | 45 | HOCO+[107] |
| HCNO | Acid fulminic[108] | 43 | — |
| HOCN | Acid cyanic[109] | 43 | — |
| CNCN | Isocyanogen[110] | 52 | — |
| HOOH | Hydro peroxide[111] | 34 | — |
| HNCO | Acid isocyanic[89] | 43 | — |
| HNCN | Gốc cyanomidyl[112] | 41 | — |
| HNCS | Acid isothiocyanic[113] | 59 | — |
| NH3 | Amonia[16][114] | 17 | — |
| HSCN | Acid thiocyanic[115] | 59 | — |
| SiC3 | Silic tricarbide[16] | 64 | — |
| HMgNC | Hydromagnesi isocyanide[116] | 51,3 | — |
| HNO2 | Acid nitrơ[117] | 47 | — |
Năm nguyên tử (20)

| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| — | Ion amoni | 18 | NH+ 4[119][120] |
| CH4 | Methan[121] | 16 | — |
| CH3O | Gốc methoxy[122] | 31 | — |
| c-C3H2 | Cyclopropenyliden[30][123][124] | 38 | — |
| l-H2C3 | Propadienyliden[124] | 38 | — |
| H2CCN | Cyanomethyl[125] | 40 | — |
| H2C2O | Keten[89] | 42 | — |
| H2CNH | Methylenimin[126] | 29 | — |
| HNCNH | Carbodiimide[127] | 42 | — |
| — | Formaldehyde proton hóa | 31 | H2COH+[128] |
| C4H | Butadiynyl[16] | 49 | C4H−[129] |
| HC3N | Cyanoacetylen[16][30][79][130][131] | 51 | — |
| HCC-NC | Isocyanoacetylen[132] | 51 | — |
| HCOOH | Acid formic[130][133] | 46 | — |
| NH2CN | Cyanamide[134][135] | 42 | — |
| NH2OH | Hydroxylamin[136] | 37 | — |
| — | Cyanogen proton hóa | 53 | NCCNH+[137] |
| HC(O)CN | Cyanoformaldehyde[138] | 55 | — |
| C5 | Linear C5[139] | 60 | — |
| SiC4 | Cụm silic-carbide[55] | 92 | — |
| SiH4 | Silan[140] | 32 | — |
Sáu nguyên tử (16)
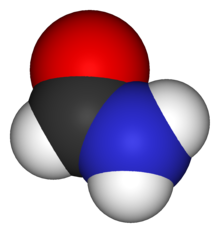
| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| c-H2C3O | Cyclopropenone[142] | 54 | — |
| E-HNCHCN | E-Cyanomethanimin[143] | 54 | — |
| C2H4 | Ethylen[144] | 28 | — |
| CH3CN | Acetonitril[89][145][146] | 40 | — |
| CH3NC | Methyl isocyanide[145] | 40 | — |
| CH3OH | Methanol[89][147] | 32 | — |
| CH3SH | Methanethiol[148] | 48 | — |
| l-H2C4 | Diacetylen[16][149] | 50 | — |
| — | Cyanoacetylen proton hóa | 52 | HC3NH+[79] |
| HCONH2 | Formamide[141] | 44 | — |
| C5H | Pentynylidyn[16][65] | 61 | — |
| C5N | Gốc cyanobutadiynyl[150] | 74 | — |
| HC2CHO | Propynal[151] | 54 | — |
| HC4N | —[16] | 63 | — |
| CH2CNH | Ketenimin[123] | 40 | — |
| C5S | —[152] | 92 | — |
Bảy nguyên tử (13)
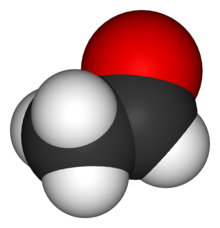
| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| c-C2H4O | Ethylen oxide[154] | 44 | — |
| CH3C2H | Methylacetylen[30] | 40 | — |
| H3CNH2 | Methylamin[155] | 31 | — |
| CH2CHCN | Acrylonitril[89][145] | 53 | — |
| HCCCHNH | Propargylimin[156] | 53 | — |
| H2CHCOH | Rượu vinyl[153] | 44 | — |
| C6H | Gốc hexatriynyl[16][65] | 73 | C6H−[124][157] |
| HC4CN | Cyanodiacetylen[89][131][145] | 75 | — |
| HC4NC | Isocyanodiacetylen[158] | 75 | — |
| HC5O | —[159] | 77 | — |
| CH3CHO | Acetaldehyde[16][154] | 44 | — |
| CH3NCO | Methyl isocyanat[160] | 57 | — |
| HOCH2CN | Glycolonitril[161] | 57 | — |
Tám nguyên tử (14)

| Phân tử | Tên gọi | Khối lượng |
|---|---|---|
| H3CC2CN | Methylcyanoacetylen[163] | 65 |
| HC3H2CN | Propargyl cyanide[164] | 65 |
| H2COHCHO | Glycolaldehyde[165][166] | 60 |
| (CHOH)2 | 1,2-ethenediol[167] | 60 |
| HCOOCH3 | Methyl format[89][130][166] | 60 |
| CH3COOH | Acid acetic[162] | 60 |
| H2C6 | Hexapentaenyliden[16][149] | 74 |
| CH2CHCHO | Propenal[123] | 56 |
| CH2CCHCN | Cyanoallen[123][163] | 65 |
| CH3CHNH | Ethanimin[168] | 43 |
| C2H3NH2 | Vinylamin[169] | 43 |
| C7H | Gốc heptatrienyl[170] | 85 |
| NH2CH2CN | Aminoacetonitril[171] | 56 |
| (NH2)2CO | Ure[172] | 60 |
Chín nguyên tử (10)
| Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|
| CH3C4H | Methyldiacetylen[173] | 64 | — |
| CH3OCH3 | Dimethyl ether[174] | 46 | — |
| CH3CH2CN | Propionitril[16][89][145] | 55 | — |
| CH3CONH2 | Acetamide[123][135][141] | 59 | — |
| CH3CH2OH | Ethanol[175] | 46 | — |
| C8H | Gốc octatetraynyl[176] | 97 | C8H−[177][178] |
| HC7N | Cyanohexatriyn hoặc Cyanotriacetylen[16][114][179][180] | 99 | — |
| CH3CHCH2 | Propylen (propen)[181] | 42 | — |
| CH3CH2SH | Ethyl mercaptan[182] | 62 | — |
| CH3NHCHO | N-methylformamide[135] |
Mười nguyên tử hoặc hơn (21)
| Số nguyên tử | Phân tử | Tên gọi | Khối lượng | Ion |
|---|---|---|---|---|
| 10 | (CH3)2CO | Aceton[89][183] | 58 | — |
| 10 | (CH2OH)2 | Ethylen glycol[184][185] | 62 | — |
| 10 | CH3CH2CHO | Propanal[123] | 58 | — |
| 10 | CH3OCH2OH | Methoxymethanol[186] | 62 | — |
| 10 | CH3C5N | Methylcyanodiacetylen[123] | 89 | — |
| 10 | CH3CHCH2O | Propylen oxide[187] | 58 | — |
| 11 | NH2CH2CH2OH | Ethanolamin[188] | 61 | — |
| 11 | HC8CN | Cyanotetraacetylen[16][179] | 123 | — |
| 11 | C2H5OCHO | Ethyl format[189] | 74 | — |
| 11 | CH3COOCH3 | Methyl acetat[190] | 74 | — |
| 11 | CH3C6H | Methyltriacetylen[123][173] | 88 | — |
| 12 | C6H6 | Benzen[149] | 78 | — |
| 12 | C3H7CN | n-Propyl cyanide[189] | 69 | — |
| 12 | (CH3)2CHCN | iso-Propyl cyanide[191][192] | 69 | — |
| 13 | C 6H 5CN | Benzonitril[193] | 104 | — |
| 13 | HC10CN | Cyanopentaacetylen[179] | 147 | — |
| 17 | C9H8 | Indene[9] | 116 | — |
| 19 | C10H7CN | 1-cyanonaphthalen[8] | 153 | — |
| 19 | C10H7CN | 2-cyanonaphthalen[8] | 153 | — |
| 27 | C11H12N2O2 | Tryptophan[194] | — | |
| 60 | C60 | Buckminsterfullerene (C60 fullerene)[195] | 720 | C+ 60[196][197][198] |
| 70 | C70 | C70 fullerene[195] | 840 | — |
Phân tử deuteri (22)
Các phân tử dưới đây chứa một hoặc nhiều nguyên tử deuteri, một đồng vị nặng của hydro.
| Số nguyên tử | Phân tử | Tên gọi |
|---|---|---|
| 2 | HD | Hydro deuteri[199][200] |
| 3 | H2D+, HD+ 2 | Trihydro cation[199][200] |
| 3 | HDO, D2O | Nước nặng[201][202] |
| 3 | DCN | Hydro cyanide[203] |
| 3 | DCO | Gốc formyl[203] |
| 3 | DNC | Hydro isocyanide[203] |
| 3 | N2D+ | —[203] |
| 3 | NHD, ND2 | Gốc amoni[204] |
| 4 | NH2D, NHD2, ND3 | Amonia[200][205][206] |
| 4 | HDCO, D2CO | Formaldehyde[200][207] |
| 4 | DNCO | Acid isocyanic[208] |
| 5 | NH3D+ | Ion amoni[209][210] |
| 6 | NH 2CDO; NHDCHO | Formamide[208] |
| 7 | CH2DCCH, CH3CCD | Methylacetylen[211][212] |
Chưa xác nhận (13)
Bằng chứng về sự tồn tại của các phân tử sau được báo cáo trong các tài liệu khoa học, nhưng các phát hiện được các nhà nghiên cứu mô tả là dự kiến hoặc đã bị các nhà nghiên cứu khác phản biện. Chúng vẫn chờ xác nhận độc lập.
| Số nguyên tử | Phân tử | Tên gọi |
|---|---|---|
| 2 | SiH | Silylidin[76] |
| 4 | PH3 | Phosphin[213] |
| 4 | MgCCH | Magnesi monoacetylide[152] |
| 4 | NCCP | Cyanophosphaethyn[152] |
| 5 | H2NCO+ | —[214] |
| 6 | SiH3CN | Silyl cyanide[152] |
| 10 | H2NCH2COOH | Glycin[215][216] |
| 10 | C2H5NH2 | Ethylamin[169] |
| 12 | CO(CH2OH)2 | Dihydroxyacetone[217][218] |
| 12 | C2H5OCH3 | Ethyl methyl ether[219] |
| 18 | C 10H+ 8 | Cation naphthalen[220] |
| 24 | C24 | Graphen[221] |
| 24 | C14H10 | Anthracen[222][223] |
| 26 | C16H10 | Pyren[222] |
Xem thêm
Ghi chú
Tham khảo
Liên kết ngoài
- Woon, David E. (1 tháng 2 năm 2007). “Interstellar and circumstellar molecules”. The Astrochemist. Truy cập ngày 13 tháng 2 năm 2007.
- Hudson, Reggie (1 tháng 2 năm 2007). “Interstellar Molecules”. NASA's Cosmic Ice Lab. Truy cập ngày 13 tháng 2 năm 2007.
- Wootten, Al (tháng 11 năm 2005). “The 129 reported interstellar and circumstellar molecules”. National Radio Astronomy Observatory. Truy cập ngày 13 tháng 2 năm 2007.
- F. J. Lovas, R. A. Dragoset (tháng 2 năm 2004). “NIST Recommended Rest Frequencies for Observed Interstellar Molecular Microwave Transitions, 2002 Revision”. National Institute of Standards and Technology. Truy cập ngày 13 tháng 2 năm 2007.
- “Molecules in Space”. Universität zu Köln. tháng 4 năm 2022. Truy cập ngày 22 tháng 8 năm 2023.
- Dworkin, Jason P. (1 tháng 2 năm 2007). “Interstellar Molecules”. NASA's Cosmic Ice Lab. Truy cập ngày 22 tháng 8 năm 2023.
- Williams, David A.; Cecchi-Pestellini, Cesare (8 tháng 2 năm 2023). Astrochemistry: Chemistry in Interstellar and Circumstellar Space (bằng tiếng Anh). Royal Society of Chemistry. ISBN 978-1-83916-939-7.



