Propan
(Đổi hướng từ Prôpan)
| Propan | |
|---|---|
Propan 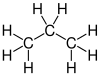  | |
| Tổng quan | |
| Công thức hóa học | CH3CH2CH3 C3H8 |
| SMILES | CCC |
| Phân tử gam | 44,096 g/mol |
| Bề ngoài | chất khí không màu |
| số CAS | [74-98-6] |
| Thuộc tính | |
| Tỷ trọng và pha | 1,83 kg/m³, khí, 0,5077 kg/l, lỏng |
| Độ hoà tan trong nước | 0,1 g/cm³ ở 37,8 °C |
| Nhiệt độ nóng chảy | - 187,6 °C (85,5 K) |
| Nhiệt độ sôi | - 42,09 °C (231,1 K) |
| Cấu trúc | |
| Momen lưỡng cực | 0.083 Debye |
| Nhóm đối xứng | C2v |
| Nguy hiểm | |
| MSDS | MSDS ngoài |
| Phân loại của EU | Rất dễ cháy (F+) |
| Nguy hiểm | R12 |
| An toàn | S2, S9, S16 |
| Điểm bốc cháy | -104 °C |
| Nhiệt độ tự bốc cháy | 432 °C |
| Nhiệt độ cháy tối đa | 2385 °C |
| Giới hạn nổ | 2,37–9,5% |
| Số RTECS | TX2275000 |
| Dữ liệu bổ sung | |
| Cấu trúc và tính chất | n, εr, v.v.. |
| Tính chất nhiệt động | Pha Rắn, lỏng, khí |
| Phổ | UV, IR, NMR, MS |
| Hóa chất liên quan | |
| alkan liên quan | ethan Butan |
| Ngoại trừ có thông báo khác, các dữ liệu được lấy ở 25°C, 100 kPa Thông tin về sự phủ nhận và tham chiếu | |
Propan (propane) là một hyđrocacbon nhóm alkan có công thức C3H8. Propan được sản xuất trong quá trình xử lý dầu mỏ hay khí tự nhiên. Propan được sử dụng như một nguồn năng lượng chính cho động cơ cũng như trong gia đình.
Propan thường được trộn với một lượng nhỏ của propylen, butan và butylen để sản xuất một loại nhiên liệu - khí dầu mỏ hoá lỏng (liquified petroleum gas, hay LPG, hoặc khí LP).
Tính chất
| NFPA 704 "Biểu đồ cháy" |
|---|
Được tách từ khí thiên nhiên, khí đồng hành hoặc từ các sản phẩm khí được hình thành trong cracking sản phẩm dầu mỏ. Dùng trong tổng hợp hữu cơ để điều chế Propan, nitromethan. Hỗn hợp P và butan được dùng làm khí đốt dùng trong đời sống (khí dầu mỏ hoá lỏng LPG).
Tham khảo
Liên kết ngoài
- Hiệp hội Khí dầu mỏ hoá lỏng thế giới (World LP Gas Association - WLPGA)
- Hướng dẫn về an toàn
- Hướng dẫn về an toàn của NIOSH
- Hình 3D của propan Lưu trữ 2006-10-05 tại Wayback Machine
- Hiệp hội Khí Propan Hoa Kỳ Lưu trữ 2016-09-01 tại Wayback Machine
- Hội đồng Giáo dục và Nghiên cứu Propan Hoa Kỳ
- Hiệp hội Khí Propan Canada Lưu trữ 2009-08-31 tại Wayback Machine
- Hiệp hội Khí hóa lỏng: Propan và Butan ở Anh Lưu trữ 2006-10-04 tại Wayback Machine
- Computational Chemistry Wiki Lưu trữ 2006-10-02 tại Wayback Machine
🔥 Top keywords: Đài Truyền hình Kỹ thuật số VTCTrang ChínhGiỗ Tổ Hùng VươngTrương Mỹ LanĐặc biệt:Tìm kiếmHùng VươngVương Đình HuệUEFA Champions LeagueKuwaitChiến dịch Điện Biên PhủFacebookĐài Truyền hình Việt NamTrần Cẩm TúĐội tuyển bóng đá quốc gia KuwaitGoogle DịchViệt NamCúp bóng đá U-23 châu ÁCúp bóng đá U-23 châu Á 2024Real Madrid CFBảng xếp hạng bóng đá nam FIFACleopatra VIITô LâmTim CookNguyễn Phú TrọngHồ Chí MinhHai Bà TrưngManchester City F.C.VnExpressChủ tịch nước Cộng hòa xã hội chủ nghĩa Việt NamNguyễn Ngọc ThắngĐền HùngCúp bóng đá trong nhà châu Á 2024Võ Văn ThưởngOne PieceLịch sử Việt NamCuộc đua xe đạp toàn quốc tranh Cúp truyền hình Thành phố Hồ Chí Minh 2024Phạm Minh ChínhTikTokĐinh Tiên Hoàng
