Quecksilber(II)-sulfat
Quecksilber(II)-sulfat ist eine chemische Verbindung des Schwermetalls Quecksilber mit der Summenformel HgSO4. Beim Erhitzen auf etwa 450 °C oder Einwirkung von energiereichem Licht zersetzt sich der Stoff und bildet elementares Quecksilber und Schwefeloxide. Wie die Verbindung selbst sind diese äußerst giftig und sollten deshalb nicht eingeatmet werden.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
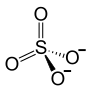 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Quecksilber(II)-sulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | HgSO4 | |||||||||||||||
| Kurzbeschreibung | weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 296,68 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest[1] | |||||||||||||||
| Dichte | 6,47 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | Zersetzung in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | 0,1 mg·m−3[1] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Quecksilber(II)-sulfat kann aus Quecksilber und konzentrierter Schwefelsäure hergestellt werden.[3]
Es kann nur aus schwefelsaurer Lösung auskristallisiert werden, da sich in wässriger Lösung schwerlösliches basisches Quecksilbersulfat HgSO4·2 HgO bildet. Dieses ist ein hellgelbes Pulver, das sich an Licht zersetzt und früher in der Pharmazie eingesetzt wurde.
In wenig Wasser bzw. in einer leicht mit Schwefelsäure angesäuerten Lösung bildet es ein Monohydrat aus HgSO4·H2O.[4]
Eigenschaften
Quecksilber(II)-sulfat ist ein weißes, nicht brennbares Pulver. Bei seiner Zersetzungstemperatur von 450 °C erglüht es und zerfällt in Quecksilber, Schwefeldioxid und zu einem geringen Teil auch in Schwefeltrioxid. Mit Alkalisulfaten bildet es Doppel- oder Komplexsalze aus, z. B.: K2SO4·3 HgSO4·2 H2O.[4] Es kristallisiert in einer orthorhombischen Struktur mit der Raumgruppe Pn21m (Raumgruppen-Nr. 31, Stellung 5) und den Gitterparametern a = 4,778 Å, b = 4,812 Å und c = 6,572 Å.[5]
Verwendung
Quecksilber(II)-sulfat wird als Katalysator bei der Produktion von Acetaldehyd aus Ethin und Wasser verwendet. Dabei entsteht Methylquecksilber als Nebenprodukt.
In wässriger Lösung wird es als Denigés-Reagenz (benannt nach dem französischen Biochemiker Georges Denigés) zum Nachweis von Isoolefinen und tertiären Alkoholen verwendet, die in Gegenwart von Säure leicht zu Isoolefinen dehydratisiert werden können. Ein positiver Nachweis wird durch einen festen gelben oder roten Niederschlag angezeigt.[6][7]
Sicherheitshinweise
Quecksilber(II)-sulfat ist sowohl für Tiere, als auch für den Menschen ein giftiger Stoff. Quecksilbersulfat ist ein Umweltgift und darf nicht auf normalem Wege entsorgt werden, da es besonders für Gewässer und deren Bewohner eine Bedrohung darstellt.




