Etila nitrato
kemia kombinaĵo
| Etila nitrato | ||
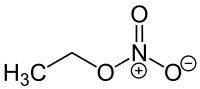 | ||
| Plata kemia strukturo de la Etila nitrato | ||
 | ||
| Tridimensia kemia strukturo de la Etila nitrato | ||
 | ||
| Antaŭnelongaj esploroj konfirmas ke etila nitrato ĉeestas en la profundaĵoj de la oceanoj. | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 625-58-1 | |
| ChemSpider kodo | 11756 | |
| PubChem-kodo | 12259 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora, eksplodema likvaĵo kun agrabla odoro, dolĉeca gusto kaj oksidigaj proprecoj[1] | |
| Molmaso | 91,066 g·mol−1 | |
| Denseco | 1,1084g cm−3 | |
| Fandpunkto | −102 °C | |
| Bolpunkto | 87,5 °C | |
| Refrakta indico | 1,3852 | |
| Ekflama temperaturo | −37 °C | |
| Solvebleco | Akvo:Nesolvebla | |
| Sekurecaj Indikoj | ||
| Riskoj | R2 | |
| Sekureco | S23 S24/25 [2] | |
| Pridanĝeraj indikoj | ||
| Danĝero | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Damaĝa substanco | |
| GHS Deklaroj pri damaĝoj | H200 | |
| GHS Deklaroj pri antaŭgardoj | P201, P202, P281, P372, P373, P380, P401, P501 | |
(25 °C kaj 100 kPa) | ||
Etila nitrato aŭ C2H5NO3 estas organika etila estero de nitrata acido, senkolora, eksplodema likvaĵo kun agrabla odoro, dolĉeca gusto kaj oksidigaj proprecoj[1], nesolvebla en akvo sed solvebla en la plejmulto el la organikaj solvantoj, kaj uzata en preparado de kemiaj sintezoj, drogoj, farboj kaj parfumoj.
Etila nitrato ekzistas en la atmosfero kaj ĝi ĉeestas sub la formo de densa nebulo ĉefe dum humidaj tagoj. Antaŭe konsiderita kiel poluaĵo, estigita ĉefe per brulado de fosiliaj fuelaĵoj, antaŭnelongaj analizoj de oceanakvaj specimenoj malkaŝas tion, ke en lokoj kie varmaj akvoj leviĝas el la profundo, la akvo saturiĝas per alkilaj nitratoj, eble formitaj per naturaj procezoj.
Sintezoj
Sintezo 1
- Preparado per traktado de nitrata acido sur etanolo en ĉeesto de sulfata acido:[3]
Sintezo 2
- Preparado per interagado de nitrila fluorido sur etanolo:
Sintezo 3
- Preparado per reakcio inter kloroetano kaj natria nitrato:
Sintezo 4
- Preparado per reakcio inter kloroetano kaj arĝenta nitrato:
Reakcioj
Reakcio 1
- Malkomponado de la etila nitrato:
Reakcio 2
- Eksploda oksidado de la etila nitrato:
Reakcio 3
- Preparado de nitrobenzeno:
Reakcio 4
- Preparado de 5-nitro-benzotiazolo:[4]
Reakcio 5
Literaturo
Referencoj
🔥 Top keywords: Vikipedio:ĈefpaĝoSpecialaĵo:SerĉiCarles Puigdemont i Casamajó14-a de junio17-a de septembro25-a de majo28-a de marto18-a de junioMarie-AntoinetteSpecialaĵo:Lastaj ŝanĝojEsperantoPortalo:KomunumoHelpo:EnhavoVikipedio:KontaktojVikipedioDigesta sistemoVikipedio:AktualaĵojMichael JacksonDua MondmilitoVikipedio:Bonvenon al VikipedioVikipedio:MalgarantioMichael BeckerDigestadoVikipedio:DiskutejoKrystyna Łuczak-SurówkaHelpo:Alŝuti dosieron11-a de junioWilhelm HegelerDobra (Satu Mare)Juan Antonio VillacañasȘugagVikipedio:AdministrantojBirdumoŜablono:RomSerĉilo-optimumigoKategorio:Vilaĝoj de RumanioFelix EpsteinUzanto:DominikPornhub