پروتون
پروتون (به انگلیسی: Proton) ذرهای زیراتمی، با نماد یا است که جرمش ۱۸۳۷ برابر جرم الکترون و اندکی کمتر از جرم نوترون است. به پروتون و نوترون که هر کدام جرمی حدود ۱ یکای جرم اتمی (amu) دارند نوکلئون (ذرات درون هستهٔ اتمها) هم میگویند. بار پروتون مثبت و اندازهاش با بار الکترون (1e+) یعنی ۱۹-۱۰× ۱٫۶۰۲۲ کولن برابر است.
 | |
| طبقهبندی | باریون |
|---|---|
| آمار | فرمیونی |
| نیروهای بنیادی | گرانش، الکترومغناطیس، ضعیف، قوی |
| نماد | p, p+ , N+ , 1 1H+ |
| پادذره | آنتی پروتون |
| نظریهپردازی | ویلیام پرووت (۱۸۱۵) |
| جرم | ۱٫۶۷۲۶۲۱۷۷۷(۷۴)×۱۰−۲۷ kg[۱] MeV/c۲ |
| ثابت واپاشی | > ۳٫۶×۱۰۲۹ years[۲] (stable) |
| بار الکتریکی | +۱ e |
| شعاع بار | ۰٫۸۴۱۴(۱۹) fm[۳] |
| گشتاور دوقطبی الکتریکی | < ۲٫۱×۱۰−۲۵ e⋅cm[۴] |
| قطبشپذیری | ۰٫۰۰۱۱۲(۴) fm۳ |
| گشتاور مغناطیسی | μB μN |
| قطبشپذیری | ۱٫۹(۵)×۱۰−۴ fm۳ |
| اسپین | 1/2 ħ |
| ایزواسپین | 1/2 |
| پاریته | +۱ |
| تقارنهای چگالی | I(JP) = 1/2(1/2+) |
هستهٔ هر اتم، یک یا چند پروتون دارد. شمار پروتونها در هسته، عدد اتمی نام دارد که با Z نمایش داده میشود و مشخصکنندهٔ عنصر شیمیاییست، به این معنی که شمار پروتونهای هستهٔ اتم هر عنصر شیمیایی یکتاست؛ هر عنصر شیمیایی، عدد اتمی منحصر به خود دارد.
پروتون که در یونانی به معنی «نخستین» است، نامیست که در ۱۹۲۰، ارنست رادرفورد به هستهٔ هیدروژن داد. او سالها پیشاز آن دریافتهبود که هستهٔ هیدروژن را (که میدانستند سبکترین هسته است) میتوان با برخورد اتمی از هستهٔ نیتروژن بیرون کشید. ازاینرو به نظر میرسید پروتون باید ذرهای بنیادی و واحد سازندهٔ هستهٔ نیتروژن و دیگر هستههای سنگینتر (از هیدروژن) باشد.
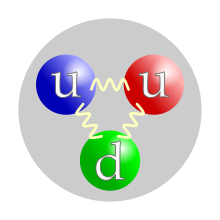
با آنکه در آغاز گمان میرفت، پروتون ذرهٔ بنیادیست، امروزه در طبقهبندیِ مدل استاندارد فیزیک ذرات، پروتون مانند نوکلئونِ دیگر، یعنی نوترون، یکی از هادرونها و ذرهای با سه کوارک ظرفیتیست؛ دو کوارک بالا که بار الکتریکی هر یک (۲e/۳)+ و یک کوارک پایین که بار الکتریکیش ۳/e - است.[۵][۶] سهم جرم سکون کوارکها در جرم پروتون تنها ۱٪ است.[۷] بقیهٔ جرم پروتون، برخاسته از انرژی بستگیِ کرومودینامیکِ کوانتومی شامل انرژی جنبشی کوارکها و انرژی میدانهای گلوئونهاییست که کوارکها را پیوند میدهد. ازآنجاکه پروتون ذرهٔ بنیادی نیست، اندازهٔ فیزیکی دارد که میتوان آن را سنجید؛ جذر میانگین مربعی شعاع پروتون، ۰٫۸۴ تا ۰٫۸۷ فِرمی است (هر فرمی برابر ۱۵-۱۰ متر است).[۸] ۲۰۱۹، دو بررسی مستقل با روشهای متفاوت، شعاع پروتون را اندازه گرفتند و به ۰٫۸۳۳ فرمی رسیدند. خطای این اندازهگیریها ۰٫۰۱۰± فرمی بود.
پروتون آزاد و الکترون، در دمای کم، پیوند میسازند، گرچه ویژگی پروتون تغییر نمیکند. پروتونی که بهسرعت از ماده میگذرد، در اثر برهمکنش با هستهها و الکترونهای ماده کُند میشود و سرانجام ابر الکترونی یکی از اتمها آن را جذب میکند؛ بنابراین، اتم، پروتوندار و در واقع ترکیب شیمیایی آن اتم با هیدروژن است. هر جا که الکترون آزاد در خلأ باشد، پروتونی که بهاندازه کافی کُند باشد میتواند یک الکترون جذب کند و اتم خنثای هیدروژن بسازد که از دیدگاه شیمیایی، رادیکال آزاد است. این اتمهای «هیدروژن آزاد» در انرژی کم تمایل به واکنش شیمیایی با دیگر اتمها دارند. واکنش اتمهای آزاد هیدروژن با هم، به ساخت مولکول هیدروژن () میانجامد که که فراوانترین بخش ابرهای مولکولی در فضای میانستارهای است.
شرح
پروتون، فرمیونی با اسپین ½- است که از سه کوارک ظرفیت ساختهشده[۹] و دارای توزیع بار الکتریکی مثبتی است که با آهنگ نمایی کم میشود. شعاع پروتون حدوداً ۰/۸ فمتومتر است.[۱۰] همین کوارکهای ظرفیت هستند که پروتون را به یک باریون، که خود یک زیرذرهٔ هادرونیست، تبدیل میکنند. دو کوارک بالا و یک کوارک پایین با نیرویی بسیار زیاد و با میانجیگری گلوئون به هم وصل هستند. امروزه بر این باورند که پروتون از سه کوارک ظرفیت (بالا بالا پایین)، گلوئونها و جفتهایی ظرفیتی از کوارک دریایی تشکیل شدهاند.
پروتون و نوترون ذرات درونهستهای هستند و میتوانند از راه نیروی هستهای به هم وصل شده، هسته اتم را شکل دهند. هسته فراوانترین ایزوتوپ هیدروژن، تنها یک پروتون دارد. دو ایزوتوپ دیگر هیدروژن، دوتریوم و تریتیوم، به ترتیب یک و دو نوترون دارند که به پروتون وصل شدهاند. هسته سایر اتمها از بیش از یک پروتون و تعداد متفاوتی نوترون شکل گرفتهاست.
تاریخچه
زمان زیادی گذشت، تا مفهوم ذرهٔ هیدروژنمانند به عنوان سازنده اتمهای دیگر توسعه یابد. نخست، ویلیام پروت، ۱۸۱۵، برپایه برداشت سادهانگارانهای از وزن اتمی، چنین فرض کرد که همه اتمها از اتمهای هیدروژن که او آنها را پروتیل مینامید، تشکیل شدهاند. پس از آن که وزن اتمی دقیقتر اندازه گرفتهشد، این فرضیه رد شد.[۱۱]
۱۸۸۶، اویگن گلدشتاین با کشف پرتوهای آنُدی نشان داد که آنها ذرههایی با بار مثبت هستند که از گازها تولید میشوند. البته، ازآنجاکه این ذرات منتشرشده از گازها، نسبت بار به جرم متفاوتی داشتند، شناسایی آنها به عنوان یک ذره، برخلاف الکترون با بار الکتریکی منفی، امکان نداشت. اما، ۱۸۹۸، ویلهلم وین، یون هیدروژن را به عنوان ذرهای که دارای بیشترین نسبت بار به جرم در گازهای یونیزه است، کشف کرد.
پس از کشف هسته اتم از سوی ارنست رادرفورد در ۱۹۱۱، آنتونیوس فاندِر بروک پیش نهاد که جای هر عنصر در جدول تناوبی، متناظر با بار هسته آن است. هنری موزلی در ۱۹۱۳ آن را با بهکارگیری طیف پرتو ایکس، تجربی تأیید کرد.[۱۲]
۱۹۱۷، رادرفورد ثابت کرد که هستههای دیگر نیز هسته هیدروژن دارند، که معمولاً این را کشف پروتون میدانند.[۱۳] رادرفورد آزمایشی کرد که در آن، ذرات آلفا به هوا (که بیشتر آن نیتروژن است) شلیک میشدند و آشکارگرها اثراتی از هیدروژن را به عنوان محصول واکنش نشان میدادند. رادرفورد پسازآنکه آزمایش را با نیتروژن خالص تکرار و مشاهده کرد که اثرات بیشتر شدهاند، نتیجه گرفت که این ذرههای هیدروژن تنها میتوانند از نیتروژن آمده باشند، و بنابراین هسته نیتروژن باید دارای هیدروژن باشد. در این آزمایش یک هسته هیدروژن جدا میشد و نیتروژن به اکسیژن-۱۷ تبدیل میشد. این رخداد، نخستین واکنش هستهای گزارش شدهاست.
14N + α → 17O + p
رادرفورد با تأثیر از فرضیه پروت میدانست که هیدروژن سادهترین و سبکترین عنصر، و واحد سازنده عناصر دیگر است. کشف این که هیدروژن در هسته همه اتمهای دیگر نیز هست، رادرفورد را بر آن داشت که نامی ویژه به عنوان یک ذره، به هسته هیدروژن بدهد. رادرفورد چنین پنداشت که هیدروژن به عنوان سبکترین عنصر، تنها دارای یکی از این ذرهها است و این واحد سازنده بنیادی جدید را پروتون نامید. این واژه از ریشه یونانی، به معنی نخستین، میآمد.[۱۴]
۲۴ اوت ۱۹۲۰، اولیور لاج در جلسه ای در مؤسسه بریتانیایی پیشرفتهای علمی از رادرفورد خواست تا برای جلوگیری از اشتباهگرفتن هیدروژن معمولی با هیدروژن مثبت، نامی برای آن انتخاب کند. رادرفورد که واژه پروتیل را که از سوی پروت استفاده شدهبود در ذهن داشت، پروتون (proton) و پرووتون (prouton) را پیش نهاد، که واژه نخستین پذیرفته شد.[۱۵][۱۶][۱۷]
تحقیقات نشان میدهد که رعدوبرق میتواند پروتونهایی با انرژی تا چند دهمیلیون الکترونولت تولید کند.[۱۸]

از پروتون معمولاً در پروتوندرمانی یا آزمایشهای فیزیک ذرهای استفاده میشود. یکی از بهترین نمونهها، شتابدهنده بزرگ هادرونی است.
پایداری
پروتون آزاد (که به هیچ نوترون یا الکترونی بسته نباشد) ذرهای پایدار است که تاکنون واپاشی آن به ذرات دیگر دیده نشدهاست. پروتون آزاد، بهطور طبیعی در دما و انرژی زیاد، که پروتون دارای انرژی کافی برای جداشدن از الکترون باشد، دیده میشود. در پلاسما، پروتون آزاد هست، زیرا دما چنان زیاد است که مانع میشود پروتون، الکترونی را جذب کند و پیوند بسازند. ۹۰٪ پرتوهای کیهانی که در فضای میانستارهای منتشر میشوند، پروتونهای پرسرعت (پرانرژی) است. در برخی واپاشیهای هستهای نادر نیز پروتون از هستهٔ اتم گسیل میشود. نوترون آزاد ناپایدار است و در اثر واپاشی، پروتون، الکترون و پادنوترینو آزاد میشوند.
تاکنون واپاشی خودبهخود پروتون آزاد دیده نشدهاست. برای همین، پروتون در مدل استاندارد، ذرهای پایدار است. اما در برخی نظریههای وحدت بزرگ فیزیک ذرات، واپاشی پروتون پیشبینی میشود و نیمهعمر آن از ۳۱+۱۰ تا ۳۶+۱۰ سال است و در برخی پژوهشهای تجربی برای عمر میانگین پروتون در اثر واپاشی فرضیِ آن به ذرات دیگر حد پایین تعیین شدهاست.[۱۹][۲۰][۲۱]
در آزمایشها با آشکارگر سوپر کامیوکانده در ژاپن، حد پایین ۳۳+۱۰ × ۶٫۶ سال برای نیمهعمر واپاشی پروتون به پادمیوئون و پیون خنثی و حد پایین ۳۳+۱۰× ۸٫۲ سال برای نیمهعمر واپاشی پروتون به پوزیترون و پیون خنثی به دست آمدهاست؛ یعنی در این آزمایشها واپاشی پروتون دیده نشده و اگر پروتون وابپاشد با توجه به مدت آزمایش و مقدار ماده، نیمهعمر پروتون از این دو حد بیشتر است.[۲۲] در آزمایشی دیگر در رصدخانهٔ نوترینو سادبری در کانادا، پژوهشگران تلاش کردند پرتوهای گاما حاصل از واپاشی هستههای بهجامانده از هر نوع واپاشیِ یکی از پروتونهای هستهٔ اتم اکسیژن ۱۶ را آشکار کنند. در این آزمایش حد پایین ۲۹+۱۰× ۲٫۱ سال برای نیمهعمر پروتون به دست آمد.[۲۳]
از سوی دیگر، جذب الکترون و تبدیل پروتون به نوترون (که واپاشی بتای وارون نام دارد)، فرایندی آشنا در فیزیک است. این فرایند برای پروتون آزاد خودبهخود روی نمیدهد و نیاز به انرژی دارد. این واکنش، برگشتپذیر است و نوترون در واپاشی بتا که یکی از شکلهای معمول واپاشی هستهایست، با میانگین نیمهعمر پانزده دقیقه به پروتون تبدیل میشود.
جستارهای وابسته
منابع
پیوند به بیرون
- Encyclopedia of Nuclear Physics and its Applications (به انگلیسی). 2012. Retrieved 2013-10-08.
- Proton definition


