Alcanfor
O alcanfor[5][6] ou cánfora[7] é un sólido incoloro ceroso cun forte aroma.[8] Quimicamente, clasifícase como un terpenoide e unha cetona cíclica. Encóntrase na madeira da árbore alcanforeiro (Cinnamomum camphora), unha grande árbore perenne de Asia oriental; e na árbore kapur (Dryobalanops sp.), unha árbore madeireira alta do sueste asiático. Tamén aparece nalgunhas outras árbores relacionadas da familia do loureiro, especialmente en Ocotea usambarensis. As follas do romeiro (Rosmarinus officinalis) conteñen do 0,05 ao 0,5% de alcanfor,[9] mentres que as de Heterotheca conteñen un 5%.[10] Unha fonte importante de alcanfor é Ocimum kilimandscharicum. O alcanfor tamén se produce sinteticamente a partir do aceite de trementina.
| Alcanfor[1][2] | |
|---|---|
 (+)- e (−)-alcanfor | |
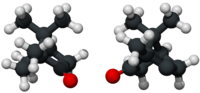 | |
1,7,7-Trimetilbiciclo[2.2.1]heptan-2-ona | |
Outros nomes 2-Bornanona; bornan-2-ona; 2-canfanona; formosa ; cánfora ; canfor | |
| Identificadores | |
| Número CAS | 76-22-2, 464-49-3 (R), 464-48-2 (S) |
| PubChem | 2537, 9543187 (R), 10050 (S) |
| ChemSpider | 2441, 7822160 (R), 9655 (S) |
| UNII | 5TJD82A1ET, N20HL7Q941 (R), 213N3S8275 (S) |
| Número CE | 200-945-0 |
| Número UN | 2717 |
| DrugBank | DB01744 |
| KEGG | D00098 |
| MeSH | Camphor |
| ChEBI | CHEBI:36773 |
| ChEMBL | CHEMBL504760 |
| Ligando IUPHAR | 2422 |
| Número RTECS | EX1225000 |
| Referencia Beilstein | 1907611 |
| Referencia Gmelin | 83275 |
| 3DMet | B04902 |
| Imaxes 3D Jmol | Image 1 Image 2 |
| |
| |
| Propiedades | |
| Fórmula molecular | C10H16O |
| Masa molar | 152,23 g mol−1 |
| Aspecto | cristais brancos, translúcidos |
| Olor | Fragrante e penetrante |
| Densidade | 0,992 g·cm−3 |
| Punto de fusión | 175 °C; 347 °F; 448 K |
| Punto de ebulición | 209 °C; 408 °F; 482 K |
| Solubilidade en auga | 1,2 g·dm−3 |
| Solubilidade en acetona | ~2500 g·dm−3 |
| Solubilidade en ácido acético | ~2000 g·dm−3 |
| Solubilidade en dietil éter | ~2000 g·dm−3 |
| Solubilidade en cloroformo | ~1000 g·dm−3 |
| Solubilidade en etanol | ~1000 g·dm−3 |
| log P | 2.089 |
| Presión de vapor | 4 mmHg (at 70 °C) |
| Rotación quiral [α]D | +44,1° |
| Perigosidade | |
| Pictogramas GHS |  |
| Palabra sinal GHS | Warning (Advertencia) |
| NFPA 704 | |
| Punto de inflamabilidade | 54 °C; 129 °F; 327 K |
| Límites de explosividade | 0.6–3.5%[3] |
| LD50 | 1310 mg/kg (rato, oral)[4] |
| Compostos relacionados | |
| relacionados | Fenchona, tuiona |
| Compostos relacionados | Canfeno, pineno, borneol, isoborneol, ácido canforsulfónico |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O composto é quiral, polo que existen dous posibles enantiómeros como se mostra nos diagramas estruturais. A estrutura da esquerda ié o isómero que máis aparece na natureza, o (+)-alcanfor ((1R,4R)-bornan-2-ona), mentres que a súa imaxe especular que se mostra á dereita é o (−)-camphor ((1S,4S)-bornan-2-ona). O alcanfor ten poucos usos, pero ten importancia histórica como composto que se purifica doadamente de fontes naturais.
Etimoloxía
A palabra deriva do árabe: كافور al kāfūr,[6] quizais a través do sánscrito: कर्पूर karpūra, aparentemente procedente do austronesio malaio: kapur, 'cal' (xiz).[11] Tamén se lle dá o nome cánfora[7] desde tempos medievais e usado en portugués.
Produción
Alcanfor natural
O alcanfor obtívose como produto forestal desde hai séculos, condensado do vapor desprendido da cachiños de madeira torrada de certas árbores, e posteriormente facendo pasar vapor de auga a través da madeira pulverizada e dos vapores.[12] A principios do século XIX a maioría das reservas de árbores de alcanfor estaban case esgotadas e as que quedaban estaban no Xapón e Taiwán, sendo a produción taiwanesa moito maior que a xaponesa. O alcanfor era un dos principais recursos extraídos polos poderes coloniais de Taiwán e tamén o máis lucrativo. Primeiro os chineses e despois os xaponeses estableceron monopolios sobre o alcanfor taiwanés. En 1868 unha forza naval británica chegou ao porto de Anping e o representante local británico demandou o final do monopolio chinés do alcanfor. Como o representante imperial rexeitou a demanda, os barcos británicos bombardearon a cidade e tomaron o porto. As "regulacións do alcanfor" negociadas entre ambos os bandos supuxeron o final do monopolio do alcanfor.[13]
Alcanfor sintético
O alcanfor prodúcese a partir do alfa-pineno, que é abundante nos aceites de árbores coníferas e pode destilarse a partir da trementina producida como subproduto da produción de polpa de papel. Usando ácido acético como solvente e coa catálise dun ácido forte, o alfa-pineno convértese en acetato de isobornilo. A hidrólise deste éster dá isoborneol, que pode ser oxidado para render alcanfor racémico.
Reaccións
As reaccións do alcanfor foron examinadas extensamente. Algunhas transformacións representativas son:
- sulfonación:[14]
O alcanfor tamén pode ser reducido a isoborneol usando borohidruro de sodio.
Bioquímica
Biosíntese
Na súa biosíntese o alcanfor prodúcese a partir de xeranil pirofosfato, por ciclación de linaloíl pirofosfato a bornil pirofosfato, seguida da hidrólise de borneol e a oxidación a alcanfor.
Usos
O alcanfor foi usado polo seu recendo, como fluído para embalsamar, como medicamento tópico, como composto químico para a fabricación doutros compostos e en cerimonias relixiosas.
Primeiros plásticos
Os primeiros plásticos significativos fabricados foron plásticos de nitrocelulosa (piroxilian) baixos en nitróxeno (ou "solubles"). Nas primeiras décadas da industria do plástico, o alcanfor utilizábase en enormes cantidades[16]:130 como o plastificador que xeraba celuloide a partir da nitrocelulosa, en lacas de nitrocelulosa e outros plásticos e lacas.
Medicina tradicional

O alcanfor foi utilizado na medicina tradicional popular durante séculos, probablemente na maior parte dos casos como deconxestivo.[17] O alcanfor foi utilizado na antiga Sumatra para tratar torceduras, inchamentos e inflamacións.[18] Tamén se usou durante séculos na medicina tradicional chinesa para varios propósitos.[17] En Europa, o alcanfor foi utilizado durante e despois da era da peste negra como fumigante.[19]
Veterinaria
Ten un uso limitado en veterinaria por inxección intramuscular para tratar as dificultades para respirar en cabalos.[20]
Medicamento tópico
O alcanfor aplícase de forma tópica como unha crema para a pel ou ungüento para aliviar o proído das picadas de insectos, irritacións menores da pel ou dores articulares.[21] Absórbese na epiderme,[21] onde estimula as terminacións nerviosas sensibles á calor e o frío, producindo unha sensación de calor cando se aplica vigorosamente, ou de frío cando se aplica suavemente, o que indica as súas propiedades como contrairritante.[17] A acción sobre as terminacións nerviosas tamén induce unha lixeira analxesia local.[22]
Aerosol respiratorio
O alcanfor tamén se usa en forma de aerosol, normalmente por inhalación de vapores, ás veces en forma de barras inhaladoras nasais para inhibir a tose e aliviar a conxestión das vías respiratorias superiores debido a catarreiras comúns.[23] Porén, a eficiencia clínica destes remedios está posta en dúbida.[24]
Analéptico
No século XX o alcanfor foi utilizado como analéptico por inxección,[25] e para inducir convulsións en esquizofrénicos nun intento de tratar a psicose.[26]
Antirreflectante
O alcanfor utilízano os tiradores para escurecer a parte anterior e posterior das miras dos rifles para evitar que se vexan reflexos.[27]
Repelente de pragas e conservante
O alcanfor crese que é tóxico para os insectos e ás veces é utilizado como repelente.[28] O alcanfor utilízase como alternativa ás bólas de naftalina. Os cristais de alcanfor úsanse ás veces para protexer as coleccións de insectos dos danos causados por outros insectos. Ponse en traxes usados en ocasións especiais, esquinas de lacenas como repelente de cascudas. O fume dos cristais de alcanfor ou das barras de incenso de alcanfor poden utilizarse como repelente de mosquitos non daniño para o medio ambiente.[29]
Estudos recentes indicaron que o aceite esencial de alcanfor pode utilizarse como fumigante efectivo contra as formigas de fogo, xa que afecta ao comportamento de atacar, morder, gabear e alimentarse das obreiras.[30]
Tamén se usa como substancia antimicrobiana. No embalsamamento o aciete de alcanfor era un dos ingredientes usados polos antigos exipcios para a momificación.[31]
Antioxidante
O alcanfor sólido libera vapores que forman un recubrimento que prevén a oxidación e, por tanto, déixase na caixa das ferramentas para impedir que enferruxen.[32]
Perfume
No antigo mundo árbe o alcanfor era un ingrediente común dos perfumes.[33] Os chineses denominaban o mellor alcanfor "perfume do cerebro de dragón" debido ao seu "aroma portentoso e penetrante" e os "séculos de incerteza sobre a súa proveniencia e modo de orixe".[34]
Usos culinarios
Unha das primeiras recietas coñecidas para os xeados é chinesa e data da dinastía Tang; inclúe o alcanfor como ingrediente.[35] Foi utilizado para aromatizar pan levedado no antigo Exipto.[36] Na Europa antiga e medieval o alcanfor usábase como ingrediente de doces. Usábase nunha ampla variedade de de pratos e doces nos libros de cociña árabes medievais, como o al-Kitab al-Ṭabikh compilado por ibn Sayyār al-Warrāq no século X.[37] Tamén se usaba en pratos e doces no Ni'matnama, segundo un libro escrito a finais do século XV polos sultáns de Mandu na India.[38] É o principal constituínte da especia chamada "alcanfor comestible" (ou kapur), que se usa en sobremesas tradicionais do sur da India como o Payasam e o Chakkarai Pongal.[39]
Ritos relixiosos
Utilízase frcuentemente en cerimonias relixiosas hindús. O ritual aarti realízase despois de situalo nunha plataforma e prenderlle lume xeralmente como último paso do puja.[40] O alcanfor menciónase no Corán como a fragrancia do viño que se lles dá aos crentes no ceo.[41]
Toxicidade
Aplicado á pel o alcanfor pode causar reaccións alérxicas nalgunhas persoas; cando a crema ou ungüento de alcanfor se inxire pola boca é velenosa.[21] Con altas doses inxeridas, o alcanfor produce síntomas de irritabilidade, desorientación, letargo, espasmos musculares, vómitos, cambras abdminais e convulsións.[42] As doses letais por inxestión en adultos están entre 50–500 mg/kg (oralmente). Xeralmente, a inxestión de dous gramos causa unha grave toxicidade e catro gramos son potencialmente mortais.[43]
Os vapores de alcanfor no aire poden ser tóxicos se os respiran os humanos. O límite permisible no aire ambiental é de 2 mg/m3 nun tempo de exposición de non máis de 8 horas. Unha concentración de 200 mg/m3 considérase moi perigosa.[44]
Notas
Véxase tamén
Outros artigos
- 1,4-Diclorobenceno
- Citral
- Eucaliptol
- Lavanda
Ligazóns externas
- INCHEM en IPCS (International Programme on Chemical Safety)
- NIOSH Pocket Guide to Chemical Hazards – Camphor en Centers for Disease Control and Prevention





