Ціан
Ціан (діціан, ціаноген) — хімічна сполука вуглецю з азотом із формулою (CN)2, дінітрил щавлевої кислоти. Найпростіший стабільний нітрид вуглецю[en], безбарвний і високотоксичний газ із різким запахом.
Молекула є псевдогалогеном. Молекули ціану складаються з двох груп CN — аналогів двоатомних молекул галогенів, як-от Cl2, але набагато менш окислювальних. Дві ціаногрупи з'єднуються атомами вуглецю: N≡C‒C≡N, хоча виявлено й інші ізомери[1]. Назва використовується також для радикалу ‒C≡N[2], а отже для таких сполук, як-от бромціан[en] (NCBr).
Ціан є ангідридом оксамиду[en]:
- H2NC(O)C(O)NH2 → NCCN + 2 H2O
хоча оксамид виготовляється з ціану шляхом гідролізу:
- NCCN + 2 H2O → H2NC(O)C(O)NH2
Отримання
Ціан зазвичай отримують із ціанідних сполук. Один із лабораторних методів передбачає термічне розкладання ціаніду ртуті(II)[en]:
- 2 Hg(CN)2 → (CN)2 + Hg2(CN)2
Крім того, можна поєднати розчини солей міді (II), як-от сульфат міді(II), з ціанідами. Утворюється нестійкий ціанід міді(ІІ), який швидко розкладається на ціанід міді(І) і ціан[3].
- 2 CuSO4 + 4 KCN → (CN)2 + 2 CuCN + 2 K2SO4
У промисловості ціан отримують окисленням ціаніду водню (синильної кислоти), зазвичай із використанням хлору з активованим каталізатором — діоксидом кремнію або діоксидом азоту над сіллю міді. Ціан також утворюється, коли азот і ацетилен реагують під дією електричних іскор або розряду[4].
Ізомери
Формула ціану — NCCN. Існують менш стабільні ізомери з іншим порядком розташування атомів:
- Ізоціаноген (ціаноізоціаноген) — NCNC
- Діізоціаноген — CNNC
- Діазодікарбон — CCNN.
Параціан
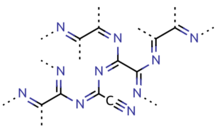
Параціан є полімером ціану. Його можна отримати нагріванням ціаніду ртуті. Крім того, його можна отримати нагріванням ціаніду срібла[en], ціанату срібла[en], ціаніду йоду[en] або йодиду ціанурової кислоти[5]. Параціан також можна отримати шляхом полімеризації ціану при температурі від 300 до 500 °C за наявності слідів домішок.
Параціан можна перетворити на ціан шляхом нагрівання до 800 °C. Згідно з експериментальними даними, структура цього полімерного матеріалу вважається досить нерегулярною, причому більшість атомів вуглецю мають тип sp2 і локалізовані домени π-сполучення[6].
Історія
Ціан вперше був синтезований у 1815 році Жозефом Луї Гей-Люссаком, який визначив його емпіричну формулу та дав йому назву. Гей-Люссак склав слово cyanogène із грецьких слів κυανός (синій) і γεννάω (створюю), тому що ціанід вперше виділив шведський хімік Карл Вільгельм Шеєле з пігменту «берлінська лазур»[7].
У 1824 році німецький хімік Фрідріх Велер одержав із диціану і води щавлеву кислоту.
До 1850-х років фотографи використовували ціанове мило для видалення з рік плям срібла[8]. Ціан набув важливості з розвитком промисловості добрив наприкінці XIX століття і залишається важливим проміжним продуктом у виробництві багатьох добрив. Використовується також як стабілізатор у виробництві нітроцелюлози.
Ціан часто зустрічають у кометах[9]. У 1910 році спектроскопічний аналіз комети Галлея виявив ціан у хвості комети, що призвело до загальних побоювань, що Землю буде отруєно, коли вона пройде через хвіст комети. Люди в Нью-Йорку носили протигази, а торговці продавали шарлатанські «таблетки від комети», які нібито нейтралізували отруєння[9]. Коли Земля проходила крізь хвіст комети Галлея, через його надзвичайно малу густину не спостерігалося жодних ефектів[10][11].
Ціан було виявлено на кометі Борисова[12], а також в атмосфері Титана[13].
Безпека
Як і інші ціаніди, ціан є дуже токсичним, оскільки він легко перетворюється на ціанід, які отруює цитохром-c-оксидазний комплекс, тим самим перериваючи електронтранспортний ланцюг у мітохондріях.
Ціан подразнює очі та дихальну систему. Його вдихання здатне спричинити головний біль, запаморочення, прискорений пульс, нудоту, блювоту, втрату свідомості, судоми та смерть, залежно від концентрації[14]. Смертельна доза при вдиханні зазвичай коливається від 100 до 150 мг.
Ціан створює друге за температурою полум'я природного походження (після ацетилендінитрилу), коли він горить у кисні — з температурою понад 4525 °C[15][16]. Ціан горючий і легкозаймистий, утворює з повітрям вибухові суміші.
У масовій культурі
У серіалі «Доктор Хто» «Мозок Морбіуса[en]» (5-та серія 13-uj сезону) Доктор синтезує ціан, використовуючи як вихідний матеріал ціанистий водень, і випускає його через трубу, щоб завадити Солонові провести операцію на мозку тіла Морбіуса. Утім, той її завершує, але незабаром після цього помирає від отруєння ціаном.
У фільмі «Мережі зла» (1987) Фрайдей (Ден Екройд) і Стрібек (Том Генкс) вистежують лиходія, який викрав «псевдогалогенову ціанову сполуку»[17].