Tantal(V) chloride
Tantal(V) chloride, hay tantal pentachloride, là một hợp chất vô cơ có công thức hóa học TaCl5. Nó có dạng bột màu trắng và thường được sử dụng làm nguyên liệu ban đầu trong hóa học tantal. Nó dễ bị thủy phân, tạo thành tantal(V) oxychloride (TaOCl3) và tantal(V) oxide (Ta2O5); điều này đòi hỏi nó phải được tổng hợp và sử dụng trong điều kiện khan, sử dụng các kỹ thuật không có không khí.
| Tantal(V) chloride | |
|---|---|
 | |
| Danh pháp IUPAC | Tantalum(V) chloride Tantalum pentachloride |
| Tên khác | Tantal pentachloride |
| Nhận dạng | |
| PubChem | |
| Số EINECS | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | TaCl5 |
| Khối lượng mol | 358,2105 g/mol |
| Bề ngoài | tinh thể đơn nghiêng màu trắng[1] |
| Khối lượng riêng | 3,68 g/cm³ |
| Điểm nóng chảy | 216 °C (489 K; 421 °F) |
| Điểm sôi | 239,4 °C (512,5 K; 462,9 °F) (phân hủy) |
| Độ hòa tan trong nước | phản ứng |
| Độ hòa tan | chloroform, CCl4 tạo phức với amonia |
| MagSus | +1400×10−6 cm³/mol |
| Cấu trúc | |
| Cấu trúc tinh thể | đơn nghiêng, mS72 |
| Nhóm không gian | C2/m, No. 12 |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH | -858,98 kJ/mol |
| Entropy mol tiêu chuẩn S | 221,75 J K−1 mol−1 |
| Các nguy hiểm | |
| NFPA 704 | |
| Điểm bắt lửa | không bắt lửa |
| LD50 | 1900 mg/kg (đường miệng, chuột) |
| Ký hiệu GHS |   |
| Báo hiệu GHS | Danger |
| Chỉ dẫn nguy hiểm GHS | H302, H314 |
| Chỉ dẫn phòng ngừa GHS | P280, P305+P351+P338, P310 |
| Các hợp chất liên quan | |
| Anion khác | Tantal(V) fluoride Tantal(V) bromide Tantal(V) iodide |
| Cation khác | Vanadi(V) chloride Niobi(V) chloride |
| Hợp chất liên quan | Tantal(III) chloride Tantal(IV) chloride |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
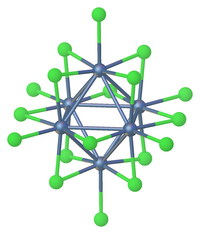
Cấu trúc
TaCl5 kết tinh trong nhóm không gian thuộc hệ tinh thể đơn nghiêng C2/m.[2] Mười nguyên tử chlor xác định cặp bát diện có chung cạnh. Các nguyên tử tantal chiếm các tâm của bát diện và được nối với nhau bằng hai cầu nối chlor. Cấu trúc dimer tồn tại trong các dung môi không phức tạp và phần lớn ở trạng thái nóng chảy. Tuy nhiên, ở trạng thái hơi, TaCl5 là monomer. Monomer này có cấu trúc lưỡng chóp tam giác, giống như cấu trúc của PCl5.[3]
Tính chất vật lý
Độ tan của tantal(V) chloride tăng nhẹ đối với dãy hydrocarbon thơm sau:
Điều này thể hiện ở việc dung dịch có màu đậm dần từ vàng nhạt sang cam. Tantal(V) chloride ít tan trong cyclohexan và carbon tetrachloride hơn trong các hydrocarbon thơm. Các dung dịch như vậy của tantal(V) chloride là chất dẫn điện kém, cho thấy khả năng bị ion hóa thấp. TaCl5 được tinh chế bằng cách thăng hoa để tạo ra các tinh thể hình kim màu trắng.
Tantal(V) chloride có thể được điều chế bằng phản ứng của tantal dạng bột với khí chlor ở nhiệt độ giữa 170 và 250 °C. Phản ứng này cũng có thể được thực hiện với HCl ở 400 °C.[4]
- 2 Ta + 5 Cl2 → 2 TaCl5
- 2 Ta + 10 HCl → 2 TaCl5 + 5 H2
Nó cũng có thể được điều chế bằng phản ứng giữa tantal(V) oxide và thionyl chloride ở 240 °C.
- Ta2O5 + 5 SOCl2 → 2 TaCl5 + 5 SO2
Tantal(V) chloride có sẵn trên thị trường, tuy nhiên các mẫu có thể bị nhiễm tantal(V) oxychloride (TaOCl3), được tạo thành do quá trình thủy phân.
Phản ứng
TaCl5 là chất điện di và nó hoạt động giống như chất xúc tác Friedel–Crafts, tương tự như AlCl3. Nó tạo thành các phức hợp với nhiều base Lewis.[5]
Phức hợp đơn giản
TaCl5 tạo phức ổn định với ether:
- TaCl5 + R2O → TaCl5(OR2) (R = Me, Et)
TaCl5 cũng phản ứng với phosphor pentachloride và phosphoryl trichloride, chất trước đóng vai trò là chất cho chloride và chất sau đóng vai trò phối tử, liên kết qua oxy:
- TaCl5 + PCl5 → PCl+
4TaCl−
6 - TaCl5 + POCl3 → TaCl5·POCl3 (tinh thể không màu)[6]
Tantal(V) chloride phản ứng với các amin bậc ba để tạo ra các phức hợp kết tinh.
- TaCl5 + 2R3N → TaCl5(NR3)
Phản ứng chuyển vị chloride
Tantal(V) chloride phản ứng ở nhiệt độ phòng với lượng dư triphenylphosphine oxide để tạo ra phức hợp oxychloride:
- TaCl5 + 3 OPPh3 → [TaOCl3(OPPh3)]x
Sự hình thành ban đầu được cho là của các chất cộng giữa TaCl5 và các hợp chất hydroxyl như rượu, phenol và acid carboxylic được tạo ra bởi quá trình loại bỏ hydro chloride và hình thành liên kết Ta–O:
- TaCl5 + 3 HOEt → TaCl2(OEt)3 + 3 HCl
Với sự có mặt của amonia như một chất nhận HCl, tất cả năm phối tử chloride đều bị thay thế với sự hình thành Ta(OEt)5. Tương tự, TaCl5 phản ứng với lithi methoxide trong methanol khan để tạo thành các dẫn xuất methoxy có liên quan:
- TaCl5 + 4 LiOMe → Ta(OMe)4Cl + 4 LiCl
Phân giải amoni, phân giải rượu và các phản ứng liên quan
Amonia sẽ thay thế hầu hết các phối tử chloride khỏi TaCl5 để tạo thành chất. Chloride bị chiếm chỗ chậm hơn bởi các amin bậc một hoặc bậc hai nhưng việc thay thế cả năm phối tử chloride bằng các nhóm amido có thể thực hiện bằng cách sử dụng lithi dialkylamide, như được minh họa bằng quá trình tổng hợp pentakis(dimetylamido)tantal:
- TaCl5 + 5 LiNMe2 → Ta(NMe2)5
Với rượu, pentachloride phản ứng để tạo ra alkoxide. Như phương pháp điều chế tantal(V) ethoxide ở trên, các phản ứng thường được tiến hành với sự có mặt của bazơ:
- 10 EtOH + Ta2Cl10 + 10 NH3 → Ta2(OEt)10 + 10 NH4Cl
Tantal(V) chloride bị khử bởi các chất dị vòng nitơ như pyridin.
Phản ứng tạo phức với amonia
Phản ứng của TaCl5 với NH3 ở điều kiện thường sẽ cho sản phẩm là các phức hợp:
- TaCl5 + 17 NH3 → Ta(NH2)2Cl3·7NH3 + 2 NH4Cl·3NH3
Nếu phản ứng được thực hiện ở nhiệt độ thấp, phức TaCl5·12NH3 sẽ được tạo thành ở −81,5 °C (−114,7 °F; 191,7 K). Tăng nhiệt độ lên −67,5 °C (−89,5 °F; 205,7 K) sẽ tạo ra TaCl5·10NH3, ở −44 °C (−47 °F; 229 K) phức TaCl5·7NH3 được tạo thành. Cả ba phức amonia đều có màu trắng. Phức heptaamonia bị phân hủy ở 0 °C (32 °F; 273 K).[7]
- TaCl5·7NH3 → Ta(NH2)2Cl3·3NH3 + 2 NH4Cl
Sự khử
Khử tantal(V) chloride sẽ tạo ra các anion và hợp chất như Ta6Cl184− và Ta6Cl14(H2O)n, với n =4[8], 7, 8[9].
Tham khảo
Đọc thêm
- Ozin, G. A.; Walton, R. A. (1970). “Vibrational spectra and structures of the 1:1 complexes of niobium and tantalum, pentachlorides and tantalum pentabromide with aceto-, perdeuterioaceto-, and propionitriles in the solid and solution states and a vibrational analysis of the species MX5, NC·CY3 (Y = H or D)”. J. Chem. Soc. A: 2236–2239. doi:10.1039/j19700002236.
- Bullock, J. I.; Parrett, F. W.; Taylor, N. J. (1973). “Some metal halide–phosphorus halide–alkyl halide complexes. Part II. Reactions with niobium and tantalum pentachlorides and tungsten hexachloride”. J. Chem. Soc., Dalton Trans. (5): 522–524. doi:10.1039/DT9730000522.
- Đorđević, C.; Katović, V. (1970). “Co-ordination complexes of niobium and tantalum. Part VIII. Complexes of niobium(IV), niobium(V), and tantalum(V) with mixed oxo, halogeno, alkoxy, and 2,2′-bipyridyl ligands”. J. Chem. Soc. A: 3382–3386. doi:10.1039/j19700003382.
- Cowley, A.; Fairbrother, F.; Scott, N. (1958). “The halides of niobium (columbium) and tantalum. Part V. Diethyl ether complexes of the pentachlorides and pentabromides; the solubility of tantalum pentaiodide in ether”. J. Chem. Soc.: 3133–3137. doi:10.1039/JR9580003133.
Liên kết ngoài
| HCl | He | ||||||||||||||||||||
| LiCl | BeCl2 | B4Cl4 B12Cl12 BCl3 B2Cl4 +BO3 | C2Cl2 C2Cl4 C2Cl6 CCl4 +C +CO3 | NCl3 ClN3 +N | ClxOy Cl2O Cl2O2 ClO ClO2 Cl2O4 Cl2O6 Cl2O7 ClO4 +O | ClF ClF3 ClF5 | Ne | ||||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 | Si5Cl12 Si2Cl6 SiCl4 | P2Cl4 PCl3 PCl5 +P | S2Cl2 SCl2 SCl4 +SO4 | Cl2 | Ar | ||||||||||||||
| KCl | CaCl CaCl2 | ScCl3 | TiCl2 TiCl3 TiCl4 | VCl2 VCl3 VCl4 VCl5 | CrCl2 CrCl3 CrCl4 | MnCl2 MnCl3 | FeCl2 FeCl3 | CoCl2 CoCl3 | NiCl2 | CuCl CuCl2 | ZnCl2 | GaCl GaCl3 | GeCl2 GeCl4 | AsCl3 AsCl5 +As | Se2Cl2 SeCl2 SeCl4 | BrCl | Kr | ||||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 | NbCl3 NbCl4 NbCl5 | MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 | TcCl3 TcCl4 | RuCl2 RuCl3 RuCl4 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 | SnCl2 SnCl4 | SbCl3 SbCl5 | Te3Cl2 TeCl2 TeCl4 | ICl ICl3 | XeCl XeCl2 XeCl4 | ||||
| CsCl | BaCl2 | * | LuCl3 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 | ReCl3 ReCl4 ReCl5 ReCl6 | OsCl2 OsCl3 OsCl4 OsCl5 | IrCl2 IrCl3 IrCl4 | PtCl2 PtCl4 | AuCl (Au[AuCl4])2 AuCl3 | Hg2Cl2 HgCl2 | TlCl TlCl3 | PbCl2 PbCl4 | BiCl3 | PoCl2 PoCl4 | AtCl | Rn | |||
| FrCl | RaCl2 | ** | LrCl3 | RfCl4 | DbCl5 | SgO2Cl2 | BhO3Cl | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| * | LaCl3 | CeCl3 | PrCl3 | NdCl2 NdCl3 | PmCl3 | SmCl2 SmCl3 | EuCl2 EuCl3 | GdCl3 | TbCl3 | DyCl2 DyCl3 | HoCl3 | ErCl3 | TmCl2 TmCl3 | YbCl2 YbCl3 | |||||||
| ** | AcCl3 | ThCl4 | PaCl4 PaCl5 | UCl3 UCl4 UCl5 UCl6 | NpCl3 | PuCl3 | AmCl2 AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl3 | FmCl2 | MdCl2 | NoCl2 | |||||||
