Pentaerythrit
Pentaerythrit (nach IUPAC-Nomenklatur 2,2-Bis(hydroxymethyl)-1,3-propan-diol) ist ein 4-wertiger Alkohol. Das Präfix Penta (fünf) weist auf die 5 Kohlenstoffatome hin; Erythrit auf den gleichfalls 4-wertigen Alkohol.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
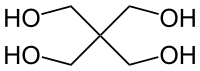 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Pentaerythrit | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C5H12O4 | |||||||||||||||||||||
| Kurzbeschreibung | weißes, kristallines Pulver mit süßlichem Geschmack[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 136,15 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||
| Dichte | 1,396 g·cm−3[3] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt | ||||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Gewinnung und Darstellung
Die technische Herstellung erfolgt durch Umsetzung von Formaldehyd mit Acetaldehyd durch dreifache Aldolreaktion mit anschließender gekreuzter Cannizzaro-Reaktion. Es wird mit molarem Überschuss von Formaldehyd gearbeitet, um die Bildung von Dipentaerythrit zu vermeiden. Pentaerythrit wurde 1882 von Bernhard Tollens entdeckt, als er eine wässrige Lösung von Formaldehyd und Acetaldehyd mit Bariumhydroxid versetzte.
Eigenschaften
Physikalische Eigenschaften
Pentaerythrit ist ein weißes, kristallines Pulver mit süßlichem Geschmack. Es ist in siedendem Wasser gut und in kaltem Wasser mäßig löslich. Es ist wenig löslich in Ethanol und unlöslich in Benzol, Tetrachlormethan, Ether und Petrolether.[2]
Chemische Eigenschaften
Die vier Hydroxygruppen gehen im Wesentlichen die für Alkohole typischen Reaktionen wie Veresterung mit Säuren ein. Bei Veresterung von Pentaerythrit mit Salpetersäure, nicht ganz korrekt Nitrierung genannt, entsteht das Pentaerythrittetranitrat (Nitropenta).
Verwendung
PE wird überwiegend zur Herstellung von Alkydharzen sowie Weichmachern und Emulgatoren verwendet, zusätzlich auch zur Herstellung der Sprengstoffe Pentaerythrittrinitrat und Nitropenta (Pentaerythrittetranitrat).
Literatur
- Beyer / Walter: Organische Chemie, 25. Auflage, S. Hirzel Verlag, Stuttgart 2015, ISBN 3-7776-1673-7.
