Οξείδιο του αργύρου
Το οξείδιο του αργύρου είναι η χημική ένωση με τον χημικό τύπο Ag2O. Είναι μια λεπτή μαύρη ή σκούρα καφετιά σκόνη που χρησιμοποιείται για να παρασκευάσει άλλες ενώσεις του αργύρου.
 | |
 | |
| Ονόματα | |
|---|---|
| ΟνοματολογίαIUPAC Άργυρος(Ι) οξείδιο | |
| ΆλλαΟνόματα Οξείδιο του αργύρου | |
| Αναγνωριστικά | |
| 20667-12-3 | |
| ChemSpider | 7970393 |
| Αριθμός_EC | 243-957-1 |
InChI=1S/2Ag.O/q2*+1;-2 Key: NDVLTYZPCACLMA-UHFFFAOYSA-N InChI=1S/2Ag.O/q2*+1;-2 Key: NDVLTYZPCACLMA-UHFFFAOYSA-N | |
| Jmol 3Δ Πρότυπο | Image |
| MeSH | άργυρος+οξείδιο |
| PubChem | 9794626 |
| Αριθμός RTECS | VW4900000 |
[O-2].[Ag+].[Ag+] | |
| Ιδιότητες | |
| Ag2O | |
| Μοριακή μάζα | 231,74 g·mol−1 |
| Εμφάνιση | Μαύροι/καφέ κρύσταλλοι του κυβικού κρυσταλλικού συστήματος |
| Οσμή | Άοσμο[1] |
| Πυκνότητα | 7,14 g/cm3 |
| Σημείο τήξης | 300 °C (572 °F; 573 K) αποσυντίθεται από ≥200 °C[2][3] |
| Διαλυτότητα στο νερό | 0,013 g/L (20 °C) 0,025 g/L (25 °C)[4] 0,053 g/L (80 °C)[2] |
Γινόμενο διαλυτότητας (Ksp) του AgOH | 1,52·10−8 (20 °C) |
| Διαλυτότητα | Διαλυτό σε οξέα, αλκάλεα Αδιάλυτο σε αιθανόλη[4] |
| −134,0·10−6 cm3/mol | |
| Δομή | |
| Κυβικό | |
Ομάδα χώρου | Pn3m, 224 |
| Θερμοχημεία | |
| 65,9 J/mol·K[4] | |
Πρότυπη μοριακή εντροπία (S | 22 J/mol·K[5] |
Πρότυπη ενθαλπία σχηματισμού(ΔfH | −31 kJ/mol[5] |
Ελεύθερη ενέργεια Γκιμπς (ΔfG˚) | −11.3 kJ/mol[3] |
| Κίνδυνοι | |
| Εικονογράμματα GHS |   [6] [6] |
Δηλώσεις κινδύνου GHS | H272, H315, H319, H335[6] |
Προληπτικές δηλώσεις GHS | P220, P261, P305+351+338[6] |
| NFPA 704 | |
| Θανάσιμη δόση ή συγκέντρωση (LD, LC): | |
LD50 (μέση θανατηφόρα δόση) | 2,82 g/kg (επιμύες, στοματικά)[1] |
| Σχετικές ενώσεις | |
Σχετικές ενώσεις | Άργυρος(I,III) οξείδιο |
Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες (25°C, 100 kPa). | |
| | |
| Infobox references | |
Παρασκευή

Το οξείδιο του αργύρου μπορεί να παρασκευαστεί με επίδραση αραιών διαλυμάτων νιτρικού αργύρου και υδροξειδίου αλκάλεως.[7][8] This reaction does not afford appreciable amounts of silver hydroxide due to the favorable energetics for the following reaction:[9]
- 2 AgOH → Ag2O + H2O (pK = 2,875)[10])
Η ευρεσιτεχνία ΗΠΑ 20050050990 περιγράφει την παρασκευή του Ag2O με ιδιότητες κατάλληλες για χρήση ως λεπτού κοκκώδους αγώγιμου πληρωτή αλοιφής.
Δομή και ιδιότητες
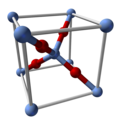
Το Ag2O χαρακτηρίζεται ως γραμμικό, με διδεσμικά κέντρα Ag συνδεμένο με τετραεδρικά οξείδια. Είναι ισοδομικό με το Cu2O. "Διαλύεται" σε διαλύτες που το αποσυνθέτουν. Είναι ελαφρά διαλυτό στο νερό λόγω του σχηματισμού του ιόντος Ag(OH)2− και πιθανόν συσχετίζεται με τα προϊόντα υδρόλυσης.[11] Διαλύεται σε διάλυμα αμμωνίας για να δώσει διαλυτά παράγωγα.Πολτός του Ag2O προσβάλλεται άμεσα από οξέα:
- Ag2O + 2 HX → 2 AgX + H2O
όπου HX = HF, HCl, HBr, ή HI, HO2CCF3. Αντιδρά επίσης με διαλύματα χλωριούχων αλκαλίων για να καθιζήσει χλωριούχο άργυρο (silver chloride), αφήνοντας διάλυμα του αντίστοιχου υδροξειδίου του αλκάλεως.[11][12]
Όπως πολλές ενώσεις του αργύρου, το οξείδιο του αργύρου είναι φωτοευαίσθητο. Αποσυντίθεται επίσης σε θερμοκρασίες πάνω από 280 °C.[13]
Εφαρμογές
Αυτό το οξείδιο χρησιμοποιείται σε κάποιες μπαταρίες οξειδίου του αργύρου, όπως στο μικτό οξείδιο αργύρου(I,III), Ag4O4. Στην οργανική χημεία, το οξείδιο του ασβεστίου χρησιμοποιείται ως ήπιο οξειδωτικό μέσο. Παραδείγματος χάρη, οξειδώνει τις αλδεΰδες σε καρβοξυλικά οξέα. Τέτοιες αντιδράσεις δουλεύουν καλύτερα όταν το οξείδιο του αργύρου έχει παρασκευαστεί επί τόπου από νιτρικό άργυρο και υδροξείδιο αλκάλεως.
Παραπομπές
Εξωτερικοί σύνδεσμοι
- Annealing of Silver Oxide – Demonstration experiment: Instruction and video
- Silver Oxide, Ag2O
