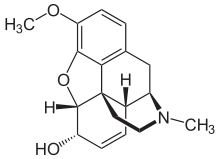
Morphine
| Morphine | ||
 | ||
 | ||
| Structure 2D de la morphine et animation 3D. | ||
| Identification | ||
|---|---|---|
| DCI | Morphine | |
| Nom UICPA | 17-méthyl-7,8-didéshydro-4,5α-époxymorphinan-3,6α-diol | |
| No CAS | (sulfate de morphine) | |
| No ECHA | 100.000.291 | |
| No CE | 200-320-2 | |
| No RTECS | QC8760000 (pentahydrate de sulfate) | |
| Code ATC | N02 | |
| DrugBank | DB00295 | |
| PubChem | 5288826 | |
| ChEBI | 17303 | |
| SMILES | ||
| InChI | ||
| Apparence | Poudre blanche • Solution limpide | |
| Propriétés chimiques | ||
| Formule | C17H19NO3 [Isomères] | |
| Masse molaire[1] | 285,337 7 ± 0,016 g/mol C 71,56 %, H 6,71 %, N 4,91 %, O 16,82 %, | |
| pKa | 7,9[réf. souhaitée] | |
| Propriétés physiques | ||
| T° fusion | 195 à 200 °C[réf. souhaitée] | |
| T° ébullition | 254 °C[réf. souhaitée] | |
| Solubilité | 0,15 g L−1 dans l'eau à 20 °C[2] | |
| Masse volumique | 1,31 g cm−3[réf. souhaitée] | |
| Précautions | ||
| SGH[3] | ||
| H302 | ||
| Données pharmacocinétiques | ||
| Biodisponibilité | Orale : ~30 % Sous-cutanée : ~50 % | |
| Liaison protéique | 30–40 % | |
| Métabolisme | Hépatique (90 %) | |
| Demi-vie d’élim. | 2 à 3 heures (métabolite actif 3-6 heures) | |
| Excrétion | ||
| Considérations thérapeutiques | ||
| Classe thérapeutique | Analgésique opioïde • Stupéfiant | |
| Voie d’administration | Orale, sous-cut., IV, IM, péridurale, intrathécale | |
| Grossesse | Utilisable, dans certaines conditions | |
| Conduite automobile | Dangereuse | |
| Précautions | Dépresseur respiratoire | |
| Antidote | Naloxone | |
| Caractère psychotrope | ||
| Catégorie | Dépresseur opioïde | |
| Mode de consommation | Ingestion, insufflation (sniff), inhalation (fumée), injection | |
| Risque de dépendance | Très élevé (physique et psychique) en cas d'usage non thérapeutique | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier | ||
La morphine (du grec Μορφεύς, Morphée, dieu grec du sommeil et des rêves) est le principal alcaloïde de l'opium, le latex du pavot somnifère (Papaver somniferum). C'est une molécule complexe utilisée en médecine comme analgésique (médicament utilisé pour lutter contre la douleur) et comme drogue pour son action euphorisante.
L'opium est utilisé en médecine depuis le IIIe millénaire av. J.-C. dans diverses cultures[4] et fut l'un des piliers de la pharmacopée traditionnelle mais la morphine n'est néanmoins découverte et isolée qu'en 1804 ; sa nature chimique et son usage pharmaceutique furent établis dans les années suivantes par l'Allemand Friedrich Wilhelm Sertürner, révolutionnant l'analgésie dans la médecine[5].
Elle est l'anti-douleur de référence, l'un des plus efficaces et l'un des plus utilisés dans le monde, celui auquel est comparée l'efficacité des autres médicaments à visée anti-douloureuse. Présente sous forme orale à libération prolongée ou immédiate ou en solution pour injection sous cutanée ou intraveineuse, elle occupe toujours une place de choix dans l'arsenal thérapeutique contre les douleurs intenses ou rebelles, notamment d'origine cancéreuse[6],[7],[8].
Sa pharmacologie est l'une des mieux connues et explorées, et une grande partie de la grande variété de ses effets est bien documentée. Elle agit en activant les récepteurs opiacés (récepteur µ). Elle induit une analgésie profonde et une dépression respiratoire pouvant mener à la mort par asphyxie. Un état d'euphorie parfois intense est provoqué par la morphine, ce qui en favorise l'usage abusif[9].
Son usage prolongé provoque l'apparition d'une accoutumance : les doses de morphine nécessaires pour égaler les effets de la première prise peuvent croître énormément (il est par exemple possible de devoir passer de 5 mg de morphine à 20 mg lors d’un usage prolongé afin de ressentir les mêmes effets qu’initialement), cette augmentation intensifiant alors significativement hors d’un usage médical les risques d’overdose et de dépressions respiratoires pouvant mener à la mort, ainsi qu'une dépendance associée à un syndrome de sevrage dont la sévérité dépend de la durée de l'usage et des doses absorbées[10].
La morphine est ainsi classée comme stupéfiant dans la plupart des pays du monde.
De la morphine ont été dérivés de nombreux composés d'action similaire comme l'héroïne, plusieurs autres ont été synthétisés à partir de la thébaïne (un autre alcaloïde de l'opium) comme l'oxycodone, la buprénorphine et l'hydromorphone. Par ailleurs, d'autres molécules structurellement différentes comme le fentanyl, la méthadone ou le tramadol possèdent des activités analgésiques comparables, se liant aux mêmes récepteurs et sont ainsi regroupés dans la famille des narcotiques. Tandis que les substances issues de l'opium sont appelés les opiacés, les substances qui partagent des effets voisins à la morphine et qui se fixent aux mêmes cibles au sein du cerveau sont appelées les opioïdes.
Provenance

La morphine est principalement présente dans le latex du pavot somnifère (Papaver somniferum), mais aussi dans celui d'autres espèces du genre Papaver comme Papaver dubium (Pavot douteux) et Papaver argemone[11].
L'opium brut, selon les variétés et la provenance, contient entre 4 et 21 % de morphine[12]. L'opium officinal, de qualité pharmaceutique standardisée, doit titrer 10 % de morphine.

La morphine et les autres alcaloïdes de l'opium sont synthétisés dans la plante de pavot au niveau des cellules lactifères dans les bulbes[13] à partir de la tyrosine, un acide aminé courant dans la nature, qui est transformé en réticuline puis en salutaridine[14].
La production du latex est maximale quelques jours après la chute des pétales et sa récolte s'effectue à ce moment-là. Le latex est ensuite mis à sécher, utilisé tel-quel ou purifié pour le fumer ou en extraire la morphine, la codéine ou la thébaïne.

L'extraction peut se faire par différentes méthodes, dont la plupart utilisent l'action de la chaux ou du chlorure de calcium, avant d'être précipitée par l'action du chlorure d'ammonium ou de l'acide chlorhydrique pour faire précipiter la morphine sous forme de sel chlorhydrique (chlorhydrate de morphine)[15]. La morphine peut également être retrouvée à partir de la thébaïne, au cours de procédés industriels.
Ces méthodes sont pratiquées industriellement ou par des laboratoires clandestins en vue de préparer l'héroïne par acétylation de la morphine.
La France et l'Australie sont les principaux producteurs légaux de morphine[16],[17].
Histoire
Connue comme l'une des premières drogues de l'histoire, différentes sources historiques témoignent de l'utilisation du pavot par les Sumériens, Égyptiens, Grecs, Romains et de nombreux peuples de l'Antiquité, principalement pour ses vertus sédatives et antalgiques. Pline l'Ancien le mentionne dans son Histoire naturelle, et en décrit l'usage et les effets, et le célèbre Galien l'utilise déjà au IIe siècle[18]. Occupant une place de choix dans la pharmacopée européenne durant le Moyen Âge et la Renaissance, cultivé dans le jardin des monastères[19],[20] comme plante officinale, il est sélectionné : le pavot originel hypothétique papaver setigerum est devenu le cultivar que nous connaissons aujourd'hui, papaver somniferum. En effet, il n'existe aucun spécimen de pavot connu à l'état sauvage[4].
Dès 1688, Daniel Ludwig, médecin du duc de Saxe-Gotha, signale dans sa « dissertation de pharmacie » la morphine sous le terme de « magistère d'opium »[21],[22],[23]. Il extrait la morphine par extraction acide-base puis précipitation. La morphine ne sera cependant vraiment découverte qu'à partir de 1804. La morphine et ses sels (Codex de 1866) deviendra l'analgésique par excellence des syndromes douloureux, aigus ou chroniques[24],[25].

Découverte
La morphine fut découverte simultanément en 1804 par Armand Seguin et Bernard Courtois, ainsi que par Jean-François Derosne (« sel de Derosne »)[26], mais c’est à Friedrich Wilhelm Sertürner, jeune pharmacien d'Eimbeck près de Hanovre, que revient le mérite.
Friedrich Sertüner publie en 1805 une étude préliminaire dans Journal der Pharmacie de Johann Trommsdorff puis en 1806 l'article final dans lequel il précise n'avoir pris connaissance des découvertes de Derosne qu'après avoir abouti à ses propres conclusions. En 1811, il publie plusieurs articles dans le Journal der Pharmacie de Johann Trommsdorff où il affirme clairement la qualité d'alcali du principium somniferum. En 1815, il identifie plusieurs composants.

C'est finalement un article paru en 1817 dans Annalen der Physik de GIlbert qui fait connaître ses travaux sur la substance que Sertürner nomme désormais « Morphium » en référence à Morphée, et sur l'autre composant qu'il isole de l'opium : l'« acide méconique »[27].
Gay-Lussac fait traduire et publier immédiatement cet article dans les prestigieuses Annales de Chimie. C'est lui qui introduit le terme « Morphine ». Dans la préface qu'il adjoignit à cette traduction, Gay-Lussac amorça notamment un système de standardisation de la nomenclature de chimie organique qui eut pour première illustration l'apparition du terme de « morphine ». Gay-Lussac demanda à Robiquet de vérifier les résultats de Sertrüner : le « sel de Derosne » s'avéra être une substance différente de la morphine. Robiquet nomma la substance purifiée issue des sels de Derosne « narcotine » (alors même que ces sels étaient dépourvus de propriété narcotique)[28].
La querelle de la priorité de la découverte de la morphine est tranchée en 1831 quand Sertürner reçoit le prix Montyon de l'Institut de France[29].
Préparée par la combinaison avec des acides, la morphine formait différents sels : l'acétate de morphine, le sulfate et le chlorhydrate de morphine.
La découverte de la morphine et d'autres alcaloïdes est un point crucial dans le développement de la chimie organique dans l'histoire[30].
Développement
En 1818, Magendie fait savoir qu'il a réussi à soulager les souffrances d'une femme. Il utilise alors de la morphine à la place de l’opium en pratique clinique avec prescription orale comme sédatif et antalgique. C'est en 1819 que figure pour la première fois sur un formulaire de prescription des hôpitaux de Paris, une préparation buvable d'acétate de morphine[31] mais seulement en 1822 que la parution de son Formulaire fait connaître la morphine au monde médical. Il en caractérise l'usage sous forme de sulfate et d'acétate[32]. L'entrée de la morphine se fait alors dans la thérapeutique grâce aux préparations de sels de morphine à base d'acétate de morphine que Magendie appelait « gouttes calmantes ».
En 1828, Bally, fort d'une étude portant sur plus de 700 malades, précise les effets de la morphine ; il publie ses Observations sur les effets thérapeutiques de la morphine ou narcéine ; en 1823, Bally étudiait les effets de l'acétate de morphine à l'exclusion de tous les autres sels[33].
En 1831, William Grégory, à Édimbourg, fait connaître un procédé pour obtenir du chlorhydrate de morphine à un coût comparable à celui du Laudanum et très pur. Ce produit est commercialisé dès 1833[34].
En 1832, examinant le procédé de Gregory, Robiquet met au jour une autre substance active de l'opium, la codéine[35].
La galénique se limitait alors souvent aux formulations per os, principalement des solutions ou des sirops.
L'usage de la voie endermique, qui consistait à déposer de la poudre sur une portion de peau mise à nu par un vésicatoire, le marteau de Mayor ou par les cantharides, était alors marginal et fut étudié pour le traitement des rhumatismes ; en 1837, Lafargue, utilisant une lancette, pratiquera une inoculation sous-cutanée qualifiée de « vaccination morphinique »[36].
La morphine va rencontrer l’invention de la seringue hypodermique à aiguille creuse du médecin orthopédiste lyonnais Charles Pravaz en destiné au départ à l'injection de fer coagulant dans le traitement des anévrismes. C'est le médecin écossais Alexander Wood qui pratiqua toutefois le premier l'injection sous-cutanée de morphine ; puis, dans une série d'observations qu'il publia en 1855, il remarqua l'efficacité des injections pratiquées, notamment celles qui contenaient le chlorhydrate de morphine, contre les névralgies.
Les formes galéniques pour injection intraveineuse de morphine chez l'homme n'auront cours qu'au vingtième siècle, notamment en association avec la scopolamine.

L'apparition de la forme injectable, particulièrement sur les champs de bataille (guerre de Sécession aux États-Unis, guerre de Crimée, guerre austro-prussienne, guerre franco-prussienne de 1870 en Europe, etc.) révolutionne le traitement des blessures et de la chirurgie, notamment dans le cas des amputations qu'elle rend mieux tolérables par le patient.
C'est dans ce contexte d'utilisation en médecine militaire apparaît ce que l'on appelle alors la « maladie du soldat » puis « morphinisme » et enfin « morphinomanie ».

Pendant la guerre de 1870, la morphine est distribuée sans retenue aux blessés ; elle est également distribuée aux combattants valides à qui elle donne le courage de monter au front[37],[38]. Les premières descriptions de morphinomanie apparaissent dès [5] d'autant qu'elle est alors en vente libre dans de nombreuses préparations pharmaceutiques artisanales pour soigner les maux les plus divers. L'opium était toutefois bien plus largement répandu.
En , le Dr Levinstein et le pharmacologue Louis Lewin introduisent la notion de manie issue de la psychiatrie, alors naissante, et décrivent pour la première fois ce que l'on appellera « toxicomanie » stigmatisant pour le grand public la morphine dans cette image péjorative. Son prix moins accessible que l'alcool en fait un produit en vogue dans l'aristocratie jusqu'au début du XXe siècle et nombre de personnages connus sont réputés pour leur morphinomanie : Baudelaire, John Pemberton, Béla Lugosi, Hermann Göring, Otto von Bismarck, Alphonse Daudet, Jules Verne à la suite d'une balle dans le pied[39], plus tard Édith Piaf, etc. En cette fin de XIXe siècle, la morphine est un des médicaments les plus populaires de tous les temps et l'un des plus efficaces.
La morphinomanie est alors très répandue dans les couches aisées, et les méthodes de désintoxication ou de sevrage sont multiples, avec des abus. Les protocoles de sevrage vont alors de la suppression brusque de la morphine au sevrage dégressif, au frais du patient, comme le dénonce à l'époque Laurent Tailhade dans son pamphlet La « Noire Idole »[40]. Les jugements moraux sont alors monnaie courante, et à leurs côtés les préjugés raciaux ou politiques[41],[42].
La morphine, bien que crainte pour l'accoutumance qu'elle produit, est également donnée aux soldats pendant la Première Guerre mondiale, sur le front comme à l'arrière[43]. Certains en deviennent dépendants, comme Hermann Göring, soigné à l'origine pour une blessure à la jambe.


En 1874, Alder Wright découvre la diacétylmorphine, nommée « héroïne » en référence aux espoirs qu'elle suscite alors en tant que remplaçant éventuel de la morphine, source d'addictions. Outre son usage comme antalgique (analgésique), antitussif notamment en sirops[44] (dont elle a conservé l'indication à travers sa prodrogue la codéine), elle était utilisée aux États-Unis d'Amérique pour soigner toute une gamme d'affections mentales (alcoolisme, dépression, psychose maniaco-dépressive, hystérie, les mères en donnaient à leurs enfants pour les endormir, etc.) jusqu'aux mesures prises par l'Opium Act en 1906 (qui prohibent la production, le commerce, la détention et l'usage des drogues d'opium et ses dérivés aux États-Unis).
La pharmacologie de la morphine commence à être catégorisée, et la dépendance qu'elle induit lui est attribuée, malgré des débats[45].
Dans des articles parus en 1923[46] puis en [47], les chimistes britanniques J. Masson Gulland et Robert Robinson rendent compte de sa structure moléculaire complexe. Cette formulation chimique ne sera définitivement acceptée qu'en 1950[48].
Au début des années 1950, on redécouvre les bienfaits de la morphine grâce au cocktail de Brompton, mais en le réservant pour apaiser les souffrances à la fin de la vie. Ce cocktail était composé d'un mélange de morphine, de cocaïne (ou d'amphétamine) et d'un sédatif comme l'alcool ou la chlorpromazine. La morphine est notamment utilisée durant l'expédition française à l'Annapurna par le médecin de l'expédition, le Dr Oudot en association avec la scopolamine, pour soulager les douleurs des membres gelés et induire le sommeil en haute altitude[49].
En France, Henri Laborit élabore un cocktail injectable associant opiacés et neuroleptiques qui fut utilisé pendant la guerre d'Indochine pour faciliter le transfert des blessés vers l'arrière où on pouvait les opérer. Ce mélange fut précurseur de la neuroleptanalgésie.
En 1973, des chercheurs suédois et américains mettent en évidence, in vitro, l'existence de récepteurs spécifiques aux opioïdes au niveau du système nerveux central.
En , en Écosse, Hughes et Kosterlitz partent de l'hypothèse que la morphine « végétale » doit prendre la place sur les récepteurs de molécules endogènes. Ils découvriront ainsi les endomorphines, « morphines » naturellement produites par le corps humain, qu'ils nommeront « enképhalines ». Cette découverte ouvrira la voie à une multitude d'autres qui permettront dans les années 1980 de mieux comprendre le fonctionnement de la douleur et de l'action de la morphine.

Les années 1980 voient de nombreux progrès dans l'adaptation des doses aux besoins des patients et dans la mise au point de nouvelles voies d'administration.

Définie comme une priorité, la lutte contre la douleur passe alors par la redécouverte des opiacés et leur usage croissant. Ainsi, de nouvelles formes galéniques de la morphine, notamment à libération prolongée comme le Skénan, le Moscontin ou le Kapanol, et à libération immédiate comme l'Actiskénan. L'arrivée sur le marché d'autres antalgiques comme l'oxycodone signe également ce renouveau. Le développement des centres de lutte contre la douleur en France et au Canada s'est fait au début des années 2000. Le mésusage de ces spécialités est également apparu, de même que leur utilisation comme substitut d'autres opiacés comme l'héroïne.
Pharmacologie
La morphine est un composé dont la pharmacologie est une des mieux connues et explorées. Les nombreux effets de la morphine conditionnent ses nombreuses applications thérapeutiques.
Pharmacodynamie
La morphine, comme d'autres opioïdes, agit comme agoniste des récepteurs opioïdes μ (mu) (MOR), κ(kappa) (KOR) et δ(delta) (DOR). Ce sont des protéines transmembranaires, enchâssées dans la membrane du neurone, qui appartiennent à une classe très répandue de récepteurs particuliers : les récepteurs couplés aux protéines G.
Quand la morphine se fixe sur le récepteur, celui ci transmet l'information à une Protéine G à activité GTPase (elle hydrolyse le GTP) dont la sous-unité alpha (α) échange le GDP qui y est associé avec un GTP ce qui va aboutir (selon le modèle classique) à sa dissociation du reste de la protéine, la sous-unité alpha ainsi libérée va engendrer la production de seconds messagers qui iront activer différents mécanismes. C'est une réaction en cascade.
Grâce à son activité GTPase la sous-unité (α) va pouvoir hydroliser le GTP en GDP et se réassocier aux autres sous-unités de la protéine G, pouvant ainsi être réactivée.

La morphine stimule ainsi plusieurs récepteurs normalement activés par des molécules endogènes, les endorphines produites par l'hypophyse[50] dans des circonstances particulières comme l'orgasme, l'effort physique[51], le stress[52] ou même l'acupuncture[53].
Ces récepteurs sont situés dans tout le système nerveux central et sont impliqués particulièrement dans le phénomène de perception de la douleur et son contrôle. L'activation de ces récepteurs produit une cascade d'effets et la production de seconds messagers qui exercent une multitude d'activité, à la fois sur le côté pré-synaptique et le côté post-synaptique de la synapse, ce qui contribue à la variabilité d'effets, à la fois inhibiteurs et stimulants[54].
Elle provoque de nombreux effets cliniques et psychiques liée principalement à l'activation des récepteurs μ. La dépression du système nerveux central complexe est responsable de l'effet antalgique (contre la douleur) principalement dans la substance grise périaqueducale. De plus :
- elle agirait sur le système nerveux central au niveau de la perception de la douleur ;
- elle agirait également sur la moelle épinière sur la transmission de la douleur et son rétrocontrôle descendant ;
- mais aussi plus ou moins indirectement au niveau du tronc cérébral, région responsable du contrôle de la respiration. La morphine inhibe également la libération de noradrénaline et de substance P, ce qui pourrait contribuer à son effet antalgique.


Effets neurologiques centraux
Son action dépressive centrale[55] est dose-dépendante[56].
De par sa stimulation des récepteurs opiacés μ, κ et δ, présents surtout dans la moelle (dans la corne dorsale) et dans le cerveau au niveau du plancher du IVe ventricule et de la substance grise périaqueducale, elle induit des symptômes comme la dépression respiratoire et le myosis (contraction importante de la pupille, typique des opiacés).
Elle agit également sur le jugement, le contrôle des émotions et des actions, la coordination mais aussi, par son actions sur le tronc cérébral, sur le rythme cardiaque (tendance à la bradycardie) et sur la tension artérielle (tendance à l'orthostatisme)[57]. Sa modification des taux de glutamate et de substance P est directement reliée à son action sur la douleur[57].
La morphine est à la fois un dépresseur et un stimulant : elle est responsable d'une sédation importante, comme d'une stimulation suivant les doses utilisées. En effet, la prise de morphine stimulerait certaines capacités intellectuelles lors de tests psychométriques[58].
Elle exerce une stimulation de l'area postrema, responsable du contrôle des vomissements, ce qui provoque de la nausée et augmente la libération de dopamine dans le noyau accumbens[59]. Ces deux zones sont riches en neurones dopaminergiques et jouent également un rôle dans les sensations de plaisir. Elle augmente la pression intracrânienne.
D'un point de vue clinique, elle provoque : trémulations, troubles du sommeil, hyperactivité, hyperexcitabilité, hypertonie et convulsions spécialement chez le sujet jeune ou naïf à la morphine[60].
Lors d'un usage prolongé, la morphine accroît la sensibilité à la douleur, et ce phénomène est de plus en plus étudié. Véritable défi pour les médecins de la douleur, ce phénomène nommé hyperalgésie aggrave la tolérance et pose un problème conséquent de traitement au long cours de la douleur. Il semble être partiellement évitable par la rotation des opioïdes, et peut être traité par l'adjonction d'anti-inflammatoires comme les coxibs[61],[62],[63],[64]. Le Néfopam peut également être utilisé.
Des molécules antagonistes des récepteurs NDMA, comme la kétamine ou le dextrométhorphane, sont utilisées en médecine de la douleur pour réduire l’effet hyperalgique des morphiniques[65], tout comme les gabapentinoïdes (en). Ces dernières molécules partagent également la propriété de réduire la tolérance aux morphiniques, et la gabapentine et la prégabaline potentialisent l’action analgésique de la morphine, et réciproquement.
Effets digestifs
L'action des opioïdes et de la morphine sur le tube digestif est bien connue et est essentiellement spasmodique, ce qui conduit à une constipation. Elle s'explique notamment par l'action de la morphine sur le système nerveux entérique (les plexus myentériques et sous muqueux)[54]. La morphine provoque notamment des spasmes du sphincter d'Oddi[66], ce qui conduit à des douleurs abdominales (crampes). L'observation de la constipation produite par les opioïdes a conduit à l'élaboration de traitements des diarrhées comme le lopéramide.
Effets hormonaux
La morphine exerce des effets neuro-endocriniens sur l'hypophyse et l'hypothalamus, dont elle déséquilibre le complexe, provoquant d'importants effets neuro-endocriniens comme la baisse considérable du taux de testostérone chez l'homme (hypogonadisme), pouvant provoquer des troubles de l'érection[67],[68],[69].
Ces déséquilibres, désignés par le terme d'hypogonadisme ou d'endocrinopathies sont désormais bien documentés et semblent être dépendants des doses utilisées. Les endocrinopathies consécutives au traitement par la morphine semblent être très fréquentes[70],[71],[72].
Il semblerait que les opioïdes exercent de nombreux autres effets hormonaux et neuro-hormonaux, comme la baisse du taux extracellulaire de glutamate[73] ou la modulation de la communication des fibroblastes du rein[74].
Elle provoque un retard à l'éjaculation à court terme, et est utilisé comme aphrodisiaque, mais favorise la survenue de troubles de l'érection et de troubles de l'éjaculation à long terme. Le sevrage est notamment caractérisé par l'apparition d'une éjaculation précoce[69].
La morphine possède également un potentiel effet immunosuppresseur et diminue la résistance aux infections en inhibant la réponse des macrophages[75] et serait également impliquée dans une perte d'efficacité des traitements anticancéreux (adduits de cis-platine)[76]. Elle semble stimuler faiblement la croissance des tumeurs[77] contrairement à d'autres opioïdes[78]. Ces données d'oncologie sont peu documentées.
L'interaction avec d'autres produits comme l'alcool, les antihistaminiques ou les tranquillisants majorent le risque de dépression respiratoire et de surdose[79].
La prise de morphine est également un facteur de libération d'histamine, ce qui peut mener à un prurit[55] (envie de se gratter).
Pharmacocinétique
La morphine subit un effet de premier passage hépatique important, c'est-à-dire qu'elle est beaucoup dégradée quand elle entre dans le foie après avoir été absorbée par les capillaires sanguins du système porte (dans l'intestin et l'estomac) et possède donc une biodisponibilité limitée (de l'ordre de 30 %) lorsqu'elle est prise par voie orale.

Elle est également produit par le métabolisme de la codéine par le CYP2D6, laquelle n'exerce ses effets que par cette transformation. Le pic plasmatique est atteint en 45 minutes lors d'une prise par voie orale[80].
La pharmacocinétique de la morphine influence beaucoup ses effets car certains de ses métabolites sont actifs[81].
Ainsi, la morphine est pour la plus grande partie transformée dans les reins, le foie et la rate[82] par glucuronoconjugaison, et transformée en métabolites dont certains sont actifs par une enzyme de phase II, l'UDP-glucuronyl-transférase.[83]
Les plus importants est la morphine-3-glucuronide (M3G) et la morphine-6-glucuronide (M6G). Des métabolites mineurs sont également formés (normorphine, codéine et morphine-3-sulfate). La M6G possède une activité opioïde intrinsèque importante[84]. la M3G possède quant à elle un profil pharmacologique complexe et semblerait contrer l'action analgésique de la morphine[85] mais pas de façon significative[86]. Elle serait impliquée dans la tolérance à la morphine par son activation du récepteur TLR4[87].
L'accumulation de M6G, notamment en cas d'insuffisance rénale, est associée avec une augmentation de certains effets secondaires comme la dépression respiratoire ou les nausées[88].
La morphine est également déméthylée[89].
La morphine passe la barrière placentaire et atteint le fœtus en cas de grossesse[90].
Effets indésirables
La morphine possède de nombreux effets secondaires qui vont de pair avec sa grande efficacité (liste non exhaustive) :
Des troubles digestifs :
- nausées et vomissements surtout au début de l'administration ;
- prurit (rare) ;
- constipation ;
- douleur abdominale, spasmes digestifs.
Des troubles neurologiques ou d'origine neurologique (centrale) ;
- hypotension, notamment orthostatique. Les sujets âgés sont plus affectés par cet effet, du fait de la désensibilisation des barorécepteurs avec l'âge ;
- bradycardie ;
- somnolence ;
- hallucinations, surtout chez les personnes âgées ;
- sécheresse buccale (très fréquente)[91] ;
- rétention urinaire ;
- dépression respiratoire : bradypnée, respiration de cheyne-stockes, arrêt respiratoire ;
- hyperalgésie, notamment après usage prolongé[61],[62],[63],[64]. En effet, cet effet paradoxal de la morphine consiste en une sensibilité accrue à la douleur. Il est prévenu par la rotation des opioïdes, mais aussi par l'introduction d'autres antalgiques.
Des troubles hormonaux :
- retard d'éjaculation ;
- troubles de l'érection (à long terme) ;
- déséquilibre de l'axe hypothalamo-hypophysaire.
En cas d'administration de longue durée, certains symptômes comme les nausées cessent, tandis que d'autres comme la constipation, perdurent et doivent être traités.
En effet les effets secondaires de la morphine sont souvent traités :
- la nausée est souvent traitée par des antiémétiques comme la dompéridone ou la métopimazine ;
- la constipation est prévenue par l'usage de laxatifs osmotiques comme le macrogol.
Surdosage (overdose) et toxicité
| Dose létale de morphine chez différentes espèces | ||
|---|---|---|
| Espèces | Voies d'administration | DL50 en mg/kg |
| Rat | orale | 170 |
| intraveineuse | 46 | |
| Souris | orale | 670 |
| intraveineuse | 200 | |
| Chien | intraveineuse | 316 |
Le surdosage de morphine, à l'instar des autres opioïdes, est une urgence médicale et un événement grave dont les symptômes sont l'apparition d'un état de somnolence, d'hypothermie et d'hypotension, et rapidement une dépression respiratoire[92]. Un myosis accompagne ces symptômes et si un état d'hypoxie s'installe, l'apparition d'une mydriase est un signe de grande gravité. Le traitement d'urgence est la naloxone, antagoniste global des récepteurs opioïdes[93].
En l'absence de traitement, et en fonction de la sévérité des symptômes, de la dose absorbée et de nombreux paramètres, la plupart des cas évoluent vers la dépression cardio-respiratoire généralisée, puis rapidement vers le décès par hypoxie cérébrale. Si le traitement est entrepris trop tard, des lésions irréversible peuvent survenir.
Le traitement débute en priorité par une ventilation assistée pour pallier la dépression respiratoire puis éventuellement l'absorption de charbon actif pour éliminer le médicament non absorbé, notamment lorsqu’une formulation à libération modifiée a été avalée. Le lavage gastrique n'est plus recommandé[94],[95],[96],[97].
Le traitement médicamenteux passe ensuite par l'utilisation d'un antagoniste des récepteurs des opiacés, en général de la naloxone, antidote spécifique de la dépression respiratoire par les opiacés. Le traitement débute à 0,2 mg de naloxone par voie intraveineuse suivie par des administrations supplémentaires de 0,1 mg toutes les deux minutes.

Lors d'un surdosage massif, on administre de la naloxone à la dose de 0,4–0,8 mg par voie intraveineuse. Les effets de la naloxone sont d'une durée relativement brève, une perfusion de naloxone peut être installée jusqu'à ce qu'une respiration spontanée revienne. Une certaine quantité de morphine (ou ses métabolites) peut persister dans le sang jusqu'à 24 heures après l'administration, et le traitement du surdosage de morphine est adapté en conséquence.
La naloxone, principal antagoniste des récepteurs de la morphine, est administrée avec précaution chez les personnes ayant une dépendance physique à la morphine, une inversion brutale ou complète des effets des opiacés pouvant précipiter un syndrome de sevrage aigu.
Des préparations pour administration intranasale sont désormais distribuées (souvent gratuitement) par les acteurs de la réduction des risques, d'accompagnement et d'information que sont les CSAPA et CAARUD, notamment au Canada et en France sous les noms de Narcan ou Nalscue. Le produit n'est cependant pas disponible en pharmacie en France[98].
La dose nécessaire pour atteindre une toxicité par surdosage dépend de la présence d'un état douloureux ou non et de son intensité. Ainsi, des cas de patients douloureux ou des toxicomanes s'administrant du sulfate de morphine par voie orale, sont connus pour avoir pris plus de 1 000 mg par jour sans présenter des signes de surdosage[99],[100].
Chez une personne normale, la dose minimum létale du sulfate de morphine est de 120 mg[101]. Or, dans des cas d'hypersensibilité, une dose de 60 mg peut s'avérer fatale. Différentes méthodes de consommation produisent des effets bien différents aux mêmes doses, avec une multiplication par 3 de la puissance des effets en cas d'injection, comparé à l'ingestion[102]. Chez des morphinomanes très dépendants (avec une grande accoutumance), une dose de 2 000–3 000 mg/j peut être tolérée[103].
Accoutumance et addiction
La morphine est une substance fortement addictive, mais l'accoutumance et l'addiction sont des phénomènes qui dépendent de nombreux facteurs : l'âge, le sexe, le métabolisme, les doses employées, la durée de traitement et la susceptibilité individuelle, notamment à des facteurs d'origine génétique.
Historiquement, l'addiction à la morphine fut un fléau entre les XIXe et XXe siècles, dans le corps médical comme dans les milieux artistiques et littéraires, et fut alors intensément représentée dans l'art notamment pictural, signifiant par là son importance cruciale dans la culture de l'époque[104].
Accoutumance


Comme la plupart des opioïdes, et par des mécanismes complexes et encore mal connus, les individus qui consomment de la morphine développent une accoutumance (besoin d'augmenter les doses pour obtenir des effets similaires) aux effets de la morphine comme la nausée, l'analgésie ou l'euphorie. Cette accoutumance est favorisée par et implique, selon un mécanisme circulaire, l'augmentation des doses.
Les récepteurs à la morphine se modifient, dans leur structure lors de son administration fréquente, ils sont moins efficaces pour recevoir la morphine et pour transmettre le signal[105]. Ainsi, lors de l'arrêt de la morphine, les endorphines naturelles ne suffisent plus pour activer les récepteurs comme elles le devraient. Cette accoutumance provoque des effets comportementaux comme la recherche de plus de substance pour assouvir ses besoins, ce qui est observé chez le rat[106].
L'assuétude et la résistance aux effets anti-douleur de la morphine s'observent couramment lors de son utilisation en médecine ainsi que sur des modèles animaux comme celui du rat de laboratoire par exemple lors d'expérience d'auto-administration.

La résistance à d'autres effets, comme les nausées ou la somnolence, arrivent plus rapidement et son moins bien catégorisés.
Définie comme une habituation[107] de l'organisme à la morphine, la tolérance se développe au niveau du cerveau mais surtout dans la moelle épinière et impliquerait de nombreux éléments, comme la glie (tissu de soutien, d'alimentation et de défense des neurones dans le système nerveux central), potentiellement à travers le récepteur purinergique P2X7 de type R[108], un type de récepteur notamment impliqué dans l'inflammation, la douleur chronique, la mort cellulaire et certaines maladies neurodégénératives, mais aussi à travers les récepteurs opiacés μ (mu) et δ (delta) qui interagissent également entre eux lors de l'exposition chronique à la morphine et semblent jouer un rôle important dans l'apparition de la tolérance[109]. Des récepteurs à l'inflammation comme le récepteur des glucocorticoïdes semblerait être également impliqué[110] mais aussi le récepteur TLR4 qui est impliqué dans l'immunité et l'inflammation[111].
Le mécanisme global de la tolérance à la morphine implique différentes cascades d'activation, lesquelles produisent un état global d'hyperactivité du système nerveux central, similaire à celui rencontré dans l'hyperalgésie, causé par la modification du fonctionnement de certains récepteurs aux acides aminés excitateurs[112] comme le glutamate. Ainsi, l'effet d'autres substances qui agissent sur la transmission glutaminergique (qui utilise le glutamate) pourrait en être affecté : l'effet analgésique de la kétamine (antagoniste des récepteurs NMDA du glutamate) est ainsi diminué par l'accoutumance à la morphine[113], et réciproquement, l'administration de kétamine diminuerait la tolérance à la morphine[114].
La résistance à la morphine n'impliquerait pas la glycoprotéine-P[115] mais est régulée par les PPAR (récepteur activé par les proliférateurs de peroxysomes)[116] au contraire de nombreux médicaments : c'est un mécanisme à part, complexe et multifactoriel.
D'éventuelles différences génétiques (polymorphisme) entre les récepteurs ne semblent pas être la cause de différences de sensibilité à l'accoutumance de la morphine (chez la souris)[117]. En revanche la sensibilité à la morphine varie selon les espèces de rat[118] ou de souris[119],[120] et selon les groupes ethniques chez l'homme.
Ces différences pourraient être liées à des différences dans les séquences génétiques qui codent les récepteurs aux opioïdes, ainsi que pour l'enzyme principale qui métabolise la morphine, l'UDP-Glucuronosyltransferase-2B7[121] (sujette à un polymorphisme génétique[122]).
La tolérance à la morphine serait également dépendante du sexe, avec une plus grande sensibilité chez les hommes que chez les femmes[123].
Cette accoutumance est un des critères de l'addiction qu'occasionne également la morphine. Cette addiction est en premier lieu une dépendance physique, caractérisée par l'apparition à l'arrêt de la consommation d'un syndrome de sevrage.
Syndrome de sevrage
Le syndrome de sevrage à la morphine, comme celui des autres morphiniques, est dépendant de la dose, de la durée et de nombreux facteurs[124]. Il dépend principalement du récepteur opiacé μ, particulièrement μ2[125]. Il est bien documenté car de connaissance ancienne. Il dure environ huit jours (paroxysme le 3e jour) et provoque un état de souffrance physique et psychologique extrême, malgré sa moins grande dangerosité que le sevrage à l'alcool, aux benzodiazépines ou aux barbituriques, lesquels peuvent entraîner un coma, des convulsions et la mort[126]. Il peut être précipité par l'administration de naloxone, de buprénorphine ou de naltrexone et des antagonistes opioïdes en général[127].
Impliquant essentiellement le locus cœruleus, riche en systèmes catécholaminergiques, et la substance grise périaqueducale[128], riche en récepteurs opiacés, le syndrome de sevrage passe par un état d’hyper-activation du système nerveux central, notamment à travers la libération massive de catécholamines comme la noradrénaline, l'adrénaline ou la dopamine[129], qui génèrent de l'angoisse, de l'hypertension, et contribuent à l'insomnie en activant le système nerveux sympathique[130]. Il exerce également une activité sur le système immunitaire[131] et implique l'expression de protéines G spécifiques[132].
Le système des catécholamines reste profondément modifié à la suite du sevrage à la morphine et le rôle d'autres médiateurs comme les cytokines pro-inflammatoires et la sérotonine restent discutés. Il pourrait être impliqué dans le syndrome prolongé de sevrage.
Le tableau clinique comprend[133] :
- Nausées, vomissements
- Diarrhée, souvent liquide
- Insomnie, agitation nocturne, cauchemars
- hypersialorrhée (hyper-salivation)
- angoisse, hypertension, tachycardie
- lipothymie, perte de connaissance
- Confusion, désorientation, agressivité. Il n'est pas rare que l'individu se mette spontanément en position fœtale ou que l'on observe un comportement de recherche compulsive de produit. Le syndrome de sevrage conduit l'usager à reprendre de la morphine pour en faire cesser les symptômes ; il est donc un facteur important de rechute.
La sévérité du syndrome de sevrage peut être atténuée par l'emploi de certaines substances comme les benzodiazépines (employées principalement pour réduire l'état de tension musculaire, l'insomnie et l'angoisse), la clonidine[134],[135],[136],[137] (antihypertenseur utilisé notamment dans des protocoles de sevrage sous le nom de Catapressan), mais aussi le cannabis[138], les bêta-bloquants ou des hallucinogènes comme l'ibogaïne[139]. Certaines études pointent du doigt d'autres effecteurs éventuels, comme la nitroarginine[140], le baclofène (avec différence entre les genres)[141], le vérapamil[142], les sels de lithium[143], et même la curcumine, qui aurait également un effet antinociceptif[144].
Le syndrome de sevrage peut être également soulagé par l'emploi d'antagonistes du glutamate[145].

En cas de dépendance, après l'arrêt de la consommation de morphine, la tolérance aux effets s'effondre rapidement, jusqu'à atteindre progressivement les niveaux d'avant l'addiction. Le risque d'overdose est alors maximal et la mortalité élevée : c'est une « zone » temporelle très dangereuse où l'usager est très vulnérable. Ainsi, sous la pression de nombreux facteurs comme le syndrome prolongé de sevrage ou sous la pression de l'entourage, le consommateur est susceptible d'absorber à nouveau des doses anciennement habituelles, devenues très élevées. En cas d'une addiction passée à la morphine, l'accoutumance et la dépendance ne semblent pas arriver plus vite que chez un sujet sans antécédents[146].
Il arrive que le syndrome de sevrage dure plusieurs semaines ou plusieurs mois sous une forme atténuée, essentiellement psychique : le syndrome prolongé de sevrage ou PAWS, qui implique des mécanismes encore mal connus.
Mésusage et usage détourné
Comme tout opiacé, la morphine provoque une dépendance physique et est susceptible de provoquer une dépendance psychologique dans certains contextes précis hors du contexte médical. Elle est habituellement prévenue par la mise en adéquation des doses avec le besoin, notamment à travers une évaluation régulière du symptôme douloureux, la prise à heure fixe, et par la rotation des opioïdes[147],[148]. En effet, lorsque l'on change de molécule en lui substituant un composé de profil similaire, au sein de la même classe thérapeutique (ici, les opiacés) et en respectant les équivalences, il s'agit d'une rotation. Par exemple, on peut substituer l'oxycodone à la morphine, puis l'hydromorphone à l'oxycodone, etc.
Son usage est fréquent parmi les populations de toxicomanes précaires, majoritairement dans des contextes de polyconsommation et de polytoxicomanie[149]. Elle est alors souvent obtenue illégalement et/ou broyée pour être injectée. Dans ce contexte de détournement récurrent, les associations promouvant la réduction des risques et l'accompagnement des toxicomanes en France ainsi que des addictologues demandent l'obtention d'une autorisation de mise sur le marché (AMM) de la morphine comme traitement de substitution, et l'autorisation de nouvelles galéniques particulièrement injectables dans un contexte de risque sanitaire important.
Historiquement, le sulfate de morphine a été utilisé dans un cadre de pénurie d'autres traitements de substitution, notamment avant la mise sur le marché de la buprénorphine, de manière particulière en France, à destination des individus dépendants aux opiacés, avec des résultats contrastés[60].
En effet, l'efficacité de la morphine comme traitement de substitution aux pharmacodépendances opioïdes est difficile à catégoriser, de surcroît en l'absence de données de qualité et de méthodologie fiable et non biaisée[150],[151].
Le risque de dépendance a été nettement surestimé, et a contribué à la mise au ban de la morphine au cours des années 1950 et l'abandon progressif de son emploi, avant qu'il ne soit remis à la norme à la fin du XXe siècle.
Il semblerait que la pharmacodépendance du sujet âgé ait été sous-estimé[152].
Thérapeutique
La morphine, du fait de ses effets pharmacologiques, est un antalgique puissant, mais aussi une substance fortement euphorisante. Ses indications concernent majoritairement les situations de douleur, modérées à sévères, après une évaluation de celle-ci par le soignant, et après avoir pesé le bénéfice et le risque d'un traitement par la morphine.
Des situations de traitement particulières existent : liées à l'âge (en bas âge ou chez les personnes âgées), ou liées à une altération de la fonction d'élimination (en cas de maladie hépatique ou rénale).
Indications
La mise en route d'un traitement par morphine dépend de l'indication. Elle est indiquée dans de nombreux états douloureux intenses, notamment la douleur cancéreuse. Elle est efficace dans un grand nombre de symptômes douloureux comme la douleur abdominale, la douleur de colique néphrétique, ou l'infarctus du myocarde où elle exerce en sus une action vasodilatatrice qui soulage le cœur. Concernant la douleur abdominale, la morphine fournit une analgésie sans risque d'altération de la précision diagnostique cliniquement significative[153]. Des posologies modérées de morphine en IV (4 à 6 mg) ne masquent pas les signes péritonéaux et, en diminuant l'anxiété et la souffrance, rendent souvent l'examen plus facile[154].
La morphine est aussi étudiée comme traitement dans d'autres affections.
Elle n'est en revanche pas indiquée dans la douleur neuropathique (ou elle possède une efficacité douteuse[155]), ou on lui préfère les antiépileptiques comme la prégabaline ou les benzodiazépines.
Elle est étudiée dans le traitement de l'œdème pulmonaire[156].
La morphine et les opiacés sont utilisés dans le cadre du traitement des dyspnées d'étiologies variées, d'origine cancéreuses ou non cancéreuses, notamment en soins palliatifs ou dans le cadre des soins en fin de vie[157],[158].
Elle peut exceptionnellement servir de traitement de substitution après l'échec de la buprénorphine (Subutex) et de la méthadone dans le traitement de l'héroïnomanie, même si cet usage ne correspond pas, en France, à son autorisation de mise sur le marché (AMM). Cet usage existe également en Autriche, en Suisse, en Bulgarie et en Slovénie[159].
Contre-indications[55],[160]
- Hypersensibilité à la morphine ;
- Insuffisances respiratoires décompensées, asthme, emphysème ou insuffisance cardiaque liée à une pneumopathie chronique ; car la morphine déprime la fonction respiratoire : c'est là un de ces plus marquants effets.
- Insuffisance hépatique et rénale majeure, car elle diminue la clairance de la morphine, donc son élimination et peut donc conduire à un surdosage.
- Antécédents récents de chirurgie hépatique, cholique ou biliaire ; en effet, les opiacés exercent une action spasmodique sur les sphincters.
- Insuffisance surrénalienne, hypothyroïdie ; la morphine provoque une hypotension qui peut être dangereuse dans ces cas ;
- Syndrome abdominal aigu si l'ont craint qu'elle masque un diagnostic utile ;
- Femme enceinte ou allaitante, sauf nécessité ; la plupart des opioïdes passant dans le lait maternel, le bébé pourrait présenter des signes d'origine toxique ;
- Diverticulose sigmoïdienne (car risque rupture des diverticules par la production de spasmes) ;
- Traumatismes crâniens ; le risque d'hypertension intracrânienne est particulièrement dangereux dans cette situation, et les effets secondaires de la morphine (vomissements, myosis, hypotension) peuvent masquer des signes importants pour le diagnostic ;
- Troubles convulsifs, alcoolisme aigu, delirium tremens consécutif au sevrage alcoolique.
Des antécédents de toxicomanie ne contrindiquent pas le traitement par la morphine si celui-ci est nécessaire.
Situations particulières
Le traitement d'un enfant par la morphine est une situation particulière en raison d’un métabolisme encore immature. De plus, le traitement est peu étudié chez l'enfant. Il semble toutefois qu'une prise par voie rectale est efficace, notamment en gels[161].
Bien que le flux sanguin et l'activité enzymatique soit affectés par l'âge, le métabolisme par glucurono-conjugaison l'est moins. [réf. nécessaire]
En revanche, au cours du vieillissement, la fonction rénale suit une diminution progressive. Le flux sanguin rénal, la filtration glomérulaire, la sécrétion tubulaire, et la réabsorption tubulaire diminuent, ce qui impose une adaptation de la posologie (les doses peuvent par exemple être diminuées). Ce déclin peut être majoré par les maladies cardiovasculaires, le diabète et l'hypertension artérielle. La clairance de la créatinine ou le débit de filtration glomérulaire est un bon indicateur de cette fonction rénale, contrairement à la créatininémie, soumise à une importante variabilité. [réf. nécessaire]
La maladie rénale chronique (MRC), caractérisée par de multiples dysfonctions, représente par exemple une contre-indication relative au traitement à la morphine, car elle est éliminée sous forme de M6G — un métabolite actif — par le rein. Ce métabolite peut donc s'accumuler en cas de MRC et provoquer des surdosages.
Titration
- Dans le cas du traitement d'une douleur aigüe (fracture ouverte lors d'une évacuation vers les centres de soins, réduction de luxation très douloureuse comme la hanche ou l'épaule), on réalise une titration de la dose de morphine. On commence par diluer l'ampoule de 10 mg dans une seringue de 10 ml de sérum physiologique puis on réalise une première injection dont la dose est précisément 0,1 mg/kg (soit 7 mg pour une personne de 70 kg) puis on renouvelle l'injection à demi dose (soit 0,05 mg/kg) toutes les cinq minutes jusqu'à obtenir un effet analgésique suffisant. Le niveau de la douleur s'évalue au départ et par la suite grâce à des échelles visuelles ou numériques. Toute injection morphinique par voie intraveineuse doit être réalisée sous surveillance stricte du patient comprenant son état de conscience, sa fréquence ventilatoire et si possible sous monitorage de la tension, de la fréquence cardiaque et de la saturation artériolaire en oxygène étant donné le risque de dépression respiratoire.
- Dans le cas de douleurs chroniques, la mise en route du traitement par morphine vient en remplacement d'un autre traitement antalgique. On estime que la dose de départ correspond à environ 1 mg/kg et par jour, c’est-à-dire que pour un adulte de 60 kg, la dose initiale débutera à 60 mg/j sous forme orale, 30 mg/j en injection sous-cutanée, etc. Le titrage s'effectue progressivement en fonction de la réponse antalgique ressentie par le patient. Les doses sont augmentées régulièrement par palier de 60 mg quotidiens. Après trois jours à une dose (par exemple 60 mg/j p.o.), si la réponse antalgique est insuffisante, la dose est augmentée de 60 mg pour les trois jours suivant et ainsi de suite jusqu'à la satisfaction du patient. Il est à noter qu'il n'y a pas de dose plafond (limite) pour l'administration de la morphine, ce sont les effets indésirables qui en limitent l'usage. Un patient très endolori peut commencer à une dose de 20 mg aux quatre heures pour finir avec une dose de 80 mg aux quatre heures. À cause du phénomène de tolérance (le corps s'habitue au médicament et celui-ci est moins efficace), la dose doit être augmentée régulièrement et cela même si la douleur n'a pas augmenté.
Chimie
La morphine est un alcaloïde de masse moléculaire 285 daltons.
De formule brute C17H19NO3, c'est une molécule complexe et structurée dans l'espace, en effet, elle possède cinq carbones asymétriques en position 4, 4a, 7, 7a et 12. Elle possède donc théoriquement trente-deux stéréoisomères différents.
En pratique, seul l'isomère (-) est actif, tandis que l'isomère (+) est dénué de toute activité, principalement parce que son carbone 4 est S.
La proximité de structure avec les endorphines comme la met-enképhaline est flagrante, et repose essentiellement sur le groupe hyroxy en 3 et l'oxygène qui substitue les carbones 4 et 5.

Elle se présente sous la forme d'un mélange d'isomères, poudre blanche cristalline et alcaloïde, qui fond à 255 °C, faiblement soluble dans l'eau froide (149 mg/L) mais plus soluble dans l'eau bouillante et facilement soluble dans les alcools comme l'éthanol ou le méthanol[162].
- La structure 2D de la morphine, numérotée et lettrée.
- La structure dans l'espace de la morphine.
- Vue 3D de la molécule de morphine.
Biosynthèse
La morphine est biosynthétisée dans la capsule du pavot, à partir de la Tyrosine, un acide aminé[163].

Extraction et synthèse
Industriellement la morphine peut être obtenue de deux façons :
- à partir de pavot Œillette : on utilise la capsule égrenée et l'extrémité de la tige du pavot Œillette (Papaver somniferum nigrum) récolté « vert » pendant l'été. En France, la plante est cultivée essentiellement en Champagne-Ardenne. Les parties de la plante sont séchées, puis la morphine est extraite en milieu hydro-alcoolique avec d'autres opiacés. Elle sera séparée par une précipitation sélective avant d'être purifiée ;
- à partir de l'opium : l'opium est issu de pavots (Papaver somniferum), cultivés en Inde, par évaporation du latex qui s'écoule d'incisions faites sur la capsule. La morphine (et d'autres alcaloïdes) est obtenue par extraction aqueuse acide depuis l'opium qui en contient à peu près 10 %. Elle est ensuite obtenue seule par une précipitation sélective.
La synthèse totale de la morphine a été proposée par Robert Robinson en 1925, récipiendaire du prix Nobel de chimie 1947, et réalisée pour la première fois par Marshall D. Gates Jr. (en) en 1952, en 31 étapes, avec un rendement très faible (0,06 %). C'est un exemple de réaction de Diels-Alder.
D'autres synthèses ont depuis été réalisées par de nombreuses équipes comme celles de Evans[164] ou Fuchs[165].
- La synthèse de Gates.
- La synthèse de Rice et Keller, qui reproduit en partie la synthèse naturelle de la morphine du pavot.
Sels
La morphine est souvent utilisée sous forme de sel afin de faciliter son utilisation et son absorption par l'organisme dans les formes non injectables.
Il existe deux sels, sulfate et chlorhydrate de morphine, qui une fois dans le corps seront sous forme de morphine base.
Le sulfate de morphine est obtenu par réaction de la morphine en solution hydro-alcoolique (eau + éthanol) avec de l'acide sulfurique dilué. Une réaction similaire dans l'acide chlorhydrique est utilisée pour l'obtention du chlorhydrate de morphine.
Le sulfate a la particularité d'être un pentahydrate incluant deux molécules de morphine.
| DCI | Sulfate de morphine | Chlorhydrate de morphine |
| Nom IUPAC | sulfate de di(7,8-didéshydro-4,5α-époxy-17-méthylmorphinane-3,6α-diol) pentahydraté | chlorhydrate de 7,8-didéshydro-4,5α-époxy-17-méthylmorphinane-3,6α-diol trihydraté |
| Formule brute | C34H40N2O10S, 5H2O | C17H20ClNO3, 3H2O |
| Numéro CAS | ||
| Masse molaire | 759 g/mol | 375,8 g/mol |
| Aspect | poudre cristalline blanche | poudre cristalline blanche ou aiguilles incolores, ou masses cubiques |
| Solubilité | soluble dans l’eau, très peu soluble dans l’éthanol, pratiquement insoluble dans le toluène | soluble dans l’eau, très peu soluble dans l’éthanol, pratiquement insoluble dans le toluène |
Source : Pharmacopée européenne 5.5, EDQM, 12/2005 ; The Merck index, 13e éd.
Impuretés
De par la complexité de la composition de l'opium et de la ressemblance des produits qui le composent, on retrouve systématiquement certains autres alcaloïdes dans la morphine que l'on considère comme des impuretés. Leur teneur dans la morphine est limitée à 1 % (0,2 % pour chaque impureté et 0,4 % pour la pseudomorphine)[166] :
- codéine (impureté A de la pharmacopée européenne) ;
- pseudomorphine (impureté B de la pharmacopée européenne) ;
- oripavine (impureté C de la pharmacopée européenne) ;
- 10R-hydroxymorphine (impureté D de la pharmacopée européenne) ;
- morphinone (impureté E de la pharmacopée européenne) ;
- thébaïne ;
- N-oxyde de morphine (en) ;
- apomorphine.
Législation
La morphine est inscrite au Tableau I de la convention unique sur les stupéfiants de 1961 et son usage est réglementé dans de nombreux pays[167].
En Belgique, au Canada et en France, la morphine et ses sels sont des stupéfiants. De ce fait, la morphine est soumise à la réglementation du médicament stupéfiant, avec des règles particulières pour la prescription (ordonnance particulière limitée dans le temps — vingt-huit jours en France), la délivrance (le pharmacien doit la noter sur un cahier spécial), l'usage (uniquement pour le malade) et la détention (considéré comme une drogue).
Comme tout narcotique, la morphine est une substance dopante et, dans certains pays, il est interdit aux sportifs participant aux compétitions d'en utiliser[réf. nécessaire].
Sociologie
Perception
La perception de la morphine, souvent négative, peut mener à des défauts de soin, en générant par exemple une certaine peur. Les patients peuvent considérer qu'il s'agit d'un « dernier recours » ou qu'il serait réservé à la fin de vie[168].
Cette vision a subi depuis la fin des années 1990 une profonde mutation, issue des plans publics de lutte contre la douleur. La consommation de morphine a par exemple triplé entre 1999 et 2001 à l'Assistance publique - Hôpitaux de Paris (AP/HP)[169].
Des difficultés dans la prise en charge de la douleur persistent, du fait notamment des mentalités et des comportements. Une enquête réalisée par l’AP/HP montre que 50 % à 55 % des malades présents un jour donné ont souffert d’une douleur intense au cours des dernières 24 heures et seulement 1/3 de ces patients a connu un réel soulagement[169].
L'évaluation de la douleur étant parfois subjective et souvent mal réalisée, les prescriptions sont souvent insuffisantes.
Stéréotypes
La morphine et son usage en thérapeutique nourrit de nombreux stéréotypes, même parmi le personnel soignant[170], ce qui conduisit à une moins bonne prise en charge de la douleur.
En effet, il n'existe pas de preuves scientifiques pour dire que la morphine adéquatement utilisée administrée en fin de vie accélère la mort[171] et le risque de dépendance reste marginal lors d'une utilisation thérapeutique.
La morphine dans la culture
On a vu que les artistes sont en bonne place parmi les morphinomanes. Certains, drogués ou non, en ont fait un thème parfois récurrent de leur production.
Dans la littérature

Couverture illustrée par Manuel Orazi.
À la fin du XIXe siècle, la morphine est une véritable mode littéraire.
Charles Baudelaire publie en 1869 Les Paradis artificiels, mais à dire vrai il n’y cite que l’opium en général, à côté du hachich.
Jules Verne, certes plus connu pour des voyages moins artificiels, dédie en 1886 un sonnet À la morphine, qu’il conclut ainsi :
« Ah ! Perce-moi cent fois de ton aiguille fine
Et je te bénirai cent fois, Sainte Morphine,
Dont Esculape eut fait une divinité. »
De nombreux livres dont la morphine est un personnage central sont publiés à cette époque[172] :
- La Comtesse Morphine, de Marcel Mallat (1885) ;
- Morphine, de Claude Farrère (1889) ;
- Les Possédés de la morphine, de Maurice Talmeyer (1892) ;
- Le Royaume de l’oubli, de Daniel Borys (1909)…
Certains ne s’en remettront pas : le poète symboliste Édouard Dubus s’effondre à 31 ans dans la rue en 1895, seringue en poche. Son confrère Stanislas de Guaita, qui préconise « l’hygiène morphique » en meurt lui aussi en 1897, à 36 ans[172].
En 1927, l'écrivain et médecin russe Mikhaïl Boulgakov s'inspire de son expérience personnelle pendant la Première Guerre mondiale lors de son retrait du front en 1917 et publie la longue nouvelle Morphine, dans laquelle le médecin Poliakov sombre dans la morphine. Boulgakov défend alors le mérite pour un médecin de tester sur lui-même certains médicaments. Le réalisme clinique est inédit, et d'un dénouement tragique, le suicide[45]. Il y décrit minutieusement les conséquences des injections qui détruisent sa mémoire, le plonge dans la mélancolie, provoque des hallucinations morbides, etc. dans un témoignage « poignant » [46],[47],[48].
Jean Cocteau, qui subit une cure de désintoxication en 1928, la suit son journal, qu’il publiera, Opium : Journal d'une désintoxication (1930)[172].
Dans la peinture


La mode de la fin du XIXe siècle transparaît également dans la peinture :
Albert Besnard livre en 1887 le portrait de Deux femmes dépendantes de la morphine (voir ci-dessus : Accoutumance).
Peu après, Georges Moreau de Tours travaille sur le même thème : Les Morphinées ou Les Toxicomanes de la morphine[173].
Le peintre et écrivain catalan Santiago Rusiñol, hospitalisé à Barcelone en 1900 pour soigner sa dépendance, peint deux œuvres célèbres : La Morphine en 1894, et Avant la morphine à la même époque.
Ernst Ludwig Kirchner, plasticien expressionniste, prend comme beaucoup d’autres de la morphine pour raison médicale. Il en tire un tableau torturé, Autoportrait sous morphine (1917).
Plus récemment (2016), Andrew Littell donne une vision saisissante du sevrage avec Sevrage chimique soudain et involontaire (voir ci-dessus : Syndrome de sevrage)[174].
Formes pharmaceutiques
La morphine existe sous différentes formes galéniques selon l'indication et le patient :
- voie parentérale
- injection intraveineuse,
- injection sous-cutanée,
- injection intraveineuse en perfusion,
- injection péridurale,
- injection intrathécale,
- les pompes à morphine sont de plus en plus utilisées en soins post-opératoires ou en soins palliatifs ; analgésie contrôlée par le patient ;
- voie orale
- comprimé ou gélule,
- comprimé ou gélule à libération prolongée (LP) : utilisés dans le traitement des douleurs chroniques. Il existe des versions en gélule à deux prises par jour (BID) et plus récemment des versions à une prise par jour (OAD, de l'anglais : Once a day)[175]. Dans les deux cas, le comprimé ou la gélule ou son contenu a subi un traitement afin d'obtenir une libération étalée dans le temps,
- sirop,
- solution buvable, notamment en gouttes
- autres voies
- suppositoire (non disponible seule en France, disponible en Suisse et au Canada), notamment au sein de préparations contenant de l'opium, du paracétamol ou de la caféine.
La dose requise dépend de la voie d'administration, la morphine par voie orale subissant un premier passage hépatique, seulement 30 % de la dose ingérée sont utilisés par le corps. Il existe donc des tableaux d'équivalence (pour l'adulte) :
| Voie orale | Sous-cutanée | Intraveineuse | Péridurale | Intrathécale |
| 1 mg kg−1 j−1 | 0,5 mg kg−1 j−1 | 0,3 mg kg−1 j−1 | 0,1 à 0,05 mg kg−1 j−1 | 0,02 à 0,005 mg kg−1 j−1 |
Termes apparentés
- Morphinomanie : terme composé de morphine et de manie, du grec mania pour « folie, passion ». Il désigne une consommation régulière et non contrôlée de morphine, amenant un état de dépendance.
- Morphinomane : désigne la personne atteinte de morphinomanie.
Divers
La morphine fait partie de la liste modèle des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en avril 2013)[176].
Notes et références
Voir aussi
Articles connexes
Liens externes
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :











