Ródium(II)-acetát
| ródium(II)-acetát | |||
 ródium(II)-acetát 3D modellje | |||
 ródium(II)-acetát minta | |||
| IUPAC-név | ródium(II)-acetát | ||
| Más nevek | diródium-tetraacetát ródium-diacetát dimer | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 15956-28-2 | ||
| ChemSpider | 20370 | ||
| EINECS-szám | 240-084-8 | ||
| RTECS szám | VI9361000 | ||
| |||
| |||
| InChIKey | ITDJKCJYYAQMRO-UHFFFAOYSA-L | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C8H12O8Rh2 | ||
| Moláris tömeg | 441,99 g/mol | ||
| Megjelenés | smaragdzöld por | ||
| Sűrűség | 1,126 g/cm3 | ||
| Olvadáspont | >100 °C | ||
| Forráspont | elbomlik | ||
| Oldhatóság (vízben) | oldható | ||
| Oldhatóság (más oldószerek) | szerves poláris oldószerek | ||
| Kristályszerkezet | |||
| Kristályszerkezet | monoklin | ||
| Koordinációs geometria | oktaéderes | ||
| Dipólusmomentum | 0 D | ||
| Veszélyek | |||
| MSDS | Coleparmer MSDS | ||
| Lenyelés veszélye | idegrendszeri- és szívproblémákat okozhat | ||
| Belégzés veszélye | légzési irritációt okoz | ||
| Szembe kerülés veszélye | szemirritációt okoz | ||
| Bőr-kontaktus veszélye | bőrirritációt okoz | ||
| NFPA 704 | |||
| R mondatok | 36/38 | ||
| S mondatok | 15, 26, 28A, 37/39 | ||
| Lobbanáspont | kis lobbanékonyság | ||
| Rokon vegyületek | |||
| Rokon vegyületek | réz(II)-acetát króm(II)-acetát | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A ródium(II)-acetát a Rh2(CH3CO2)4 kémiai képlettel rendelkező vegyület. Ez a sötétzöld por poláris oldószerekben, mint a vízben, gyengén oldódik. Katalizátorként alkalmazzák alkének ciklopropanálásához.
Előállítása
A ródium(II)-acetátot leggyakrabban hidratált ródium(III)-klorid ecetsavban (CH3COOH) való hevítésével állítják elő.[1]
Felépítése
A ródium(II)-acetátban egy pár ródiumatom van, amelyek egy-egy vízmolekulához, négy, az acetátcsoportokhoz tartozó oxigénhez, valamint egymáshoz kapcsolódnak, egy 239 pm hosszúságú Rh−Rh kötéssel. A víz adduktum kicserélhető, és számos Lewis-bázis kapcsolódhat a helyekre.[2] A réz(II)-acetát és a króm(II)-acetát vegyületek hasonló szerkezettel rendelkeznek.
Reakciók
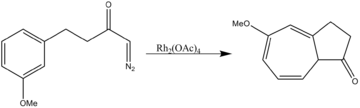
A diródium-tetraacetát számos reakcióban alkalmazható, kötésekbe való beillesztésnél, vagy alkének[3] és aromás vegyületek[4] ciklopropanálásakor. Szelektíven köti a ribonukleozidokat (a dezoxiribonukleozidokkal szemben) úgy, hogy a 2-es és 3-as −OH csoportjuknál kötődik hozzájuk.[5] A ródium(II)-acetát dimer, a réz(II)-acetáthoz hasonlítva reakcióképesebb és alkalmasabb a ribonukleozidok és dezoxiribonukleozidok megkülönböztetésére, mert oldható vízben, míg a réz(II)-acetát nem.
Kiválasztott katalitikus reakciók
A diródium-tetraacetátot használják még katalizátorként C−H, N−H, S−H és O−H kötésekbe való beillesztéshez.
Jegyzetek
Fordítás
Ez a szócikk részben vagy egészben a Rhodium(II) acetate című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.