シトクロムb6f複合体
シトクロムb6f複合体(英: cytochrome b6f complex、略称: Cyt b6f)またはプラストキノール-プラストシアニンレダクターゼ(プラストキノール-プラストシアニンオキシドレダクターゼ、英: plastoquinol/plastocyanin reductase or plastoquinol/plastocyanin oxidoreductase、EC 7.1.1.6)は植物の葉緑体、シアノバクテリア、緑藻のチラコイド膜に存在する酵素であり、プラストキノールからプラストシアニンへの電子伝達、すなわち次の反応を触媒する。
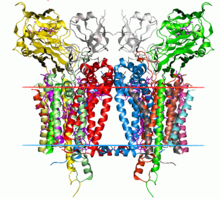
| Cytochrome b6f complex | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| 識別子 | |||||||||
| 略号 | B6F | ||||||||
| Pfam | PF05115 | ||||||||
| InterPro | IPR007802 | ||||||||
| TCDB | 3.D.3 | ||||||||
| OPM superfamily | 92 | ||||||||
| OPM protein | 4pv1 | ||||||||
| Membranome | 258 | ||||||||
| |||||||||
| Cytochrome b6f complex | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 識別子 | |||||||||
| EC番号 | 7.1.1.6 | ||||||||
| CAS登録番号 | 79079-13-3 | ||||||||
| 別名 | Plastoquinol/plastocyanin reductase | ||||||||
| データベース | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB構造 | RCSB PDB PDBj PDBe PDBsum | ||||||||
| |||||||||
この反応は、ミトコンドリアの電子伝達系においてシトクロムbc1複合体(複合体III)によって触媒される反応と類似している。光合成反応において、シトクロムb6f複合体は光化学系IIから光化学系Iへの電子伝達を媒介する段階の1つとなっており、またそれと同時にチラコイド内腔へプロトンをくみ出し、電気化学的勾配(エネルギー勾配)の形成に寄与している[2]。この勾配は後にADPからATPを合成する過程で利用される。
構造
シトクロムb6f複合体は二量体であり、各単量体は8つのサブユニットから構成される[3]。c型シトクロムであるシトクロムf(32 kDa)、低電位と高電位の2分子のヘムを結合するシトクロムb6(25 kDa)、[2Fe-2S]型鉄硫黄クラスターを有するリスケタンパク質(19 kDa)、そしてサブユニットIV(17 kDa)という4つの大きなサブユニットに加えて、PetG、PetL、PetM、PetNという4つの小さなサブユニット(3-4 kDa)が含まれる[3][4]。二量体全体では、217 kDaの大きさになる。
シトクロムb6f複合体の結晶構造は、クラミドモナスChlamydomonas reinhardtii、イデユアイミドリMastigocladus laminosus、シアノバクテリアNostoc sp. PCC 7120由来のものが決定されている[2][5][6][7][8][9]。
シトクロムb6f複合体のコア構造はシトクロムbc1複合体のコアと類似している。シトクロムb6とサブユニットIVはシトクロムbと相同であり[10]、両複合体のリスケ鉄硫黄タンパク質も相同である[11]。一方、シトクロムfとシトクロムc1は相同ではない[12]。
シトクロムb6f複合体には7つの補欠分子族が含まれている[13][14]。そのうち4つはシトクロムb6f複合体とシトクロムbc1複合体で共通しており、ヘムcがシトクロムc1とシトクロムfに、2つのヘムbがシトクロムbとシトクロムb6に、[2Fe-2S]クラスターがリスケタンパク質に含まれている。シトクロムb6f複合体に固有の3つの補欠分子族は、クロロフィルa、β-カロテン、ヘムcn(ヘムx)である[5]。
シトクロムb6f複合体のコア内部の各単量体間の空間は脂質で埋まっており、タンパク質内の誘電環境を調節することでヘム-ヘム間の電子伝達に方向性をもたらしている[15]。
生物学的機能

光合成においてシトクロムb6f複合体は、2つの光合成反応中心複合体である光化学系IIと光化学系Iの間の電子とエネルギーの伝達を媒介する機能を果たす。この過程で、葉緑体のストロマから内腔へプロトンがチラコイド膜を越えて輸送される[2]。シトクロムb6f複合体を介した電子伝達はプロトン勾配の形成を担い、葉緑体でのATP合成を駆動する[4]。

還元型フェレドキシンからNADP+への電子伝達ができない場合、シトクロムb6f複合体は循環的光リン酸化(cyclic photophosphorylation)に中心的役割を果たす[16]。このサイクルはP700+のエネルギーによって駆動され、ATP合成を駆動するプロトン勾配の形成に寄与する。このサイクルは光合成に必要不可欠であることが示されており[17]、炭素固定のための適切なATP/NADPH生成比の維持を補助している[18][19]。
シトクロムb6f複合体内のpサイド(内腔側)キノール脱プロトン化-酸化反応は、活性酸素種の産生に関与していることが示唆されている[20]。キノール酸化部位に位置するクロロフィル分子は活性酸素種の形成率を高める、非光化学的な構造的機能を果たしていることが示唆されており、おそらく細胞内の酸化還元シグナル伝達と関連している[21]。
反応機構
シトクロムb6f複合体は、2つの可動性酸化還元キャリア、プラストキノール(QH2)とプラストシアニン(Pc)の間の非循環的電子伝達(1)と循環的電子伝達(2)を担う。
| H2O | → | 光化学系II | → | QH2 | → | Cyt b6f | → | Pc | → | 光化学系 I | → | NADPH | (1) |
| QH2 | → | Cyt b6f | → | Pc | → | 光化学系 I | → | Q | (2) | ||||
シトクロムb6f複合体は、QH2からPcへの電子伝達を媒介し、その間に2つのプロトンをストロマからチラコイド内腔へくみ出す。反応は次のようにまとめられる。
- QH2 + 2Pc(Cu2+) + 2H+ (stroma) → Q + 2Pc(Cu+) + 4H+ (lumen)[16]
この反応は複合体IIIと同じくQサイクルによって行われる[22]。QH2は電子キャリアとして機能し、電子分岐と呼ばれる過程で2つの電子をhigh-potential electron transport chain(ETC)とlow-potential ETCへ伝達する[23]。複合体では最大3つのQH2分子が電子伝達ネットワークを形成しており、光合成におけるQサイクルの作動、酸化還元センサー、触媒機能を担っている[24]。
Qサイクル

前半
- QH2が複合体のpサイド(内腔側)に結合する。high-potential ETCの鉄硫黄中心によってセミキノン(SQ)へと酸化され、チラコイド内腔へ2つのプロトンが放出される。
- 還元された鉄硫黄中心は、シトクロムfを介して電子をPcへ伝達する。
- Low-potential ETCでは、SQが電子をシトクロムb6のヘムbpへ伝達する。
- ヘムbpが電子をヘムbnへ伝達する。
- ヘムbnの1電子がプラストキノン(Q)を還元し、SQが形成される。
後半
- 2つ目のQH2が複合体に形成する。
- High-potential ETCでは、1電子によって他の酸化型Pcが還元される。
- Low-potential ETCでは、ヘムbnの電子がSQへ伝達され、完全に還元されたQ2−がストロマから2つのプロトンを取り込むことでQH2が形成される。
- 再生された酸化型Qと還元型QH2は膜中へ拡散する。
循環的電子伝達
複合体IIIとは異なり、シトクロムb6f複合体は循環的光リン酸化の中心となる、別の電子伝達反応も触媒する。フェレドキシン(Fd)由来の電子はプラストキノンへ伝達され、その後シトクロムb6f複合体でプラストシアニンの還元に利用される。プラストシアニンは光化学系I中のP700によって再び酸化される[25]。フェレドキシンによるプラストキノンの還元の正確な機構に関しては現在研究が行われている。提唱されている1つの機構は、フェレドキシン:プラストキノンレダクターゼもしくはNADPデヒドロゲナーゼが存在するというものである[25]。ヘムxはQサイクルには必要ではないと考えられており、また複合体IIIにも存在しない。そのため、ヘムxは以下の機構で循環的光リン酸化に利用されていると提唱されている[23][26]。
- Fd (red) + heme x (ox) → Fd (ox) + heme x (red)
- heme x (red) + Fd (red) + Q + 2H+ → heme x (ox) + Fd (ox) + QH2
出典
関連項目
外部リンク
- 1Q90 - PDB structure of cytochrome b6f complex from Chlamydomonas reinhardtii
- 1VF5 - PDB structure of cytochrome b6f complex from Mastigocladus laminosus
- Cytochrome b6f page @ Purdue University, USA
- UMich Orientation of Proteins in Membranes families/superfamily-3 - Calculated positions of b6f and related complexes in membranes
- Cytochrome b6f Complex - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)
- Plastoquinol-plastocyanin reductase - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)
