Rotavirus
Rotavirus (em latim: rota, roda, pela sua forma) é um género de vírus de RNA bicatenário da família Reoviridae. É umas das principais causas de diarreia grave em lactentes e crianças jovens, e é um dos diversos vírus que causam infeções comummente chamadas de gastroenterites. Estima-se que, aos cinco anos de idade, quase todas as crianças do mundo tenham sido infectadas por um rotavírus ao menos uma vez. No entanto, como em cada infecção a imunidade se desenvolve, as infecções subsequentes são menos graves e adultos raramente são afectados. Existem oito espécies deste tipo de vírus, conhecidas como A, B, C, D, E, F, G e H. O Rotavírus A, o mais comum, é o responsável por mais de 90% das infecções em seres humanos.
| Rotavirus | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||
| |||||||||||
| Espécie-tipo | |||||||||||
| Rotavirus A | |||||||||||
| Espécies | |||||||||||
| |||||||||||
O vírus é transmitido pela rota fecal-oral. Infecta e danifica as células que revestem o intestino delgado (enterócitos) provocando gastroenterite. O rotavírus foi descoberto em 1973 e é responsável por 50% dos internamentos hospitalares devido a diarreias agudas em crianças. Para além do seu impacto na saúde humana, os rotavírus também causam infecções em animais, inclusive no gado.
Causam gastroenterites limitadas com diarreia, vómitos, muita dor abdominal e náuseas, após transmissão em comida, objectos ou água infectada com vírus proveniente de fezes. É a causa mais comum de diarreia infecciosa nas crianças da Europa.
A infecção de rotavírus é geralmente uma doença fácil de controlar na infância, no entanto, ainda assim, a cada ano em todo o mundo morrem cerca de 450 mil crianças com idades inferiores a cinco anos infectadas, a maioria das quais vive em países em vias de desenvolvimento económico, e quase dois milhões ficam gravemente doentes. O tratamento é feito pela administração de muita água com um pouco de sal e açúcar (soro caseiro), para restabelecer os líquidos e electrólitos perdidos na diarreia. As campanhas de higiene para combater os rotavírus centram-se na terapia de reidratação oral para crianças infectadas e na vacinação contra rotavírus. A incidência e gravidade das infecções do rotavírus baixaram significativamente nos países que incluíram a vacinação contra os rotavírus às suas normas rotineiras de imunização das crianças.
Sintomatologia
A gastroenterite produzida pelo rotavírus é uma doença que pode ser tanto leve como grave, caracterizada por vómitos, diarreia aquosa e febre baixa. Afecta sobretudo as crianças. Uma vez que uma criança é infectada pelo vírus, existe um período de incubação de aproximadamente dois dias antes de aparecerem os sintomas.[1] Estes geralmente começam com vómitos seguidos por quatro a oito dias de diarreia abundante. A desidratação é mais comum em infecções de rotavírus do que na maioria daquelas causadas por patógenos bacterianos, e é a causa mais comum das mortes relacionadas à infecção do rotavírus.[2]
As infecções de rotavírus A podem ocorrer durante toda a vida: a primeira vez geralmente constitui sintomas, mas as sucessivas possíveis infecções são normalmente leves ou assintomáticas,[3][4] uma vez que o sistema imunitário providencia alguma proteção contra o vírus.[5][6] Consequentemente, as infecções sintomáticas são mais frequentes em crianças com idades inferiores a dois anos e decresce progressivamente até aos 45 anos.[7] A infecção nas crianças recém-nascidas é comum, mas geralmente está associada a doença assintomática ou leve;[8] a maioria dos sintomas graves tendem a ocorrer em crianças entre os seis meses e os dois anos de idade, ou entre idosos e pessoas imunodeprimidas. Devido à imunidade adquirida durante a infância, a maioria dos adultos não está susceptível ao rotavírus; e as gastroenterites que surgem em adultos geralmente apresentam outros agentes diferentes do rotavírus, no entanto infeções assintomáticas nos adultos podem preservar a transmissão da infeção na comunidade.[9]
Transmissão
O rotavírus é transmitido pela rota fecal-oral, através do contacto com mãos contaminadas, superfícies, objectos[10] e possivelmente por via respiratória.[11] As fezes de uma pessoa infectada podem conter mais de 10 biliões de partículas infecciosas por grama,[3] e são tão-somente necessárias menos de cem partículas para transmitir a infecção a outra pessoa.[8]
Os rotavírus são estáveis no meio ambiente e foram encontrados em amostras em estuários a níveis tão elevados como 1-5 partículas infecciosas por galão americano (3,78 litros); o vírus permanece infeccioso entre 9 e 19 dias.[12] As medidas sanitárias adequadas para a eliminação de bacterias e parasitas parecem ser ineficazes no controle do rotavírus, uma vez que a incidência de infeções em países com altos padrões de saúde é similar à dos países de nível inferior.[11]
Mecanismos da infecção

A diarreia é causada por diversas actividades dos vírus. A má-absorção deve-se à destruição das células do epitélio intestinal denominadas enterócitos. A proteína tóxica NSP4 do rotavírus induz uma secreção de cloreto dependente do ião cálcio e da idade, que interrompe o transportador SGLT1, o qual intervém na reabsorção de água, reduzindo aparentemente a actividade das dissacaridases e, possivelmente, activa os reflexos secretores dependentes do ião cálcio do sistema nervoso entérico.[13] Os enterócitos intactos segregam lactase no intestino delgado; a intolerância à lactose do leite causada por uma deficiência de lactase é um sintoma da infecção de rotavirus,[14] que pode persistir durante semanas.[15] Muitas vezes a diarreia reaparece quando se reintroduz o leite na dieta da criança, devido à fermentação bacteriana do açúcar dissacárido lactose no intestino.[16]
Diagnóstico e detecção
O diagnóstico das infeções do rotavírus normalmente é feito depois que se diagnostica gastroenterite como causa duma diarreia grave. À maioria das crianças internadas nos hospitais com gastroenterite é-lhes feito um exame para detecção do rotavírus A.[17][18] O diagnóstico específico da infecção do rotavírus A é realizado examinando as fezes das crianças por meio de um ensaio de imunoabsorção enzimática. Os testes são sensíveis e específicos e detectam todos os serotipos do rotavírus A.[19] Em laboratórios de investigação podem ser utilizados outros métodos, como a microscopia electrónica e a PCR.[20] A PCR com reversotranscrição (RT-PCR) pode detectar e identificar todas as espécies e serotipos de rotavírus nos humanos.[21]
Tratamento e prognóstico
O tratamento das infeções agudas de rotavírus não é específico e implica o tratamento dos sintomas e, o mais importante, a manutenção da hidratação.[22] Se não forem tratadas, as crianças podem morrer duma grave desidratação dela resultante.[23] Dependendo da gravidade da diarreia, o tratamento consiste numa terapia de reidratação oral, durante a qual é dada à criança água extra para beber que contém pequenas quantidades de sais e açúcares.[24] Em 2004, a OMS e a UNICEF recomendaram o uso de soluções de reidratação oral de baixa osmolaridade e suplementos de zinco para tratamento em duas fases da diarreia aguda.[25] Algumas infeções são graves o bastante que justificam hospitalização, durante a qual se administram fluídos por via intravenosa ou por tubo nasogástrico, e podem ser monitorizados os níveis de electrólitos e glicemia da criança.[17] As infeções de rotavírus raramente causam outras complicações, e se a criança receber o tratamento adequado o prognóstico é positivo.[26]
Epidemiologia

O rotavírus A é responsável por mais de 90% das gastroenterites por rotavírus nos humanos,[27] e é endémico em todo o mundo. A cada ano os rotavírus provocam milhões de casos de diarreia nos países em vias de desenvolvimento, quase 2 milhões necessitam de hospitalização e estima-se que haja 453 mil mortes de crianças menores de cinco anos devido a esta doença,[28][29] 85% das quais vivem em países não desenvolvidos.[30][31][32] O importante papel do rotavírus enquanto causador de diarreias não é suficientemente reconhecido pela comunidade sanitária em todo o mundo,[33] especialmente nos países em vias de desenvolvimento.[28] É possível afirmar que praticamente todas as crianças foram infectadas pelo rotavírus antes dos 5 anos.[34] Entre as crianças pequenas é a principal causa de diarreia grave, e é responsável por aproximadamente 20% dos casos e por 50% das hospitalizações nesta faixa etária.[28] Os rotavírus causam 37% das mortes atribuídas a todos os tipos de diarreia e 5% de todas as mortes infantis em crianças com idades inferiores a 5 anos.[29][35][36] As infeções por rotavírus dão-se principalmente durante os meses frios e secos.[37][38] Desconhece-se o número de casos em que se pode atribuir a comida contaminada.[39] Noutra estimativa feita pela UNICEF e OMS é indicado o seguinte: "Estima-se que o rotavírus causa 40% de todos os ingressos hospitalares devido a diarreias entre os crianças abaixo dos 5 anos de idade em todo o mundo, dando origem a 100 milhões de episódios de diarreia aguda todos os anos, que têm como resultado a morte de entre 350.000 e 600.000 crianças".[40]
Os surtos de diarreia provocada por rotavírus A são comuns entre as crianças pequenas hospitalizadas, as crianças maiores que frequentam creches e idosos em residências da terceira idade.[41][42] Em 2005 o maior registo de epidemia de diarreia por rotavírus ocorreu em Nicarágua, associada a mutações no genoma do rotavírus A, que possivelmente fizeram com que o vírus evitasse a imunidade prevalente da população.[43][44]
O rotavírus B, também chamado rotavírus da diarreia nos adultos ou ADRV, causou grandes epidemias na China que afectaram milhares de pessoas de todas as idades. Essas epidemias ocorreram como resultado da contaminação de águas potáveis com águas residuais.[45][46] Também houve infeções de rotavírus B na Índia em 1998 por uma cepa chamada CAL, que, diferentemente do ADRV, é endémica.[47][48] Até agora, as epidemias causadas pelo rotavírus B estão confinadas fundamentalmente à China.[49]
O rotavírus C foi associado a casos raros e esporádicos de diarreia em crianças, podendo afectar a toda a família.[50]
Prevenção

Como a melhoria das medidas higiénicas não diminui a prevalência das doenças retrovirais, e a frequência de hospitalizações se mantém alta apesar do uso de terapia de reidratação oral, a principal intervenção sanitária que se pode aplicar é a vacina contra rotavírus.[51] Foram elaboradas duas vacinas contra as infeções de rotavírus A que são seguras e efectivas em crianças:[52] Rotarix da GlaxoSmithKline[53] e RotaTeq da Merck, com estruturas e esquemas posológicos diferentes.[54] Ambas são administradas por via oral e contêm vírus atenuados vivos.[52] Estas vacinas foram estudadas de uma forma extensa, incluindo países europeus, antes do seu lançamento, evidenciando um bom perfil de eficácia e segurança. Em 2009, a OMS recomendou que se incluísse uma vacina contra os rotavírus em todos os programas nacionais de imunização.[55] A incidência e gravidade das infeções por rotavírus diminuiu significativamente nos países que aplicaram esta recomendação.[56][52] Por exemplo, no México, que em 2006 estava entre os primeiros países do mundo em que a vacinação contra o rotavírus foi introduzida, as taxas de doenças diarreicas caíram durante o episódio de rotavírus de 2009 em mais do 65% entre as crianças com idades inferiores 2 anos.[57] Em Nicarágua, que em 2006 se converteu no primeiro país em vias de desenvolvimento a introduzir a vacina do rotavírus, as infeções graves de rotavírus foram reduzidas em 40% e o ingresso nos cuidados intensivos para metade.[58] Nos Estados Unidos a vacinação contra os rotavírus desde 2006 tem reduzido as hospitalizações relacionadas com o rotavírus em 86%. As vacinas puderam também contribuir para a prevenção da doença em crianças não vacinadas ao limitar o número de infeções circulantes.[59]
Existem licenças de vacinas contra o rotavírus em mais de 100 países, mas apenas 28 países introduziram nos seus planos de vacinação rotineiros a vacinação contra o rotavírus.[60][61][62][63] Os ensaios sobre a segurança e eficácia das vacinas Rotarix e RotaTeq na África e Ásia concluíram que as vacinas reduziam drasticamente as diarreias graves entre crianças nos países em vias de desenvolvimento, nos quais ocorria a maioria das mortes por rotavírus.[64] Em 2012 a revisão Cochrane de 41 ensaios clínicos. em que participaram 186.263 pessoas, concluiu que o Rotarix e o RotaTeq são vacinas efectivas.[65] Estão a ser desenvolvidas outras vacinas contra os rotavírus.[66] A partir de setembro de 2013, a vacina foi oferecida a todas as crianças no Reino Unido entre os dois e três meses de idade.[67] No estado espanhol a vacinação por rotavírus não constitui parte do programa geral de vacinação nem está financiada pela saúde pública, mas é recomendada pelo Comité Assessor de Vacinas da Associação Espanhola de Pediatria e pela Sociedade Europeia de Gastroenterologia,[68] Hepatologia e Nutrição Pediátrica (ESPGHAN) e pela Sociedade Europeia de Infetologia Pediátrica (ESPID) e Organização Mundial da Saúde (OMS). Em Portugal, as vacinas contra o rotavírus são comercializadas desde 2006. Os estudos realizados noutros países demonstram que os benefícios da vacinação compensam os custos, mas até que a relação custo-eficácia em Portugal seja apurada, a SPP não tem base para defender a inclusão no Plano Nacional de Saúde.
As recomendações americanas do Advisory Committee on Immunization Practices (ACIP) de 2009 referem que a administração não deve ser feita no hospital pelo risco de transmissão do vírus vacinal.[69] As recomendações europeias de 2015 da European Society for Paediatric Infectious Diseases (ESPID)[70] defendem a sua utilização nos ainda hospitalizados, reforçando que nestas circunstâncias deverão ser rigorosamente cumpridas as medidas para evitar transmissão a grupos de risco. Uma publicação de 2014 sobre segurança da utilização da vacina contra o rotavírus numa unidade de cuidados intensivos neonatais americana concluiu que a vacina era bem tolerada e com baixo risco de transmissão sintomática aos não vacinados.[71]
Apesar das limitações dos estudos pelo pequeno número de doentes incluídos, os resultados sugerem que as crianças infetadas por VIH têm uma resposta a esta vacina comparável às crianças VIH negativas, sendo ambas bem toleradas.[72][73]
A organização não governamental PATH, a OMS, os Centers for Disease Control and Prevention dos EEUU e a GAVI Alliance estão a trabalhar para levar as vacinas de rotavírus aos países em vias de desenvolvimento, onde se origina a maioria dos casos e mortes em crianças.[74]
Infecção noutros animais
Os rotavirus infetam crias de muitas espécies de animais e são uma das principais causas de diarreia nos animais selvagens e domésticos em todo o mundo.[75] Como são um agente patogénico do gado, designadamente de bezerros e leitões, o rotavírus é uma das causas de perdas económicas dos agricultores devido aos custos dos tratamentos associados com elevados níveis de morbidade e mortalidade.[76] Estes rotavírus que afectam os animais são um potencial reservatório para o intercâmbio genético com os rotavírus de humanos.[76] Existem evidências de que os rotavírus animais podem infetar humanos, quer por transmissão directa do vírus quer por ceder um ou vários dos seus segmentos genómicos de RNA a cepas humanas (por redistribuição ou recombinação).[77][78]
Virologia
Tipos de rotavírus
Existem cinco espécies de rotavírus, denominadas A, B, C, D e E. As infeções em humanos devem-se principalmente ás espécies A, B e C, mas especialmente à A. As cinco espécies podem provocar doenças noutros animais,[79] as espécies H em porcos, D, F e G em aves, I em gatos e J em morcegos.[80][81][82][83] O rotavírus A tem várias cepas, chamadas sorotipos.[84] Para os rotavírus, similarmente ao que ocorre no virus da gripe, é utilizado um sistema de classificação dual baseado nas duas proteínas de superfície do vírus. Uma delas é a glicoproteína VP7, que define os serotipos G, e a outra é a proteína VP4 sensível à protease, que define os serotipos P.[85] Uma vez que dois genes que determinam os tipos G e P podem transmitir-se separadamente à progénie destes vírus, podem ser encontradas diferentes combinações.[86] Foi atribuído um sistema completo de genotipagem do genoma para o Rotavírus A , que tem sido usado para determinar a origem de cepas atípicas.[87] A prevalência dos tipos G individuais e tipos P varia entre países e ao longo dos anos.[88] Existem pelo menos 36 tipos G e 51 tipos P mas em infecções humanas apenas algumas combinações de tipos G e P predominam. São eles G1P[8], G2P[4], G3P[8], G4P[8], G9P[8] e G12P[8].[89][88]
Estrutura
O genoma do rotavírus consiste de 11 moléculas de RNA bicatenário distintas, que possuem um total de 18 555 nucleótidos. Cada um destes segmentos ou moléculas é um gene, numerados do 1 ao 11 por tamanho decrescente. Cada gene codifica uma proteína, excepto o gene 9, que codifica duas.[90] O RNA é rodeado por uma cápside proteica icosaédrica de três camadas. As partículas virais têm cerca de 76,5 nm de diâmetro e não apresentam envoltura.[91][92]
Proteínas
Existem seis proteínas virais (VPs), que formam a partícula vírica (virião). Estas proteínas estruturais denominam-se por VP1, VP2, VP3, VP4, VP6 e VP7. Para além das VPs, existem seis proteínas não estruturais (NSPs), que se produzem só nas células infectadas por rotavírus, designadamente: NSP1, NSP2, NSP3, NSP4, NSP5 e NSP6.[79]
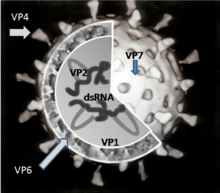
Pelo menos seis das doze proteínas codificadas pelo genoma do rotavírus unem-se ao RNA.[93] A função destas proteínas na replicação do rotavírus não é totalmente compreendida; acredita-se que estejam relacionadas com a síntese de RNA e o seu empacotamento no virião, o transporte de RNAm para o sítio de replicação do genoma, e a tradução do RNAm e regulação da expressão genética.[94]
Proteínas estruturais
A VP1 está localizada na parte central (núcleo) do vírus e é uma enzima RNA polimerase.[95] Numa célula infectada esta enzima produz transcrições de RNAm para a síntese de proteínas virais e produz cópias dos segmentos de RNA que formam o genoma do rotavírus para a produção de novas partículas víricas.
A VP2 forma a camada central do virião e liga-se ao genoma de RNA.[96]
A VP3 forma parte do núcleo interno do virião e é uma enzima chamada guanilil transferase, que catalisa a formação da cap 5' durante a modificação pós-transcricional do RNAm.[97] A cap 5' estabiliza o RNAm viral ao protegê-lo das enzimas que degradam os ácidos nucleicos designados de nucleases.[98]
A VP4 está na superfície do virião e sobressai como uma espícula.[99] Liga-se a moléculas receptoras da superfície celular e orienta a entrada do vírus na célula.[100] A VP4 deve ser modificada pela enzima tripsina (uma protease), que se encontra no trato digestivo, transformando-se em VP5* e VP8* antes que o vírus possa tornar-se infeccioso.[101] A VP4 determina o quão virulento o vírus é e define o tipo P do vírus.[102]
A VP6 forma a massa da cápside. É fortemente antigénica e pode ser utilizada para identificar as espécies de rotavírus.[3] Esta proteína é utilizada em testes laboratoriais para as infeções de rotavírus A.[103]
A VP7 é uma glicoproteína que forma a superfície externa do virião. Para além das suas funções estruturais, determina que o virus seja uma cepa do tipo G e, juntamente com a VP4, está implicada na imunidade à infecção.[91]
Proteínas virais não estruturais
A NSP1, produto do gene 5, trata-se duma proteína não estrutural que se une ao RNA.[104]
A NSP2 é uma proteína de ligação ao RNA que se acumula nas inclusões citoplasmáticas (viroplasma) necessárias para a replicação do genoma.[105][106]
A NSP3 liga-se ao RNAm viral nas células infectadas e é responsável pelo bloqueio da síntese de proteínas celulares.[107]
A NSP4 é uma enterotoxina viral que induz diarreia e foi a primeira enterotoxina viral descoberta.[13]
A NSP5 é codificada pelo segmento genómico 11 do rotavírus A e, em células infectadas pelo vírus, a NSP5 acumula-se no viroplasma.[108]
A NSP6 é uma proteína que se liga a ácidos nucleicos,[109] e é codificada no gene 11 a partir dum quadro de leitura aberta fora de fase.[110]
| Segmento de RNA (gene) | Tamanho (pares de bases) | Proteína | Peso molecular (kDa) | Localização | Cópias por partícula | Função |
|---|---|---|---|---|---|---|
| 1 | 3302 | VP1 | 125 | Nos vértices da parte central ('núcleo') | <25 | RNA polimerase RNA dependente |
| 2 | 2690 | VP2 | 102 | Forma a camada interna do núcleo | 120 | Estimula a RAN replicase viral |
| 3 | 2591 | VP3 | 88 | Nos vértices do núcleo | <25 | Enzima guanilil-transferase que coloca a cap 5' no RNAm |
| 4 | 2362 | VP4 | 87 | Espícula de superficie | 120 | Ligação à célula, virulência |
| 5 | 1611 | NSP1 | 59 | Não-estrutural | 0 | Ligação à extremidade 5' do RNA |
| 6 | 1356 | VP6 | 45 | Cápsida interna | 780 | Estrutural e antígeno específico de espécie |
| 7 | 1104 | NSP3 | 37 | Não-estrutural | 0 | Aumenta a actividade do RNAm viral e detém a síntese proteica celular |
| 8 | 1059 | NSP2 | 35 | Non estrutural | 0 | NTPase envolvida no empacotamento do RNA |
| 9 | 1062 | VP7¹ VP7² | 38 e 34 | Superfície | 780 | Estrutural e antígeno de neutralização |
| 10 | 751 | NSP4 | 20 | Não-estrutural | 0 | Enterotoxina |
| 11 | 667 | NSP5 NSP6 | 22 | Não-estrutural | 0 | Modulador que se liga ao RNA monocatenário e bicatenário de NSP2 |
Esta tabela é baseada no estudo da cepa do rotavírus símio SA11.[111][112][113] As atribuições de codificação da RNA-proteína diferem nalgumas cepas.
Replicação

Os rotavírus replicam-se principalmente no trato gastrointestinal[114] e infectam os enterócitos das vilosidades (villi) do intestino delgado, provocando mudanças estruturais e funcionais no epitélio.[115] O triplo recobrimento proteico do vírus torna-o resistente ao pH ácido do estômago e ás enzimas digestivas do trato gastrointestinal.
O vírus entra nas células por endocitose mediada por receptores e forma uma vesícula chamada endossoma. As proteínas da terceira camada (a VP7 e a espícula VP4) rompem a membrana do endossoma, criando uma diferença na concentração do cálcio. Isto provoca a rotura dos trímeros da VP7 em subunidades proteicas separadas, deixando as VP2 e VP6 em volta do RNA bicatenário viral, formando uma partícula de dupla camada (DLP).[116]
As onze moléculas de RNA bicatenário permanecem dentro das duas camadas proteicas protectoras e a RNA polimerase DNA-dependente viral gera transcritos de RNAm do genoma viral bicatenário. Ao permanecer dentro do núcleo, o RNA viral consegue evadir as respostas imunitárias do hóspede que utilizam o RNA de interferência, que são ativadas pela presença do RNA bicatenário na célula.
Durante a infecção, o rotavírus produz RNAm tanto para a síntese de proteínas como para a replicação génica. A maioria das proteínas do rotavírus acumula-se no viroplasma, onde se replica o RNA e se aglomeram as partículas de dupla camada (DLPs). O viroplasma forma-se ao redor do núcleo celular apenas duas horas depois da infecção vírica, e consiste de fábricas virais que se pensa serem formadas por duas proteínas víricas não estruturais: NSP5 e NSP2. A inibição da NSP5 por interferência de RNA dá lugar a uma forte diminuição na replicação dos rotavírus. As partículas de dupla camada migram para o retículo endoplasmático, onde adquirem a sua terceira camada, a mais externa, formada por VP7 e VP4. Os vírus filhos liberam-se da célula por lise.[101][117][118]
História

Em 1943, Jacob Luz e Horace Hodes provaram que um agente filtrável nas fezes de crianças com diarreia infecciosa também causou diarreia em bovinos.[119] Três décadas mais tarde, amostras conservadas do agente mostraram-se ser o rotavírus.[120] Nos anos seguintes, um vírus em camundongos mostrou-se relacionado com o vírus que causa diarreia.[121][122] Em 1973, Ruth Bishop descreveu vírus relacionados encontrados em crianças com gastroenterite.[123][124]
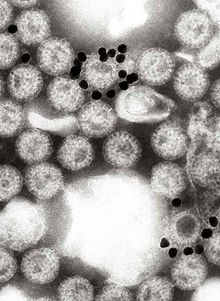
Em 1974, Thomas Henry Flewett sugeriu o nome de rotavírus depois de observar que, quando visto através de um microscópio de elétrons, uma partícula de rotavírus parece uma roda (rota, em latim);[125][126] o nome foi oficialmente reconhecido pelo Comitê Internacional de Taxonomia de Vírus quatro anos depois.[127] Em 1976, os vírus relacionados foram descritos em diversas outras espécies de animais.[122] Esses vírus, todos causando gastroenterite aguda, foram reconhecidos como um patógeno coletivo que afeta seres humanos e animais em todo o mundo.[125] Sorotipos de rotavírus foram primeiramente descritos em 1980[128] e, no ano seguinte, o rotavírus a partir de seres humanos foi cultivado em culturas de células derivadas de rins de macaco, pela adição de tripsina (uma enzima encontrada no duodeno de mamíferos e agora conhecida por ser essencial ao rotavírus para replicar) ao meio de cultura.[129] A capacidade de cultivar rotavírus em meio de cultura foi responsável por acelerar o ritmo das investigações e, em meados da década de 1980, os primeiros candidatos a vacinas estavam sendo avaliados.[130]
Em 1998, uma vacina contra o rotavírus foi licenciada para uso nos Estados Unidos. Ensaios clínicos nos Estados Unidos, Finlândia e Venezuela haviam encontrado entre 80 e 100% de eficiência na prevenção de diarreia grave causada por rotavírus, e os investigadores não tinham detectado nenhum efeito adverso grave estatisticamente significante.[131][132] O fabricante, porém, retirou o produto do mercado em 1999, depois que se descobriu que a vacina pode ter contribuído para um aumento do risco de intussuscepção, um tipo de obstrução intestinal, em uma de cada 12.000 crianças vacinadas.[133] A experiência provocou um intenso debate sobre os riscos e benefícios relativos de uma vacina contra o rotavírus.[134] Em 2006, duas novas vacinas contra a infecção do rotavírus foram mostradas seguras e eficazes em crianças[135] e, em junho de 2009, a Organização Mundial de Saúde recomendou que a vacinação contra o rotavírus fosse incluída em todos os programas nacionais de imunização para fornecer proteção contra este vírus.[136]
Em 2015, a Índia revelou uma vacina mais barata com o apoio do Instituto Nacional de Saúde dos Estados Unidos.[137]
Ver também
Referências
| Rotaviral Gastroenteritis | |
|---|---|
 , ,  | |
| Classificação e recursos externos | |
| CID-10 | A08.0 |
| CID-9 | 008.61 |
| CID-11 | 545685931 |
| DiseasesDB | 11667 |
| MedlinePlus | 000252 |
| eMedicine | emerg/401 |
| MeSH | D012400 |
 Leia o aviso médico Leia o aviso médico | |
Ligações externas
- Página web dos rotavírus da OMS
- Género Rotavirus (NCBI)
- Viralzone: Rotavirus
- Vaccine Resource Library: Rotavirus
- DefeatDD.org
- Estruturas macromoleculares tridimensionais de Rotavirus no EM Data Bank (EMDB)
- Centers for Disease Control and Prevention (2012). «Ch. 18: Rotavirus». In: Atkinson W, Wolfe S, Hamborsky J. Epidemiology and Prevention of Vaccine-Preventable Diseases 12.ª ed. Washington DC: Public Health Foundation. pp. 263–274. Consultado em 1 de maio de 2016. Arquivado do original em 12 de junho de 2012



