Živa(I) nitrat
Živa(I) nitrat je hemijsko jedinjenje sa formulom HgNO2. Ono se koristi u pripremi drugih živa(I) jedinjenja, i poput drugih živinih jedinjenje je toksično.
| Živa(I) nitrat[1][2] | |||
|---|---|---|---|
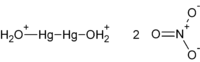 | |||
| IUPAC ime |
| ||
| Drugi nazivi | Živin nitrat | ||
| Identifikacija | |||
| CAS registarski broj | 10415-75-5 [7782-86-7] (dihidrat) | ||
| PubChem[3][4] | 11318980 | ||
| ChemSpider[5] | 9493944 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | Hg2(NO3)2 (anhydrous) Hg2(NO3)2·2H2O (dihydrate) | ||
| Molarna masa | 525,19 g/mol (anhidrat) 561,22 g/mol (dihidrat) | ||
| Agregatno stanje | Beli kristali (anhidrat) bezvojni kristali (dihidrat) | ||
| Gustina | ? g/cm3 (anhidrat) 4,8 g/cm3 (dihidrat) | ||
| Tačka topljenja | ? (anhidrat) | ||
| Rastvorljivost u vodi | neznatno rastvoran, reaktivan | ||
| Opasnost | |||
| NFPA 704 | |||
| Srodna jedinjenja | |||
| Drugi anjoni | Živa(I) fluorid Živa(I) hlorid Živa(I) bromid Živa(I) jodid | ||
| Drugi katjoni | Živa(II) nitrat | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Reakcije
Živa(I) nitrat se formira kombinovanjem žive sa razblaženom azotnom kiselinom (koncentrovana azotna kiselina bi proizvela živa(II) nitrat). Živa(I) nitrat je redukujući agens koji se oksiduje u kontaktu sa vazduhom.
Rastvori živa(I) nitrata su kiseli usled spore reakcije sa vodom:
- Hg2(NO3)2 + H2O → Hg2(NO3)(OH) + HNO3
Hg2(NO3)(OH) formira žuti talog.
Ako se rastvor zagreje do ključanja ili izloži svetlosti, živa(I) nitrat podleže reakciji disproporcionacije proizvodeći elementarnu živu i živa(II) nitrat[2]:
- 2Hg2(NO3)2 → Hg + Hg(NO3)2

