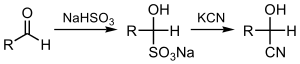
Kyánhydrín
Kyánhydrín je funkčná skupina, v ktorej sú kyano a hydroxylová skupina naviazané na rovnaký atóm uhlíka.[1][2] Všeobecný vzorec je R2C(OH)CN, kde R je H, alkyl alebo aryl. Kyánhydríny sú priemyselne dôležité prekurzory karboxylových kyselín a niektorých aminokyselín. Kyánhydríny môžu byť vytvorené kyánhydrínovou syntézou, ktorá zahŕňa reakciu ketónu alebo aldehydu s kyanovodíkom (HCN) v prítomnosti nadbytočného množstva kyanidu sodného (NaCN) ako katalyzátora:[2][3]
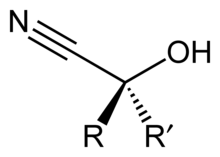
- RR'C=O + HCN → RR'C(OH)CN
V tejto reakcii napadá nukleofilný ión CN- elektrofilný karbonylový uhlík v ketóne či aldehyde a potom nasleduje protonácia pomocou HCN, čím sa regeneruje kyanidový anión. Kyánhydríny sa tiež pripravujú vytesnením siričitanu kyanidovými soľami:[4]
Kyánhydríny sú medziprodukty v Streckerovej syntéze aminokyselín. Vo vodných roztokoch kyselín hydrolyzujú na α-hydroxykyseliny.
Metódy prípravy
Kyánhydríny sa najskôr pripravovali pridaním HCN a katalyzátora (zásady alebo enzýmu) k zodpovedajúcemu karbonylu.[5] Zásada spôsobuje deprotonáciu málo reaktívneho kyanovodíku, HCN, čím vznikajú CN- ióny.[2] V laboratórnom merítku sa použitie (toxického) HCN vo veľkej miere neodporúča, z tohto dôvodu sa hľadajú iné menej nebezpečné kyanačné činidlá. In situ tvorbu HCN možno docieliť práve pomocou prekurzorov, ako je acetónkyánhydrín. Alternatívne, kyano-silylderiváty, ako je TMS-CN, umožňujú kyanáciu aj ochranu skupiny v jednom kroku bez potreby HCN.[6] Boli opísané podobné postupy založené na tvorbe esterov, fosforečnanov a uhličitanov.[7][8][9]

Príklady
Acetónové kyánhydríny
Acetónkyanohydrín, (CH3)2C(OH)CN, je kyánhydrín acetónu. Vzniká ako medziprodukt pri priemyselnej výrobe metylmetakrylátu.[10] V laboratóriu táto kvapalina slúži ako zdroj HCN, ktorý je inak veľmi prchavý. [11] Acetónkyánhydrín sa teda môže použiť na prípravu iných kyánhydrínov, na premenu HCN na Michaelove akceptory a na formyláciu arénov. Reakciou tohto kyánhydrínu s hydridom lítnym vzniká bezvodý kyanid lítny:
Iné kyánhydríny
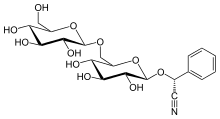
Mandelonitril so vzorcom C6H5CH(OH)CN sa v malých množstvách vyskytuje v kôstkach niektorých druhov ovocia.[4] Sú známe príbuzné kyanogénne glykozidy, ako je amygdalín.[3] Tieto glykozidy majú namiesto hydroxylovej skupiny glykozid.
Glykolonitril je organická zlúčenina so vzorcom HOCH2CN . Je to najjednoduchší kyánhydrín, odvodený od formaldehydu.[12]
- glykolonitril
- acetónkyanohydrín
- mandelonitril
Referencie
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Cyanohydrin na anglickej Wikipédii.