Бизмут пентафлуорид
Бизмут пентафлуорид е неорганско соединение со формула BiF 5 . Тоа е бела цврста материја која е многу реактивна. Соединението е од интерес за истражувачите, но не е од особена вредност.
 | |
 | |
Други називи бизмут(V) флуорид | |
| Назнаки | |
|---|---|
| 7787-62-4 | |
| ChEBI | CHEBI:30426 |
| ChemSpider | 21172752 |
МХН
| |
| 3Д-модел (Jmol) | Слика |
| PubChem | 123260 |
| |
| UNII | BX273GFK98 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | долги бели игли,[1] безбоен кристален цврст[2] |
| Густина | 5.40 g cm−3[1] |
| Точка на топење | |
| Точка на вриење | |
| Структура | |
Координациска геометрија | октаедра Би |
| Опасност | |
| GHS-ознаки: | |
Пиктограми |   |
Сигнални зборови | Опасност |
Изјави за опасност | H272, H314 |
Изјави за претпазливост | P210, P220, P221, P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P370+P378, P405, P501 |
| NFPA 704 | |
| Безбедносен лист | MSDS |
| Слични супстанци | |
| Други анјони | бизмут трихлорид, бизмут трибромид, бизмут тријодид, пентаметилбизмут |
| Други катјони | фосфор пентафлуорид, арсен пентафлуорид, антимон пентафлуорид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
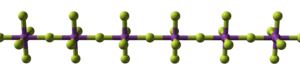
BiF 5 е полимерно соединение и се состои од линеарни синџири на транс -премостени аголни BiF 6 октаедри.[3] Ова е истата структура како <i id="mwKQ">α</i> -UF <sub id="mwKg">5</sub> .
 </img> </img> </img> </img> |  </img> </img> </img> </img> |
| (BiF 5 ) ∞ синџир | пакување на синџири |
Подготовка
BiF 5 може да се подготви со третирање на BiF 3 со F 2 на 500 °C.
- BiF 3 + F 2 → BiF 5
Во алтернативна синтеза, ClF <sub id="mwUw">3</sub> е флуорирачки агенс на 350 °C.[4]
- BiF 3 + ClF 3 → BiF 5 + ClF
Реакции
Бизмут пентафлуорид е најреактивниот од пниктогенот пентафлуориди и е исклучително силен флуорирачки агенс . Тој енергично реагира со вода за да формира озон и кислород дифлуорид, и со јод или сулфур на собна температура. BiF 5 го флуорира парафинското масло ( јаглеводороди ) до флуоројаглероди над 50 °C и оксидира UF <sub id="mwZw">4</sub> до UF <sub id="mwaQ">6</sub> на 150 °C. На 180 °C, бизмут пентафлуорид флуоринира Br 2 до BrF <sub id="mwbw">3</sub> и Cl 2 до ClF .
BiF 5, исто така, реагира со флуориди на алкални метали, MF, за да формира хексафлуоробизмутати, M[ BiF6 ], кој го содржи хексафлуоробизмутат анјон, [BiF 6 ] - .
