เฟอร์ริติน
เฟอร์ริติน (อังกฤษ: Ferritin) เป็นโปรตีนในเซลล์ทั่วไปที่สะสมธาตุเหล็กและปล่อยมันอย่างเป็นระบบโปรตีนนี้มีในสิ่งมีชีวิตเกือบทั้งหมด รวมทั้งสาหร่าย แบคทีเรีย พืชชั้นสูง และสัตว์ในมนุษย์ มันมีหน้าที่เป็นสารบัฟเฟอร์เพื่อไม่ให้ขาดเหล็กหรือมีเหล็กเกิน[3]และพบในเนื้อเยื่อโดยมากในรูปแบบของโปรตีนในไซโตซอล (ในไซโทพลาซึมของเซลล์) แต่ก็มีส่วนหนึ่งที่อยู่ในเลือดโดยทำหน้าที่เป็นตัวขนส่งธาตุเหล็กระดับเฟอร์ริตินในเลือดยังเป็นตัวชี้ทางชีวภาพ (biomarker) ของปริมาณธาตุเหล็กที่สะสมในร่างกาย และดังนั้น จึงสามารถตรวจสอบเพื่อวินิจฉัยภาวะเลือดจางเหตุขาดธาตุเหล็ก (iron-deficiency anemia)[4]
| เฟอร์ริติน (Ferritin) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
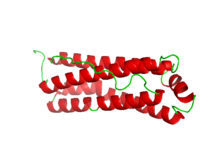
 โครงสร้างของ murine ferritin complex[1] | |||||||||
| ป้ายระบุ | |||||||||
| สัญลักษณ์ | Ferritin | ||||||||
| พีแฟม | PF00210 | ||||||||
| วงศ์ในพีแฟม | CL0044 | ||||||||
| อินเทอร์โปร | IPR008331 | ||||||||
| SCOP | 1fha | ||||||||
| SUPERFAMILY | 1fha | ||||||||
| |||||||||
| ferritin, light polypeptide | |
|---|---|
| ตัวบ่งชี้ | |
| สัญลักษณ์ | FTL |
| Entrez | 2512 |
| HUGO | 3999 |
| OMIM | 134790 |
| RefSeq | NM_000146 |
| UniProt | P02792 |
| ข้อมูลเพิ่มเติม | |
| โลคัส | Chr. 19 q13.3-13.4{{{LocusSupplementaryData}}} |
| ferritin, heavy polypeptide 1 | |
|---|---|
| ตัวบ่งชี้ | |
| สัญลักษณ์ | FTH1 |
| สัญลักษณ์อื่น ๆ | FTHL6 |
| Entrez | 2495 |
| HUGO | 3976 |
| OMIM | 134770 |
| RefSeq | NM_002032 |
| UniProt | P02794 |
| ข้อมูลเพิ่มเติม | |
| โลคัส | Chr. 11 q13{{{LocusSupplementaryData}}} |
| ferritin mitochondrial | |
|---|---|
 โครงสร้างทางผลิกศาสตร์ของ mitochondrial ferritin[2] | |
| ตัวบ่งชี้ | |
| สัญลักษณ์ | FTMT |
| Entrez | 94033 |
| HUGO | 17345 |
| OMIM | 608847 |
| RefSeq | NM_177478 |
| UniProt | Q8N4E7 |
| ข้อมูลเพิ่มเติม | |
| โลคัส | Chr. 5 q23.1{{{LocusSupplementaryData}}} |
เฟอร์ริตินเป็นคอมเพล็กซ์โปรตีนรูปทรงกลมที่มีหน่วยย่อย 24 หน่วยและเป็น "โปรตีนเก็บธาตุเหล็กในเซลล์" หลักทั้งในโพรแคริโอตและยูแคริโอต โดยเก็บเหล็กในรูปแบบที่ละลายน้ำได้และไม่มีพิษส่วนเฟอร์ริตินที่ไม่รวมเข้ากับธาตุเหล็กก็จะเรียกว่า apoferritin
ยีน
ยีนเฟอร์ริตินในสปีชีส์ต่าง ๆ คล้ายกันมากเช่น ยีนในสัตว์มีกระดูกสันหลังล้วนแต่มี intron สามหน่วยและ exon สี่หน่วย[5]ในมนุษย์ intron จะอยู่ระหว่าง residue ของกรดอะมิโนที่ตำแหน่ง 14 และ 15, 34 และ 35, 82 และ 83นอกจากนั้นแล้ว ยังมี untranslated bases ประมาณ 200 จุดที่ exon สองด้านรวมกันทั้งหมด[6]ส่วน tyrosine residue ที่ตำแหน่ง 27 เชื่อว่าเกี่ยวข้องกับกระบวนการ biomineralization[7]
โครงสร้างโปรตีน
เฟอร์ริตินเป็นโปรตีนกลวงรูปกลมมีมวลอะตอมที่ 450 kDa โดยมีหน่วยย่อย 24 หน่วยและอยู่ในเซลล์ทุกชนิด[6]โดยทั่วไปแล้วจะมีขนาดผ่าศูนย์กลางภายในภายนอกที่ 8 และ 12 นาโนเมตร ตามลำดับ[8]
ในสัตว์มีกระดูกสันหลัง หน่วยย่อยจะเป็นแบบเบา (light, L, Ferritin light chain) และแบบหนัก (heavy, H, FTH1) โดยมีมวลโมเลกุลที่ 19 kDa และ 21 kDa ตามลำดับลำดับยีนของหน่วยย่อยทั้งสองมีกำเนิดโครงสร้างเดียวกัน (homologous) ประมาณ 50%[6]ส่วนสัตว์สะเทินน้ำสะเทินบกมีเฟอร์ริตินเพิ่มอีกแบบที่เรียกว่าแบบ "M"[9]ส่วนเฟอร์ริตินรูปแบบเดียวที่พืชและแบคทีเรียมีคล้ายกับแบบ H[9]มีเฟอร์ริตินอีกสองอย่างที่พบในหอยฝาเดียว Lymnaea โดยเฟอร์รินตินที่อยู่ในตัว (somatic) และในไข่ (yolk) จะต่างกัน (ดูรายละเอียดต่อไป)[9]มีรูปแบบอื่นอีกที่คล้ายกับที่พบในตัวของ Lymnaea ที่เกี่ยวกับการสร้างเปลือกของหอยนางรม[10]ในปรสิตสกุล Schistosoma มีรูปแบบสองอย่างที่ต่างกันระหว่างตัวเมียและตัวผู้[9]รูปแบบทั้งหมดที่กล่าวถึงแล้วมีลำดับหลักคล้ายกับรูปแบบ H ของสัตว์มีกระดูกสันหลัง[9]ส่วนในแบคทีเรีย E. coli เฟอร์ริตินที่พบคล้ายกับแบบ H ของมนุษย์ที่ 20%[9]
ในเปลือกของเฟอร์ริติน ไอออนเหล็กจะอยู่ในรูปแบบผลึก (crystallite)ซึ่งจะคล้าย ๆ กับแร่ ferrihydriteคอมเพล็กซ์เฟอร์ริตินแต่ละหน่วยจะสามารถสะสมธาตุเหล็ก (Fe3+) ได้ประมาณ 4,500 ไอออน[6][9]
คอมเพล็กซ์เฟอร์ริตินบางส่วนในสัตว์มีกระดูกสันหลังเป็น hetero-oligomer ของผลิตภัณฑ์ยีนสองอย่างที่สัมพันธ์กันอย่างใกล้ชิดโดยมีคุณสมบัติทางสรีรภาพต่างกันเล็กน้อยอัตราโปรตีนสองอย่างนี้ที่มีโครงสร้างกำเนิดเดียวกัน (homologous) ในคอมเพล็กซ์จะขึ้นอยู่กับระดับการแสดงออกของยีนสองตัวที่ว่า
งานวิจัยปี 2544 แสดงว่าเฟอร์ริตินของไมโทคอนเดรีย (mitochondrial ferritin) เป็นสารตั้งต้นของโปรตีน (protein precursor) อย่างหนึ่ง และจัดเป็นโปรตีนที่จับกับโลหะภายในไมโทคอนเดรีย[11]หลังจากที่โปรตีนผ่านกระบวนการของไมโทคอนเดรียไปแล้ว ก็จะสามารถสร้างเป็นเปลือกเฟอร์ริตินที่ใช้การได้โดยมีโครงสร้างขนาด 1.70 อังสตรอม วัดโดยการเลี้ยวเบนรังสีเอกซ์ (X-ray diffraction) โดยมี residue 182 แห่งและ 67% ของโครงสร้างจะเป็นรูปวนก้นหอย (helical)กราฟ Ramachandran plot[12]แสดงว่า โครงสร้างของเฟอร์ริตินไมโทคอนเดรียเป็นรูปวนก้นหอยแบบ alpha โดยมี beta sheet น้อยและไม่เหมือนกับเฟอร์ริตินของมนุษย์ประเภทอื่น ๆ ยีนของมันปรากฏกว่าไม่มีส่วน intron
หน้าที่
การเก็บสะสมเหล็ก
เฟอร์ริตินมีหน้าที่เก็บธาตุเหล็กในรูปแบบที่ไม่เป็นพิษ และขนส่งมันไปยังที่ที่ต้องการ[13]หน้าที่และโครงสร้างของเฟอร์ริตินจะแสดงออกต่าง ๆ กันในเซลล์ต่าง ๆซึ่งโดยหลักคุมโดยปริมาณและเสถียรภาพของเอ็มอาร์เอ็นเอ (Messenger RNA, mRNA)และความเข้มข้นของ mRNA ยังแปรไปตามวิธีการที่เก็บและประสิทธิภาพในการถอดรหัสมัน[6]
การมีธาตุเหล็กเองเป็นตัวจุดชนวนหลักอย่างหนึ่งให้ผลิตเฟอร์ริติน[6]โดยมีข้อยกเว้นบ้าง (เช่น เฟอร์ริตินในไข่ของหอยฝาเดียว Lymnaea ซึ่งไม่ตอบสนองต่อการมีธาตุเหล็ก)[9]ส่วนเหล็กที่เป็นอิสระ คือไม่ยึดกับเฟอร์ริติน จะเป็นพิษต่อเซลล์เนื่องจากเป็นตัวเร่งปฏิกิริยาให้เกิดอนุมูลอิสระจากสารกลุ่ม reactive oxygen species ที่เกิดจากปฏิกิริยา Fenton Reaction[14]ดังนั้น สัตว์มีกระดูกสันหลังจึงได้วิวัฒนาการกลไกป้องกันที่ซับซ้อนเพื่อจับเหล็กในเนื้อเยื่อต่าง ๆ
ภายในเซลล์ เหล็กจะเก็บเป็นคอมเพล็กซ์โปรตีนโดยเป็น ferritin หรือ hemosiderinส่วน Apoferritin จะเป็นเฟอร์ริตินที่เข้ายึดเหล็กที่เป็นอิสระเมื่อเซลล์ใน reticuloendothelial (RE) system ซึ่งเป็นส่วนของระบบภูมิต้านทานสะสมเหล็กมากขึ้น โปรตีนที่สะสมจะรวมตัวกันเป็น hemosiderinเซลล์ใน RE สามารถดึงเอาเหล็กทั้งที่อยู่ในรูปแบบเฟอร์ริตินและ hemosiderin ได้ แต่ว่า จาก hemosiderin จะยากกว่าเมื่อคงตัว ระดับเหล็กในเลือดจะสัมพันธ์กับเหล็กที่สะสมในร่างกายดังนั้น การวัดเฟอร์ริตินในเลือดโดย FR5Rl เป็นการทดสอบทางห้องปฏิบัติการที่สะดวกที่สุดเพื่อประเมินปริมาณเหล็กที่สะสมในร่างกาย
เพราะว่าเหล็กเป็นธาตุที่สำคัญในกระบวนการ mineralization จึงมีเฟอร์ริตินในเปลือกของสิ่งมีชีวิตเช่นมอลลัสกา เพื่อควบคุมความเข้มข้นและการกระจายของเหล็ก และดังนั้น จึงมีอิทธิพลต่อสัณฐานและสีของเปลือกด้วย[15][16]มันยังมีบทบาทในของเหลว (haemolymph) ในตัวของมอลลัสกาชั้นพอลิพลาโคฟอรา ซึ่งทำหน้าที่ขนส่งเหล็กไปยัง radula (ส่วนที่คล้ายลิ้นใช้กินอาหาร) เพื่อกระบวนการ mineralization[17]
ไลโซโซมเป็นตัวปล่อยเหล็กจากเฟอร์ริตินโดยหลักผ่านกระบวนการสลายเฟอร์ริติน[18]
การทำงานของ ferroxidase
เฟอร์ริตินของสัตว์มีกระดูกสันหลังมีหน่วยย่อย 2-3 หน่วยซึ่งตั้งชื่อตามมวลโมเลกุล คือ L "light" (เบา), H "heavy" (หนัก), และ M "middle" (ปานกลาง)แต่แบบ M พบในกบบูลฟร็อกเท่านั้นส่วนในแบคทีเรียและอาร์เคีย เฟอร์ริตินจะมีหน่วยย่อยหน่วยเดียว[19]
หน่วยย่อย H และ M ของเฟอร์ริตินในยูแคริโอต และหน่วยย่อยทั้งหมดของแบคทีเรียและอาร์เคีย (ซึ่งล้วนเป็นแบบ H) จะมี ferroxidase เป็นเอนไซม์เปลี่ยนเหล็กจากรูปแบบ Fe2+ (ferrous, di-iron) เป็น Fe3+ (ferric)ซึ่งจำกัดปฏิกิริยาที่เกิดระหว่าง Fe2+ กับไฮโดรเจนเพอร์ออกไซด์ ที่เรียกว่า Fenton reaction ซึ่งผลิตอนุมูลอิสระของไฮดรอกซิลที่มีอันตรายมากการทำงานของ ferroxidase จะเกิดที่จุดยึด di-iron ที่ตรงกลางของหน่วยย่อย H แต่ละหน่วย[19][20]หลังจากกระบวนการออกซิเดชันของ Fe (II) ผลิตภัณฑ์ที่เป็น Fe (III) จะอยู่ในสภาพไม่ค่อยเสถียร (metastable) ตรงกลางของ ferroxidase จนกระทั่ง Fe (II) เข้าไปแทนที่มัน[20][21]ซึ่งดูจะเป็นกลไกสามัญของเฟอร์ริตินในอาณาจักรสิ่งมีชีวิตทั้งสาม[19]เฟอร์ริตินแบบ L ไม่มีการทำงานของ ferroxidase แต่อาจมีหน้าที่ส่งอิเล็กตรอนผ่านกรงโปรตีน (protein cage)[22]
ปฏิกิริยาของภูมิคุ้มกัน
ระดับเฟอร์ริตินจะสูงขึ้นอย่างมากเมื่อมีการอักเสบหรือมะเร็งชีวพิษภายในตัว (Endotoxin) เป็นตัวเพิ่มการผลิตเฟอร์ริตินแต่ก็มีสิ่งชีวิต เช่น แบคทีเรียสกุล Pseudomonas ที่แม้จะมีชีวพิษภายในตัว ก็จะลดระดับเฟอร์ริตินอย่างสำคัญภายใน 48 ชม. แรกที่เกิดการอักเสบฉะนั้น โดยมากแล้ว เหล็กที่สะสมภายในร่างกายจะกันไม่ให้แก่สิ่งที่ก่อโรค ซึ่งช่วยขัดขวางเมแทบอลิซึมของมัน[23]
การตอบสนองต่อความเครียด
ระดับเฟอร์ริตินพบว่าจะเพิ่มขึ้นตอบสนองต่อความเครียด เช่นเมื่อขาดออกซิเจน[24]ซึ่งแสดงว่ามันเป็นโปรตีนที่ตอบสนองต่อภาวะอักเสบในระยะเฉียบพลัน (acute-phase protein)[25]
ไมโทคอนเดรีย
เฟอร์ริตินในไมโทคอนเดรียมีบทบาทหลายอย่างคือมีส่วนร่วมในการทำงานของ ferroxidase, ของการยึดไอออนธาตุเหล็ก (iron), ของ oxidoreductase, ของการยึดเหล็กแบบ ferric, ของการยึดไอออนโลหะ (metal ion binding) และของการยึดโลหะทรานซิชันในกระบวนการชีวภาพ มันยังมีส่วนร่วมในกระบวนการออกซิเดชัน-รีดักชัน ในการขนส่งไอออนเหล็กข้ามเยื่อหุ้มเซลล์ และภาวะธำรงดุลของไอออนเหล็กภายในเซลล์
ในไข่
ในหอยทากบางชนิด โปรตีนส่วนมากในไข่จะเป็นเฟอร์ริติน[26]แต่จะเป็นเฟอร์ริตินที่ต่าง คือมีลำดับยีนต่างจากเฟอร์ริตินในตัวและผลิตในต่อมทางเดินอาหารส่วนกลาง (midgut glands) หลั่งออกใน hemolymph แล้วจึงส่งไปที่ไข่[26]
การประยุกต์ใช้ในอุตสาหกรรม
เฟอร์ริตินยังใช้ในวัสดุศาสตร์เป็นสารตั้งต้นเพื่อทำอนุภาคนาโนเพื่อก่อท่อนาโนคาร์บอนโดยกระบวนการ chemical vapor deposition
การกระจายในเนื้อเยื่อ
ในสัตว์มีกระดูกสันหลัง เฟอร์ริตินมักจะพบภายในเซลล์ แต่ว่าก็จะพบแม้ว่าปริมาณน้อยกว่าในเลือดด้วย[23]
การใช้เพื่อวินิจฉัย
ระดับเฟอร์ริตินในเลือดสามารถวัดได้ในห้องปฏิบัติการโดยเป็นส่วนของการตรวจสอบเหล็กเพื่อวินิจฉัยว่าเป็นภาวะเลือดจางเหตุขาดธาตุเหล็กหรือไม่ระดับเฟอร์ริตินในเลือดปกติจะมีสหสัมพันธ์โดยตรงกับปริมาณเหล็กที่ร่างกายสะสมแต่ว่า ระดับก็อาจจะสูงกว่าปกติในกรณีที่มีภาวะเลือดจางเหตุโรคเรื้อรัง (anemia of chronic disease) ที่เฟอร์ริตินสูงขึ้นโดยเป็นส่วนของ acute phase protein ที่เกิดจากการอักเสบ และไม่ใช่เป็นตัวชี้ว่ามีเหล็กเกิน
พิสัยปกติ
ห้องปฏิบัติการแต่ละแห่ง ๆ จะกำหนดพิสัยปกติของระดับเฟอร์ริตินและอาจอยู่ระหว่าง 30-300 ng/mL (=μg/L) สำหรับผู้ชาย และ 18-115 ng/mL (=μg/L) สำหรับผู้หญิง
| ชาย | 18-270 ng/mL |
| หญิง | 18-160 ng/mL |
| เด็ก (6 เดือน - 15 ปี) | 7-140 ng/mL |
| ทารก (1-5 เดือน) | 50-200 ng/mL |
| เด็กเกิดใหม่ | 25-200 ng/mL |
ระดับเฟอร์ริตินต่ำ
ถ้าระดับเฟอร์ริตินต่ำ จะมีโอกาสเสี่ยงขาดธาตุเหล็ก ซึ่งนำไปสู่ภาวะเลือดจางสำหรับภาวะเลือดจาง ระดับเฟอร์ริตินต่ำเป็นการทดสอบทางแล็บที่จำเพาะที่สุดต่อภาวะเลือดจางเหตุขาดธาตุเหล็ก (คือ ถ้าค่าต่ำพอ การมีเฟอร์ริตินต่ำแสดงว่าภาวะเลือดจางที่มี มีโอกาสเกิดจากการขาดธาตุเหล็กมากที่สุด)[28]แต่ว่า นี่ไม่ใช่เป็นการทดสอบที่ไว (คือการมีระดับปกติในเลือดไม่ได้แสดงว่าไม่ขาดธาตุเหล็ก) เนื่องจากระดับสามารถสูงขึ้นเนื่องจากการติดเชื้อหรือการอักเสบเรื้อรัง[29]และภาวะเหล่านี้อาจเปลี่ยนระดับเฟอร์ริตินที่ควรจะต่ำให้สูงจนถึงปกติดังนั้น การมีระดับเฟอร์ริตินต่ำให้ข้อมูลมากกว่าเมื่อมีระดับปกติแต่ระดับเฟอร์ริตินต่ำก็อาจแสดงว่ามีโรคไทรอยด์ ขาดวิตามินซี หรือเป็นโรค celiac disease ได้ด้วย
การทานอาหารมังสะวิรัติอาจทำให้มีระดับเฟอร์ริตินในเลือดต่ำเนื่องจากขาดธาตุเหล็ก โดยพบใน 19% ของคนทานเจในงานศึกษาในประเทศไทยปี 2542[30]
ระดับเฟอร์ริตินต่ำก็พบในคนไข้กลุ่มอาการขาไม่เป็นสุข (restless legs syndrome) บางคน ซึ่งอาจจะไม่เกี่ยวกับภาวะเลือดจาง แต่เนื่องจากมีธาตุเหล็กน้อยแต่ยังไม่ถึงภาวะเลือดจาง[31][32]
การมีเฟอร์ริตินต่ำโดยไม่ได้มีโรคจริง ๆ (false positive) เป็นเรื่องไม่สามัญ[29]แต่อาจเกิดจาก hook effect ของเครื่องวัดในบางกรณี[33]
ระดับเฟอร์ริตินสูง
ถ้าระดับเฟอร์ริตินสูง แสดงว่ามีการสะสมเหล็กเกิน หรือว่ามีปฏิกิริยาอักเสบอย่างฉับพลัน (acute inflammatory reaction) ที่มีการสร้างเฟอร์ริตินโดยไม่ได้มีเหล็กเกินยกตัวอย่างเช่น เมื่อติดเชื้อ ระดับเฟอร์ริตินอาจสูงขึ้นโดยไม่ได้แสดงว่ามีเหล็กเกินเฟอร์ริตินยังใช้เป็นตัวบ่งชี้โรคเหล็กเกินต่าง ๆ รวมทั้ง ภาวะเหล็กเกิน (hemochromatosis) และ hemosiderosisโรคสติลล์ที่เริ่มเป็นในผู้ใหญ่, porphyrias, hemophagocytic lymphohistiocytosis/macrophage activation syndrome ซึ่งล้วนแต่เป็นโรคที่อาจทำระดับเฟอร์ริตินให้สูง
เฟอร์ริตินสูงยังเป็นปฏิกิริยาช่วงติดโรค (acute-phase reactant) อย่างหนึ่ง ซึ่งบ่อยครั้งจะสูงขึ้นในโรคบางอย่างระดับ C-reactive protein ที่ปกติสามารถใช้กันระดับเฟอร์ริตินที่สูงเนื่องจากปฏิกิริริยาช่วงติดโรค
ตามงานศึกษาปี 2547 คนไข้โรคเบื่ออาหารเหตุจิตใจ (anorexia nervosa) สามารถมีระดับเฟอร์ริตินที่สูงในช่วงขาดอาหารอย่างฉับพลัน ซึ่งอาจจะเป็นเพราะเหล็กออกสะสมในเลือด โดยจำนวนเม็ดเลือดแดงจะตกลง[34]ส่วนงานศึกษาปี 2556 เสนอว่า เนื่องจากความผิดปกติของเมแทบอลิซึมในโรคนี้ จึงอาจมีการหลั่ง isoferritin ออกนอกจากนั้นแล้ว เฟอร์ริตินยังมีหน้าที่สำคัญที่ไม่เกี่ยวกับการเก็บเหล็ก เช่นเป็นตัวป้องกันอันตรายที่เกิดจากออกซิเดชันและระดับ isoferritin อาจทำให้ระดับเฟอร์ริตินที่วัดสูงขึ้นการวัดเฟอร์ริตินผ่านกระบวนการ immunoassay หรือ immunoturbidimeteric อาจจะจับค่า isoferritin เหล่านี้ซึ่งไม่ได้สะท้อนการเก็บสะสมเหล็กในร่างกายจริง ๆ[35]
การประยุกต์ใช้อื่น ๆ
ช่องที่อยู่ในเฟอรร์ริตินและ mini-ferritin (DNA-binding proteins from starved cells ตัวย่อ Dps) ได้ทดลองใช้เป็นห้องปฏิกิริยาเพื่อสร้างอนุภาคนาโนโลหะ[36][37][38][39]เปลือกของโปรตีน เช่น ของเฟอร์ริติน สามารถใช้เป็นตัวจำกัดการเติบโตของอนุภาคและใช้เป็นตัวเคลือบอนุภาคโดยใช้เปลือกโปรตีนขนาดต่าง ๆ กัน ก็จะสามารถสังเคราะห์อนุภาคนาโนขนาดต่าง ๆ ที่มีคุณสมบัติทางเคมี ทางกายภาพ และทางชีวเวชที่ต่าง ๆ กัน
เชิงอรรถและอ้างอิง
แหล่งข้อมูลอื่น
- Ferritins ในหอสมุดแพทยศาสตร์แห่งชาติอเมริกัน สำหรับหัวข้อเนื้อหาทางการแพทย์ (MeSH)
- Ferritin เก็บถาวร 2017-07-28 ที่ เวย์แบ็กแมชชีน ที่ Lab Tests Online
- Ferritin: analyte monograph - The Association for Clinical Biochemistry and Laboratory Medicine
- ข้อมูลเชิงโครงสร้างทั้งหมดของ UniProt: P02792 (Ferritin light chain) สามารถเข้าถึงได้ในธนาคารข้อมูลโปรตีนของ PDBe-KB.
- ข้อมูลเชิงโครงสร้างทั้งหมดของ UniProt: P02794 (Ferritin heavy chain) สามารถเข้าถึงได้ในธนาคารข้อมูลโปรตีนของ PDBe-KB.
- ข้อมูลเชิงโครงสร้างทั้งหมดของ UniProt: Q8N4E7 (Ferritin, mitochondrial) สามารถเข้าถึงได้ในธนาคารข้อมูลโปรตีนของ PDBe-KB.
