സോഡിയം പെറോക്സൈഡ്
 | |
 | |
 | |
| Names | |
|---|---|
| Other names Disodium dioxide Flocool Solozone Disodium peroxide | |
| Identifiers | |
3D model (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.828 |
| EC Number |
|
PubChem CID | |
| RTECS number |
|
| UNII | |
| UN number | 1504 |
CompTox Dashboard (EPA) | |
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | yellow to white powder |
| സാന്ദ്രത | 2.805 g/cm3 |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| reacts violently | |
| Solubility | soluble in acid insoluble in base reacts with ethanol |
| −28.10·10−6 cm3/mol | |
| Structure | |
| hexagonal | |
| Thermochemistry | |
| Std enthalpy of formation ΔfH | −515 kJ·mol−1[1] |
| Standard molar entropy S | 95 J/(mol·K)[1] |
| Specific heat capacity, C | 89.37 J/(mol·K) |
| Hazards | |
| Safety data sheet | External MSDS |
| GHS pictograms |   |
| GHS Signal word | Danger |
GHS hazard statements | H271, H314 |
GHS precautionary statements | P210, P220, P221, P260, P264, P280, P283, P301+330+331, P303+361+353, P304+340, P305+351+338, P306+360, P310, P321, P363, P370+378, P371+380+375, P405, P501 |
| Flash point | {{{value}}} |
| Related compounds | |
| Other cations | Lithium peroxide Potassium peroxide Rubidium peroxide Caesium peroxide |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
Na2O2 എന്ന സൂത്രവാക്യമുള്ള അജൈവ സംയുക്തമാണ് സോഡിയം പെറോക്സൈഡ്. ഓക്സിജനിൽ സോഡിയം ജ്വലിച്ചുണ്ടാകുന്ന ഖരരൂപത്തിലുള്ള ഉൽപ്പന്നമാണിത്. ശക്തമായ ഒരു ആൽക്കലിയാണിത്. Na2O2·2H2O2·4H2O, Na2O2·2H2O, Na2O2·2H2O2, and Na2O2·8H2O എന്നിവയുൾപ്പെടെ നിരവധി ഹൈഡ്രേറ്റുകളിലും പെറോക്സിഹൈഡ്രേറ്റുകളിലും ഈ ലോഹ പെറോക്സൈഡ് നിലവിലുണ്ട്. [3][4]സോഡിയം പെറോക്സൈഡിന് സോളോസോൺ [5], ഫ്ലോക്കൂൾ എന്നീ വാണിജ്യ നാമങ്ങളുണ്ട്. [6]
സവിശേഷതകൾ
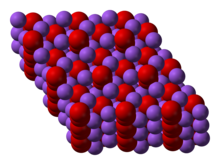
സോഡിയം പെറോക്സൈഡ് ഷഡ്ഭുജ സമമിതിയോടെ ക്രിസ്റ്റലൈസ് ചെയ്യുന്നു. [7] 512 ഡിഗ്രി സെന്റിഗ്രേഡിൽ ചൂടാക്കുമ്പോൾ, ഷഡ്ഭുജാകൃതിയിലുള്ള രൂപം അജ്ഞാത സമമിതിയുടെ ഒരു ഘട്ടത്തിലേക്ക് മാറുന്നു. [5] ഡിഗ്രി സെന്റിഗ്രേഡിന് മുകളിൽ സംയുക്തം Na2O ആയി വിഘടിക്കുകയും O2 വിമുക്തമാക്കുകയും ചെയ്യുന്നു.[6]
2 Na2O2 → 2 Na2O + O2
നിർമ്മാണം
സോഡിയം ഹൈഡ്രോക്സൈഡിനെ ഹൈഡ്രജൻ പെറോക്സൈഡിനൊപ്പം സംസ്കരിച്ചാണ് ഒക്ടാഹൈഡ്രേറ്റ് നിർമ്മിക്കുന്നത്. [4]
130-200 ഡിഗ്രി സെന്റിഗ്രേഡിൽ സോഡിയം ഓക്സിജനുമായി പ്രതിപ്രവർത്തിപ്പിച്ച് വലിയ തോതിൽ സോഡിയം പെറോക്സൈഡ് തയ്യാറാക്കാം.: [5] [8]
- 4 Na + O2 → 2 Na2O
- 2 Na2O + O2 → 2 Na2O2
ഒരു പ്ലാറ്റിനം അല്ലെങ്കിൽ പലേഡിയം ട്യൂബിനുള്ളിൽ ഖര സോഡിയം അയോഡൈഡിന് മുകളിലൂടെ ഓസോൺ വാതകം കടത്തിവിടുന്നതിലൂടെയും ഇത് നിർമ്മിക്കപ്പെടാം. ഓസോൺ സോഡിയത്തെ ഓക്സിഡൈസ് ചെയ്ത് സോഡിയം പെറോക്സൈഡ് ഉണ്ടാക്കുന്നു. നേരിയ ചൂടാക്കൽ വഴി അയോഡിൻ ഉൽപ്പാദിപ്പിക്കാം. പ്ലാറ്റിനം അല്ലെങ്കിൽ പലേഡിയം പ്രതികരണത്തെ ഉത്തേജിപ്പിക്കുന്നു.
ഉപയോഗം
സോഡിയം പെറോക്സൈഡ് ജലവിശ്ലേഷണം നടത്തി സോഡിയം ഹൈഡ്രോക്സൈഡും ഹൈഡ്രജൻ പെറോക്സൈഡും പ്രതികരണത്തിനനുസരിച്ച് നൽകുന്നു [8]
- Na2O2 + 2 H2O → 2 NaOH + H2O2
കടലാസ്, തുണിത്തരങ്ങൾ എന്നിവയുടെ നിർമ്മാണത്തിനായി മരം പൾപ്പ് ബ്ലീച്ച് ചെയ്യാൻ സോഡിയം പെറോക്സൈഡ് ഉപയോഗിക്കുന്നു. വിവിധ അയിരുകളിൽ നിന്ന് ധാതുക്കൾ വേർതിരിച്ചെടുക്കാനുമുപയോഗിക്കുന്നു. സോഡിയം പെറോക്സൈഡ് ഒരു ഓക്സിഡൈസിംഗ് ഏജന്റായി ഉപയോഗിക്കുന്നു. ഓക്സിജനും സോഡിയം കാർബണേറ്റും ഉത്പാദിപ്പിക്കാൻ കാർബൺ ഡൈ ഓക്സൈഡുമായി പ്രതിപ്രവർത്തിച്ച് ഓക്സിജൻ ഉറവിടമായും ഇത് ഉപയോഗിക്കുന്നു:
- 2 Na2O2 + 2 CO2 → 2 Na2CO3 + O2
സ്കൂബ ഗിയർ, അന്തർവാഹിനികൾ മുതലായവയിൽ ഇത് പ്രത്യേകിച്ചും ഉപയോഗപ്രദമാണ്. ലിഥിയം പെറോക്സൈഡിനും പൊട്ടാസ്യം സൂപ്പർഓക്സൈഡിനും സമാനമായ ഉപയോഗങ്ങളുണ്ട്.