Լայմի հիվանդություն
Լայմի հիվանդություն, հայտնի է նաև, որպես Լայմի բորելիոզ, վարակիչ հիվանդություն է, որը հարուցվում է բորելիա բակտերիայով, որը տարածվում է տզերով[4]։ Վարակի ամենահաճախ հանդիպող նշանը մեծացող մակերեսով մաշկի կարմրությունն է, որը կոչվում է էրիթեմա միգրանս, որն առաջանում է տզի խայթոցի հատվածում, վերջինիս խայթելուց հետո մոտ 1 շաբաթ անց[5]։ Ցանը հիմնականում չքորվող է, անցավ[5]։ Վարակված անձանց 70-80%-ի մոտ զարգանում է ցան[5]։ Այլ վաղ հանդիպող նշաններից են տենդը, գլխացավը և հոգնածությունը[5]։ Եթե չբուժվեց, կարող են դիտվել դեմքի մեկ կամ երկու կեսերի շարժման անհնարինություն, հոդացավեր, պարանոցային կարկամությամբ ծանր գլխացավեր, սրտխփոց և այլն[5]։ Ամիսներ և տարիներ անց կարող են դիտվել հոդացավերի և հոդերի այտուցի կրկնվող դրվագներ[5]։ Երբեմն, կարող է դիտվել նաև ձեռքերի և ոտքերի սուր ցավեր կամ ծակծկոցներ[5]։ Չնայած բուժմանը, մոտ 10-20% դեպքերում հոդացավերը, հիշողության խնդիրները և հոգնածությունը պահպանվում են առնվազն 6 ամսվա ընթացքում[5][6]։
| Լայմի հիվանդություն | |
|---|---|
 | |
| Տեսակ | վարակիչ հիվանդություն |
| Պատճառ | B. burgdorferi? |
| Փոխանցման ձև | փոխանցում տզերի միջոցով, I. pacificus?[1] և I. scapularis?[1] |
| Հիվանդության ախտանշաններ | Քրոնիկական թափառող էրիթեմա[2], հոգնածություն[2], գլխացավ[2], Հոդացավ[2], միալգիա[2], թելիկախաղ[2], պարէսթեզիա[2], Գլխապտույտ[2], առիթմիա[2], Քրոնիկական նեյրոպաթիկ ցավ, տենդ, Նյարդաբորբ, մենինգիտ, մենինգոէնցեֆալիտ, Սրտամկանի բորբոքում, հոդաբորբ, encephalomyelitis? և հիպերտոիկ կարդիոմիոպատիա |
| Բուժաքննություն | western blot?[3], ֆիզիկալ զննում, ELISEA?, գոտկային պունկցիա և բիոպսիա |
| Բժշկական մասնագիտություն | վարակաբանություն, մաշկաբանություն, նյարդաբանություն և սրտաբանություն |
| ՀՄԴ-10 | A69.2 |
Լայմի հիվանդությունը մարդուն փոխանցվում է Իքսոդես ցեղին պատկանող վարակված տզի խայթոցից[7]։ ԱՄՆ-ում հանդիպող հիմնական տեսակը Ixodes scapularis-ն է, որը բակտերիայի տարածման համար մարդուն կպած պետք է լինի առնվազն 36 ժամ[8]։ Եվրոպայում Ixodes ricinus-ն ավելի արագ է տարածում բակտերիան[9][10]։ Հյուսիսային ամերիկայում հարուցիչը Borrelia burgdorferi -ն և Borrelia mayonii-ն են[4][11]։ Եվրոպայում և Ասիայում հիվանդությունը հարուցում են նաև Borrelia afzelii-ն և Borrelia garinii-ն[4]։ Հիվանդությունը չի փոխանցվում մարդուց մարդուն, այլ կենդանիներով կամ սննդի միջոցով[8]։ Ախտորոշումը հիմնված է ախտանշանների համակցման, տզի խայթելու պատմության և հնարավոր է նաև արյան մեջ սպեցիֆիկ հակամարմինների հայտնաբերման վրա[12][13]։ Հիվանդության վաղ փուլերում արյան հետազոտությունները հիմնականում բացասական են լինում[4]։ Առանձին տզերի հետազոտությունը այնքան էլ հարմար չէ ախտորոշման տեսանկյունից[14]։
Կանխարգելման համար պետք է զերծ մնալ տզի խայթոցից, օրինակ՝ ձեռքերը և ոտքերը ծածկող հատուկ հագուստ կրելով և դիէթիլտոլուամիդային հիմքով միջատասպաններ օգտագործելով[4]։ Պեստիցիդներով տզերի քանակի կրճատումը նույնպես արդյունավետ է[4]։ Տիզը կարելի է հեռացնել ունելիով[15]։ Եթե հեռացվող տիզը արյունով լցված է, վարակի առաջացման կանխարգելման համար կարելի է կիրառել 1 դեղաչափ դոքսիցիկլին, բայց քանի որ հիվանդության զարգացումը հազվադեպ է դիտվում, հիմնականում խորհուրդ չի տրվում[4]։ Հիվանդության զարգացման դեպքում կարելի է կիրառել մեծ քանակությամբ հակաբիոտիկներ, որոնք արդյունավետ են այս հիվանդության համար, ներառյալ՝ դոքսիցիկլինը, ամոքսիցիլինը և ցեֆուրոքսիմը[4]։ Ստանդարտ բուժումը տևում է երկուսից երեք շաբաթ[4]։ Որոշ մարդկանց մոտ բուժման ժամանակ դիտվում է տենդ, մկանային և հոդային ցավեր, որոնք անցնում են մեկ երկու օրվա ընթացքում[4]։ Մշտական ախտանշաններով հիվանդների մոտ երկարատև հակաբիոտիկային բուժումն անարդյունավետ է[4][16]։
Լայմի հիվանդությունը հյուսիսային կիսագնդում տզերով փոխանցվող ամենահաճախ հանդիպող հիվանդությունն է[17]։ Ըստ առկա տվյալների ԱՄՆ-ում տարեկան մոտ 300,000, իսկ եվրոպայում՝ մոտ 65,000 մարդ վարակվում է այս հիվանդությամբ[4][18]։ Վարակն առավել հաճախ հանդիպում է գարնանը և վաղ ամռանը[4]։ Որպես առանձին հիվանդություն, Լայմի հիվանդությունը առաջին անգամ ախտորոշվել է 1975թ․-ին Կոնեկտիկուտ նահանգի Հին Լայմում[19]։ Սկզբում հիվանդությունը ընդունում էին, որպես յուվենիլ ռևմատոիդ արթրիտ[19]։ Բակտերիան առաջին անգամ նկարագրվել է 1981թ․-ին Վիլլի Բուրգդորֆերի կողմից[20]։ Բուժումից հետո դիտվող քրոնիկական ախտանշանները ներառված են Լայմի հիվանդության հետբուժումային համախտանիշի մեջ (ԼՀՀԲՀ)[16]։ ԼՀՀԲՀ-ն տարբերվում է քրոնիկական Լայմի հիվանդությունից․ այս տերմինը այլևս չի ընդունվում գիտական հանրության կողմից սակայն որոշ խմբեր շարունակում են այն օգտագործել[16]։ Որոշ առողջապահության կազմակերպիչներ պնդում են, որ ԼՀՀԲՀ-ն պայմանավորված է պերսիստենտ վարակով, սակայն այս պնդումը հստակ չի կարող ապացուցվել, քանի որ ստանդարտ բուժումից հետո վարակիչ օրգանիզմների հայտնաբերումն անհնար է[21]։ ԱՄՆ-ում լայմի հիվանդության պատվաստանյութը վաճառքի հանվեց 1998-2002թթ․-ին, սակայն դուրս է մղվել շուկայից վատ վաճառքի պատճառով[4][22]։ Հետազոտություններ են կատարվում նոր պատվաստանյութ ստեղծելու համար[4]։
Նշաններ և ախտանիշներ
Լայմի հիվանդությունը կարող է ախտահարել տարբեր օրգան-համակարգեր և արտահայտվել բազմաթիվ ախտանշաններով։ Լայմի հիվանդությամբ ոչ բոլոր հիվանդների մոտ են դիտվող այս բոլոր ախտանշանները, և ախտանշաններից շատերը նույնիսկ սպեցիֆիկ չեն Լայմի հիվանդությանը և առավել բնորոշ են այլ հիվանդություններին։ Հիվանդության գաղտնի շրջանը սովորաբար մեկից երկու շաբաթ է, սակայն կարող է լինել ավելի կարճատև (օրեր) կամ երկարատև (ամիսներից մինչև տարիներ)[24]։
Ախտանշանները շատ հաճախ դրսևորվում են մայիսից սեպտեմբեր ընկած ամիսների ընթացքում, քանի որ հիվանդության համար պատասխանատու են տզերի հարսնյակային ձևերը[24]։ Առկա է նաև հիվանդության անախտանիշ ձևը, սակայն ԱՄՆ-ում հանդիպում է վարակվածների ավելի քիչ, քան 7%-ի մոտ[25]։ Անախտանիշ ձևերն առավել հաճախ դիտվում են եվրոպայում[26]։
Վաղ տեղայնացված վարակ
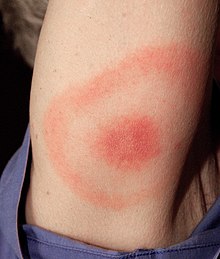
Վաղ տեղայնացված վարակը առաջանում է, երբ վարակը դեռ չի տարածվել մարմնով մեկ։ Ախտահարվում է միայն այն հատվածը, որտեղ եղել է վարակի մուտքի դուռը։ Լայմի հիվանդության վաղ տեղայնացված վարակի դասական նշանը շրջանաձև, դեպի դուրս տարածվող ցանն է, որն անվանվում է էրիթեմա միգրանս (ԷՄ), որն առաջանում է տզի խայթոցի հատվածում երեքից մինչև 32 օրվա ընթացքում[4]։ Ցանը կարմիր է, երբեմն տաք, բայց հիմնականում անցավ։ Դասականորեն, ցանի ներքին հատվածը լինում է մուգ կարմիր և հետո՝ պնդանում (ավելի հաստ և հստակ եզրերով), արտաքին եզրերը կարմիր են, իսկ նրանց միջև եղած հատվածը մաքրվում է․ ցանավորմանը տալով ցլան աչքի տեսք, այլ կերպ՝ թիրախային ախտահարում։ Այնուամենայնիվ, մասնակի մաքրումը հազվադեպ է լինում և ցլան աչքի կենտրոնական հատվածները կարմիր են մնում[4]։
Վաղ վարակի հետ ասոցացված ԷՄ ցանը դիտվում է վարակվածների մոտ 70-80% մոտ[5]։ Այն կարող է արտահայտվել ինչպես ցլան աչքի ձևով, այնպես էլ ոչ թիրախային ախտահարումներով։ Այդ 20-30%-ը ում մոտ բացակայում են դասական ցլան աչքի նշանը և ոչ թիրախային ախտահարումները դժվարությամբ են ախտորոշվում[27]։ Վարակվածների մոտ կարող են դիտվել նաև գրիպանման երևույթներ, ինչպես գլխացավը, մկանացավերը, տենդը և թուլությունը[28]։ Լայմի հիվանդությունը կարող է հարաճել ուշ ձևերի նույնիսկ առանց ցանի առաջացման[26][29]։
Վաղ դիսսեմինացված վարակ
Տեղային վարակի սկսվելուց հետո օրեր և շաբաթներ անց Բորելիա բակտերիաները կարող են տարածվել արյան շրջանառությամբ։ ԷՄ ցանավորումները կարող են առաջանալ մարմնի տարբեր հատվածներում, որոնք կապ չունեն տզի առաջնային մուտքի դռան հետ[30]։ Այլ մաշկային դրսևորումներից է բորելիալ լիմֆոցիտոման՝ մանուշակագույն գնդաձև գոյացություն ականջաբլթակի, պտուկի կամ փոշտի վրա, որը բացակայում է հյուսիսային Ամերիկայի հիվանդների մոտ, սակայն դիտվում է Եվրոպայում[31]։ Տարատեսակ սուր նյարդաբանական խանգարումները՝ նեյրոբորելիոզը, դիտվում են չբուժվածների 10-15%-ի մոտ[28][32]։ Դրանցից են դեմքի պարալիզը, որն իրենից ներկայացնում է դեմքի մեկ կամ երկու կողմերում մկանային լարվածության կորուստ և մենինգիտը, որը դրսևորվում է ծանր գլխացավերով, պարանոցային կարկամությամբ և լուսազգայնությամբ։ Ողնուղեղային նյարդերի արմատիկների բորբոքումը կարող է բերել սուր ցավերի, որոնք խանգարում են հիվանդի քունը և մաշկային ախտաբանական զգացողությունների առաջացման։ Թեթև էնցեֆալիտը կարող է բերել հիշողության կորստի, քնի խանգարումների կամ տրամադրութայն փոփոխությունների։ Որպես լրացում, որոշ հետազոտություններում նկարագրված է խանգարված մենտալ ստատուսը, որպես վաղ նեյրոբորելիոզի միակ ախտանիշ[33]։ Այս հիվանդությունը կարող է ախտահարել նաև սրտի հաղորդչական համակարգը, բերելով սրտի ռիթմի խանգարումների, ինչպես օրինակ՝ նախասիրտփորոքային պաշարումը[34]։
Ուշ դիսսեմինացված վարակ
Ամիսներ անց, չբուժված կամ անբավարար բուժում ստացած հիվանդների մոտ զարգանում են ծանր և քրոնիկական ախտանշաններ, որոնք առաջանում են մարմնի տարբեր հատվածների ախտահարման պատճառով, ներառյալ՝ գլխուղեղը, նյարդերը, աչքերը, հոդերը և սիրտը։ Խիստ հազվադեպ կարող են դիտվել հաշմանդամության բերող ախտանշաններ՝ շարժական կամ զգացող ֆունկցիաների կայուն խանգարումներ ստորին վերջույթներում[26]։ Լայմի հիվանդությամբ պայմանավորված ողնաշարից ճառագայթող նյարդային ցավերը ներառված են Բենուորթի համախտանիշի մեջ[35], որն անվանվել է Ալֆրեդ Բենուորթի պատվին։
Ուշ դիսսմենիացված փուլում վարակն ամբողջությամբ տարածված է օրգանիզմում։ Չբուժված հիվանդների մինչև 5%-ի մոտ դիտվում են քրոնիկական նյարդաբանական ախտանշաններ[28]։ Կարող է զարգանալ պոլինեյրոպաթիա, որն արտահայտվում է սուր ցավերով, թմրածությամբ և ձեռքերի ու ոտքերի ծակծկոցներով։ Լայմի էնցեֆալոպաթիան, որպես նյարդաբանական համախտանիշ արտահայտվում է նուրբ ճանաչողական խանգարումներով, անքնությամբ, ընդհանուր ինքնազգացողության վատացումով և անձնային փոփոխություններով[36]։ Այլ խանգարումներից դեպրեսիան և ֆիբրոմիալգիան, Լայմի հիվանդությամբ հիվանդների և ընդհանուր պոպուլյացիայի մոտ հանդիպում է նույն հաճախականությամբ[37][38]։
Քրոնիկական էնցեֆալոմիելիտը կարող է լինել հարաճող և ներառել ճանաչողական խանգարումներ, գիտակցության մթագնում, միգրեն, հավասարակշռության խանգարումներ, ոտքերի թուլություն, տարօրինակ քայլվածք, դեմքի պարալիզ, խնդիրներ միզապարկի հետ, գլխապտույտ և մեջքի ցավեր։ Հազվադեպ, չբուժված Լայմի հիվանդությունը կարող է բերել հասարակ փսիխոզի, որը հաճախ շփոթվում է շիզոֆրենիայի կամ երկբևեռ խանգարման հետ։ Կարող են դիտվել նաև խուճապի գրոհներ, տագնապ, ինչպես նաև սոմատոֆորմ պատրանքներ, որոնք կարող են արտահայտվել դեպերսոնալիզացիայի և դեռեալիզացիայի համախտանիշներով, երբ բուժառուները ունենում են սեփական անձից կամ իրականությունից կտրվելու զգացողություն[39][40]։
Բազմաթիվ հետազոտություններում նյարդաբանական ախտանշաններով հիվանդների և՛ ուղեղաթաղանթներից, և՛ ուղեղանյութից անջատվել են Լայմի հիվանդության հարուցիչները՝ Borrelia burgdorferi[41]։
Լայմի արթրիտի ժամանակ հիմնականում ախտահարվում են ծնկները[42]։ Ավելի հազվադեպ կարող են ախտահարվել նաև այլ հոդեր, ներառյալ՝ ոտնաթաթի, արմնկային, դաստակային, կոնքային և ուսային հոդերը։ Ցավը հիմնականում թեթև կամ միջին ծանրության է, հաճախ ախտահարված հոդի այտուցով։ Կարող են առաջանալ և պատռվել Բեյկերի բշտեր։ Որոշ դեպքերում զարգանում է հոդի էռոզիաներ։
Քրոնիկական ապաճական ակրոդերմատիտը (ՔԱԱ) քրոնիկական մաշկային հիվանդություն, որն առաջին անգամ հայտնաբերվել է մեծահասակների մոտ Եվրոպայում[31]։ ՔԱԱ-ն սկսվում է գունափոխված մաշկի կարմրակապտավուն բծերով, հաճախ ձեռքերի և ոտքերի մեջքային մակերեսներին։ Մի քանի շաբաթվա կամ ամսվա ընթացքում մաշկի ախտահարված մասերը ենթարկվում են ապաճի, դարձնելով մաշկը սկզբից բարակ և կնճռոտված, իսկ հետո, եթե չբուժվեց, խիստ չորացած և մազազուրկ[43]։
Պատճառներ



Լայմի հիվանդությունը հարուցվում է սպիրոխետներին՝ պարուրաձև բակտերիաներին պատկանող Բորելիա ցեղի ներկայացուցիչներով։ Սպիրոխետներն ունեն գրամ բացասական բակտերիաների թաղանթներին նմանվող բջջաթաղանթ, շրջապատված պեպտիդոգլիկանով և մտրակներով։ Սպիրոխետներն իրենց երկթաղանթ ծածկով պայմանավորված, հաճախ շփոթմամբ ներառվում են գրամ բացասական բակտերիաների մեջ, չնայած թաղանթային կառուցվածքում հստակ տարբերությունների առկայությանը[44]։ Լայմի հետ ասոցացվող Բորելիաները հայտնի են, որպես Borrelia burgdorferi sensu lato և ունեն նկատելի գենետիկական տարբերություններ։
B. burgdorferi sensu lato -ն ներառում է մինչև 21 մոտ գտնվող տեսակներ, բայց նրանցից երեքն են հստակ առաջացնում Լայմի հիվանդություն՝ B. burgdorferi sensu stricto (գերակշռում է հյուսիսային Ամերիկայում, բայց առկա է նաև Եվրոպայում), B. afzelii և B. garinii (երկուսն էլ գերակշռում են Եվրասիայում)[45][46]։ Ըստ որոշ հետազոտությունների B. bissettii-ն և B. valaisiana-ն նույնպես կարող են վարակել մարդկանց, բայց այս տեսակներին հիվանդության հարուցման տեսանկյունից կարևորություն չի տրվում[47]>[48]։
Փոխանցում
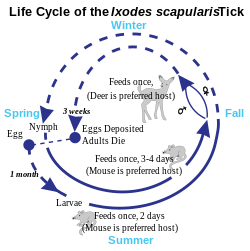
Լայմի հիվանդությունը համարվում է զոոնոզ հիվանդություն, քանի որ մարդուն հիվանդությունը փոխանցվում է բնական ռեզերվուարներից՝ փոքր կաթնասուններից և թռչուններից տզերի միջոցով, եթե այն սնվում է երկու տերերի արյունով[49]։ Ամրակազմ Ixodes ցեղի տզերը հիվանդության հիմնական փոխանցողներն են (կարող են փոխանցել նաև Բաբեզիաներ)[50]։ Վարակների մեծ մասը փոխանցվում են տզերի հարսնյակային ձևերով, քանի որ դրանք շատ փոքր են և երկար ժամանակ առանց երևալու կարող են սնվել արյունով[49]։ ԱՄՆ, Նյու Ջերսիում տզերի հարսնյակային ձևերն ունեն կակաչի սերմերի չափեր և, երբեմն, մուգ գլուխ և թափանցիկ մարմին[51] (տզերի թրթուրների ամենաերիտասարդ ձևերը հազվադեպ են վարակվում[52])։ Չնայած հասուն եղնիկի տզերի համար ցանկալի տերը եղնիկներն են, և եղնիկների բացակայության պայմաններում տզերի պոպուլյացիան նվազում է, տզերը հիմնականում չեն վարակվում բորելիաներով եղնիկից, հակառակը՝ նրանք ստանում են բորելիաները վարակված մանր կաթնասուններից, ինչպես օրինակ՝ սպիտակաոտ մկներից, և երբեմն թռչուններից[53]։
Տզի միջնաղում, բորելիայի արտաքին մակերեսային սպիտակուց Ա-ն (OspA) կապվում է տզի OspA-ի ընկալչին՝ TROSPA-ին։ Երբ տիզը սնվում է, բորելիաները նվազեցնում են OspA-ն և ավելացնում OspC: Երբ բակտերիաներն անցնում են միջնաղուց թքագեղձերի մեջ, OspC-ն կապվում է Salp15-ին․ վերջինս թքի մեջ առկա սպիտակուց է, որն ունի իմունաճնշիչ ազդեցություններ, որը խթանում է վարակի զարգացումը[54]։ Կաթնասուն տիրոջ մոտ վարակի արտահայտվածությունը կախված է բակտերիայի կողմից OspC-ի էքսպրեսիայից[55]։
Տզերի խայթոցները հաճախ չեն երևում, պայմանավորված հարսնյակային փուլում տզերի փոքր չափերով, ինչպես նաև տզի արտազատած նյութերով, որոնք կանխում են տիրոջ մոտ քորի կամ ցավի առաջացումը։ Այնուամենայնիվ, հիվանդության փոխանցումը հազվադեպ է․ տզերի խայթոցներից միայն 1% դեպքերում է փոխանցվում Լայմի հիվանդությունը։
Եվրոպայում հիվանդության փոխանցողը Ixodes ricinus, որը կոչվում է նաև ոչխարի տիզ կամ գերչակի տիզ[56]։ Չինաստանում Ixodes persulcatus (տայգայի տիզ) ամենահաճախ հանդիպող փոխանցողն է[57]։ Հյուսիսային ամերիկայում սևաոտ տիզը կամ եղնիկի տիզ (Ixodes scapularis) ամենահաճախն են հանդիպում, հատկապես արևելյան հատվածներում[52]։
Միայնակ աստղի տիզը (Amblyomma americanum), որը հայտնաբերվում է ԱՄՆ-ի հարավարևելյան հատվածներում՝ Տեքսասից դեպի արևմուտք, չի կարող փոխանցել սպիրոխետներով հարուցված Լայմի հիվանդությունը[58], սակայն այն կարող է կապված լինել հարավային տզերով ասոցացված ցանային հիվանդության հետ, որը կլինիկորեն նմանվում է Լայմի հիվանդության թեթև ձևին[59]։
ԱՄՆ-ի արևմտյան հատվածներում, հիվանդության հիմնական փոխանցողը արևմտյան սևաոտ տիզն է (Ixodes pacificus)[60]։ Այս տզերի հակվածությունը սնվելու այնպիսի կենդանիներով, ինչպիսիք մողեսներն են, որոնք կայուն են բորելիաների նկատմամբ, պայմանավորում են հիվանդության տարածվածության նվազմանը արևմուտքում[61][62]։
Հիվանդությունը կարող է փոխանցվել մորից պտղին ընկերքի միջոցով, և, ինչպես այլ սպիրոխետոզների ժամանակ, հղիության վատ հետևանքները առավել հաճախ կարող են դիտվել չբուժված հիվանդների մոտ․ արագ անցկացվող հակաբիոտիկային բուժումը նվազեցնում կամ վերացնում է ռիսկը[63][64][65][66][67]։
Չնայած Լայմի սպիրոխետները հայտնաբերվում են միջատների մոտ, հատկապես տզերի[68], վարակի փոխանցումը հազվադեպ երևույթ է[69]։ Լայմի սպիրոխետի ԴՆԹ-ն հայտնաբերվել է սերմնահեղուկի[70] և կրծքի կաթի մեջ[71]։ Այնուամենայնիվ, ըստ հիվանդությունների վերահսկման կենտրոնի, կենդանի սպիրոխետները չեն հայտնաբերվում կրծքի կաթի, սերմնահեղուկի կամ մեզի մեջ, հետևաբար այս հիվանդությունը սեռական ճանապարհով չի փոխանցվում[72]։
Տզերով զուգահեռ փոխանցվող վարակներ
Տզերը, որոնք փոխանցում են B. burgdorferi, զուգահեռ կարող են կրել և փոխանցել նաև այլ մակաբույծներ, ինչպես օրինակ՝ Theileria microti և Anaplasma phagocytophilum, որոնք փոխանցում են համապատասխանաբար բաբեշիոզ և մարդու գրանուլոցիտար անապլազմոզ (ՄԳԱ)[73]։ Կախված աշխարհագրական տեղակայումից, վաղ շրջանում Լայմի հիվանդությամբ պացիենտներից 2-12%-ի մոտ կարող են դիտվել նաև ՄԳԱ, իսկ 2-40%-ի մոտ՝ բաբեշիոզ[74]։ Այնպիսի շրջաններում, ինչպես Բալտիկ ծովի արևելյան հողերն են, զուգահեռ կարող է փոխանցվել տզային էնցեֆալիտ[75]։
Զուգահեռ ընթացող վարակները բարդացնում են Լայմի հիվանդության ախտանշանները, ախտորոշումն ու բուժումը։ Հնարավոր է, որ տիզը փոխանցի վերոնշյալ Լայմին զուգահեռ վարակները առանց բորելիաների, դարձնելով ախտորոշումը առավել բարդ։ Հիվանդությունների վերահսկման և կանխարգելման կենտրոնը հետազոտել է Նյու Ջերսիի գյուղական հատվածներից 100 տզեր և հայտնաբերել, որ 55%-ի մոտ առկա է առնվազն մեկ ախտածին պաթոգեն[76]։
Ախտաֆիզիոլոգիա
Հիվանդության ընթացքում B. burgdorferi-ն կարող է տարածվել օրգանիզմով մեկ և հայտնաբերվել է մաշկի, սրտի, հոդերի, ծայրամասային և կենտրոնական նյարդային համակարգի մեջ[55][77]։ Լայմի հիվանդության ժամանակ դիտվող տարբեր նշաններ և ախտանշաններ սպիրոխետների դեմ տարվող իմուն պատասխանի արդյունք են[28]։
B. burgdorferi ներմուծվում է մաշկի մեջ վարակված Ixodes տզերի խայթոցից։ Տզերի թուքը, որով սպիրոխետների սնվելու ընթացքում շաղախվում է վերքը, պարունակում է նյութեր, որոնք ընկճում են տեղային իմունիտետը[78]։ Սա ապահովում է պաշտպանական միջավայր սպիրոխետի գոյության համար։ Սպիրոխետները բազմանում և տեղային ձևով տարածվում են բուն մաշկում։ Մաշկի ներսում տիրոջ նկատմամբ զարգացող բորբոքային պատասխանը պատճառ է դառնում բնորոշ շրջանաձև ԷՄ-ի առաջացման[55]։ Նեյտրոֆիլները, որոնք պետք է հեռացնեին սպիրոխետներին մաշկային հյուսվածքից, չեն կարողանում անել դա։ Սա պայմաններ է ստեղծում բակտերիայի գոյատևման և տարածման համար[79]։
Տզի խայթոցից օրեր և շաբաթներ անց սպիրոխետները հայտնաբերվում են արյան մեջ և տարածվում դեպի հոդեր, սիրտ, նյարդային համակարգ և մաշկի ավելի հեռու հատվածներ, որտեղ վերջիններիս առկայությամբ պայմանավորված դրսևորվում են հիվանդության դիսսեմինացված ձևի տարբեր ախտանշանները։ B. burgdorferi -ի տարածումը օրգանիզմով մեկ պայմանավորված է իրենց մակերեսի վրա տիրոջ օրգանիզմի պրոտեազներից մեկի՝ պլազմինի կապումով[80]։
Առանց բուժման բակտերիաները կարող են պերսիստել օրգանիզմում ամիսներ և նույնիսկ տարիներ շարունակ, չնայած իմուն համակարգի կողմից հակասպիրոխետային հակամարմինների արտադրությանը[81]։ Սպիրոխետներն ունեն հնարավորություն խուսափելու իմուն պատասխանից պայմանավորված մակերեսային սպիտակուցների էքսպրեսիայի նվազեցումով, որոնք համարվում են հակամարմինների թիրախներ, VlsE մակերեսային սպիտակուցի հակածնային տարբերակներով, իմուն համակարգի հիմնական օղակների, օրինակ՝ կոմպլեմենտի ինակտիվացումով և արտաբջջային մատրիքսում նրանց պաղկվելով, ինչի արդյունքում իմունային որոշ գործոններ չեն աշխատում[82][83]։
Գլխուղեղում B. burgdorferi-ն առաջացնում է աստրոգլիոզ (պրոլիֆերացիա ապոպտոզից հետո), որը կարող է բերել նեյրոդիսֆունկցիայի[84]։ Սպիրոխետները խթանում են նաև տիրոջ բջիջների կողմից խինոլինաթթվի արտադրությունը, ինչը խթանում է նյարդային բջիջների NMDA ընկալիչները, պատճառ դառնալով հոգնածության, թուլության առաջացման, որը դիտվում է Լայմի էնցեֆալոպաթիայի ժամանակ[85]։ Որպես լրացում, սպիտակ նյութի տարածուն ախտահարումը Լայմի էնցեֆալոպաթիայի ժամանակ կարող է բերել գորշ նյութում նեյրոնալ կապերի խախտման, ինչի հետևանքով կարող է դիտվել ուշադրության, հիշողության, տեսատարածական հնարավորությունների, կոմպլեքսային ճանաչման և հուզական վիճակի դեֆիցիտի։ Սպիտակի նյութի ախտահարումն ունի վերականգման ավելի մեծ պոտենցիալ, քան գորշ նյութի ախտահարումը, իհարկե պայմանավորված նեյրոնային կորստի ավելի հազվադեպ զարգացումով։ ՄՌՇ հետազոտությամբ հայտնաբերվող հիպերինտենս սպիտակ նյութի օջախները վերանում են հակաբիոտիկային բուժումից հետո[86]։
Տրիպոտոֆանի՝ սերոտոնինի նախորդի քանակը ԿՆՀ-ում իջնում է տարբեր վարակիչ հիվանդությունների, ներառյալ՝ Լայմի հիվանդության ժամանակ[87]։ Հետազոտողներն ուսումնասիրում են այս նյարդահորմոնի արտազատման փոփոխությունները, որպես բորելիոզով որոշ հիվանդների նյարդահոգեբուժական խանգարումների առաջացման պատճառ[88]։
Իմունաբանական հետազոտություններ
Լայմի հիվանդության ժամանակ օրգանիզմի վրա բորելիաների ազդեցությունը բերում է երկարատև և օրգանիզմին վնասող բորբոքային պատասխանի[89], որը պաթոգենով խթանված աուտոիմուն հիվանդության ձև է[90]։ Այս պատասխանի առաջացումը կարող է պայմանավորված լինել մոլեկուլային միմիկրիայով, երբ բորելիաները խուսափում են իմուն համակարգի ազդեցությունից՝ նմանակելով օրգանիզմի նորմալ հյուսվածքների հակածիններին[91][92]։
Աուտոիմուն ռեակցիայի քրոնիկական ախտանշանները կարող են պատասխանել այն հարցին, թե ինչու օրգանիզմից սպիրոխետների հեռացումից հետո որոշ ախտանշաններ պահպանվում են։ Այս տեսությունը կարող է բացատրել հակաբիոտիկային բուժումից հետո քրոնիկական արթրիտի պահպանումը, ինչպես օրինակ՝ ռևմատիզմի ժամանակ է, բայց վերջինիս համընդհանուր ընդունումը կասկածելի է[93][94]։
Ախտորոշում
Լայմի հիվանդության ախտորոշումը հիմնված է կլինիկական ախտանշանների, օբյեկտիվ ֆիզիկալ նշանների (օրինակ՝ ԷՄ, դիմային պարալիզ կամ արթրիտ) կամ վարակված տզերի հնարավոր խայթման, ինչպես նաև արյան շճաբանական հետազոտությունների վրա։ ԷՄ ցանը ոչ միշտ է ցլան աչքի տեսքով, երբեմն դիտվում է պարզապես ընդհանուր կարմրություն։ Ախտորոշման հստակեցման ժամանակ առողջապահության կազմակերպիչները պետք է դիտարկեն նաև նմանատիպ դրևորումներով ուղեկցվող այլ հիվանդությունների հնարավորությունը։ Լայմի հիվանդությամբ ոչ բոլոր հիվանդներն են ունենում ցլան աչքի ցանը, իսկ շատերը չեն նշում նույնիսկ տզի խայթոց[95]։
Պայմանավորված լաբորատորիաներում բորելիաների ցանքսի դժվարությամբ, Լայմի հիվանդության ախտորոշումը հիմնվում է կլինիկական հետազոտությամբ հայտնաբերված նշանների և Լայմի էնդեմիկ շրջաններում գտնվելու պատմության վրա[50]։ ԷՄ ցանը, որը միշտ չէ, որ հայտնաբերվում է, բավարար նշան է ախտորոշման հստակեցման համար, նույնիսկ շճաբանական թեստերի բացասական լինելու դեպքում[96][97]։ Շճաբանական թեստերը կարող են օգնել ախտորոշմանը կասկածելի դեպքերում, բայց ախտորոշման չափանիշ չէ[50]։
Ուշ փուլերում Լայմի հիվանդության ախտորոշումը բավականին բարդ է, պայմանավորված բազմազան ախտանշաններով և ոչ սպեցիֆիկ նշաններով, ինչն էլ պատճառ է հանդիսացել հետազոտողներից մեկի կողմից հիվանդությունը անվանել «գերագույն նմանակող»[98]։ Լայմի հիվանդությունը կարելի է շփոթել ցրված սկլերոզի, ռևմատոիդ արթրիտի, ֆիբրոմիալգիայի, քրոնիկական հոգնածության համախտանիշի, գայլախտի, Կրոնի հիվանդության, ՄԻԱՎ-ի և այլ աուտոիմուն և նեյրոդեգեներատիվ հիվանդությունների հետ։ Քանի որ ուշ փուլերում բոլոր հիվանդների մոտ հակամարմնային թեստը դրական է, հասարակ արյան հետազոտությամբ կարելի է բացառել կամ հաստատել Լայմի հիվանդությունը[99]։
Լաբորատոր հետազոտություններ
Գոյություն ունեն Լայմի հիվանդության լաբորատոր ախտորոշման բազմաթիվ հետազոտություններ, սակայն դրանցից որոշները վավերացված չեն։ Ամենահաճախ կիրառվող հետազոտությունը շճաբանականն է, որի միջոցով որոշում են արյան մեջ սպեցիֆիկ հակամարմինների առկայությունը։ Այս հետազոտությունները կարող են բացասական լինել հիվանդության սկզբնական շրջաններում, քանի որ օրգանիզմը դեռ չի արտադրել բավարար քանակությամբ հակամարմիններ, սակայն այս հետազոտությունը վստահելի է Լայմի ուշ փուլերում[100]։ Լայմի հիվանդության անբավարար ախտանշաններով հիվանդների շճաբանական հետազոտությունը այնքան էլ նպատակահարմար չէ, քանի որ բարձր են կեղծ դրական արդյունքների հավանականությունը և ծախսը[101]։
Շճաբանական լաբորատոր հետազոտություններից ամենահասանելի և կիրառվող թեստերը Վեսթերն բլոտը և ELISA-ն են։ Հիվանդությունների վերահսկման և կանխարգելման կենտրոնը խորհուրդ է տալիս հետևյալ ուղեցույցը՝ առաջինը կիրառվում է զգայուն ELISA-ն, եթե վերջինս դրական է կամ կասկածելի՝ կիրառվում է սպեցիֆիկ Վեսթերն բլոտը[102]։ Ախտորոշման համար թեստերի վստահելիությունը վիճելի է[50]։ Հետազոտությունները ցույց են տվել, որ IgM Վեսթերն բլոտն ունի 94-96% սպեցիֆիկություն վաղ փուլի Լայմի հիվանդության ախտանիշներով հիվանդների մոտ[103][104]։ Սկզբնական ELISA-ն ունի մոտ 70% զգայունություն, իսկ վերջինիս ուղեցույցային կիրառման դեպքում ընդհանուր զգայունությունը 64% է, բայց վերջինիս զգայունությունը դիսսեմինացված ձևերի (օրինակ՝ արթրիտի) դեպքում հասնում է 100%-ի[105]։
Թեստային սխալ արդյունքներ նկարագրվել են ինչպես վաղ, այնպես էլ ուշ փուլերի հիվանդության դեպքում և կարող են պայմանավորված լինել տարբեր գործոններով, ներառյալ խաչաձև հակամարմնային ռեակցիաները այլ վարակների, ինչպես օրինակ՝ Էպշտեյն-Բարի, ցիտոմեգալովիրուսի[106] և հասարակ հերպեսի վիրուսի հետ[107]։ Վարակի վաղ փուլերում Կեղծ դրականների ընդհանուր հաճախականությունը ցածր է, մոտ 1-3%, ի համեմատ կեղծ բացասականների՝ մինչև 36%[105]։
Պոլիմերազային շղթայական ռեակցիան (ՊՇՌ) նույնպես կարող է կիրառվել Լայմի հիվանդության ախտորոշման համար, հայտնաբերելով Լայմի սպիրխետի ժառանգական նյութը (ԴՆԹ)։ ՊՇՌ հետազոտությունը հակում ունի կեղծ դրական արդյունքների, պայմանավորված վատ լաբորատոր հմտություններով[108]։ Նույնիսկ ամբողջությամբ ճիշտ կատարված աշխատանքի դեպքում ՊՇՌ-ն երբեմն տալիս կեղծ բացասական արդյունքներ արյան և ուղեղ-ողնուղեղային հեղուկի կենսանյութերի հետ[109]։ Հետևաբար ՊՇՌ-ն լայնորեն չի կիրառվում Լայմի հիվանդությունը ախտորոշելու համար, բայց կարող է օգնել Լայմի արթրիտի ախտորոշման գործում, քանի որ այն ունի շատ բարձր զգայունություն ձուսպահեղուկում ospA ԴՆԹ-ի հայտնաբերման համար[110]։
Ցանքսը և ՊՇՌ-ն այն հիմնական մեթոդներն են, որոնց միջոցով հայտնաբերում ենք օրգանիզմները, այն դեպքում, երբ շճաբանական թեստերը հայտնաբերում են միայն բորելիաների նկատմամբ առաջող հակամարմինները։ Բորելիաներն անջատում են OspA հակածիններ, որոնց որոշումը մեզում խոստումնալից հետազոտություն է[111]։ Նանոթակարդները կիրառվում եմ OspA-ների հայտնաբերման համար[112][113]։ Բորելիաների հակածինների նկատմամբ իմունոգլոբուլին G-ի և M-ի բարձր տիտրերի հայտնաբերումը վկայում է վարակի մասին, իսկ ցածր տիտրերը այնքան էլ վստահելի չեն, քանի որ IgM հակամարմինները հայտնաբերվում են վարակի սկզբնական շրջանում, իսկ IgG-ն կարող է պահպանվել տարիներով[114]։
Վեստերն բլոտի, ELISA-ի, ՊՇՌ-ի համար կիրառվում են ինչպես երակային արյունը, այնպես էլ ուղեղ-ողնուղեղային հեղուկ։ Չնայած գոտկային պունկցիան ավելի նշանակալի է ախտորոշման համար, հակածնի հայտնաբերումը ուղեղ-ողնուղեղային հեղուկում բավականին դժվար է․ դա է պատճառը, որ ուղեղ-ողնուղեղային հեղուկում մանրէի հայտնաբերումը դիտվում է ախտահարվածների միայն 10-30%-ի մոտ։ Նեյրոբորելիոզի ախտորոշումը պետք չէ բացառել միայն նորմալ ուղեղ-ողնուղեղային հեղուկի կամ բացասական շճաբանական հետազոտության պատասխանի միջոցով[115]։
Բորելիայի ախտորոշման համար ստեղծվում են նոր մեթոդներ, ինչպես օրինակ՝ LTT-MELISA-ն[116]>, սակայն այս հետազոտության արդյունքները հակասական են։ Առաջին հետազոտությունը, որն ուսումնասիրել է այդ թեստի զգայունությունը և սպեցիֆիկությունը, ներկայացվել է 2012թ․-ին և հնարավոր է հետագայում դառնալ օժանդակող ախտորոշիչ մեթոդ[117]։ 2014թ․-ին LTT-MELISA-ի հետազոտությունը եզրակացրեց, որ այս թեստը բավարար զգայունություն ունի, որպեսզի ներառվի Եվրոպական-Լայմի հիվանդության ախտորոշման ուղեցույցի մեջ[118]։ Այլ ախտորոշիչ մեթոդներից օրինակ՝ focus floating microscopy-ին հետազոտությունների փուլում են[119]։ Նոր հետազոտության համաձայն CXCL13 քեմոկինը կարող է լինել նեյրոբորելիոզի մարկեր[120]։
Որոշ լաբորատորիաների կողմի ներկայացված նոր մեթոդներ բավարար ճշգրտություն չունենալու պատճառով չեն կիրառվում։ Այս թեստերից են՝ մեզում հակածինների որոշումը, մեզի ՊՇՌ-ն, B. burgdorferi-ի առանց բջջաթաղանթի ձևերի իմունաֆլուորեսցենտային ներկումը և լիմֆոցիտային փոխակերպման թեստերը։ Հիվանդությունների վերահսկման կենտրոնը հորդորում է հնարավորինս խուսափել կամ ընդհանրապես չկիրառել այս թեստերը[109]։
Տեսապատկերում
Հակասական է նեյրոբորելիոզի ժամանակ նյարդատեսապատկերման սպեցիֆիկ նշանների առկայությունը, սակայն այն կարող է օգտագործել տարբերակիչ ախտորոշման և հիվանդության ախտաֆիզիոլոգիայի պատկերացման համար[121]։ Չնայած հակասական փաստերին, այնուամենայնիվ կան տվյալներ հիվանդության ախտորոշման հարցում վերջինիս օգտակարության մասին։ Մագնիսառեզոնանսային շերտագրությունը (ՄՌՇ) և մեկ-ֆոտոնային էմիսիոն համակարգչային շերտագրությունը (SPECT) Լայմի հիվանդությամբ հիվանդների գլխուղեղում փոփոխությունները հայտնաբերող երկու հիմնական թեստերն են։ Նյարդատեսապատկերմամբ հայտնաբերվում են հարփորոքային սպիտակ նյութի ախտահարումներ, ինչպես նաև փորոքների մեծացում և կեղևային ապաճ։ Այս փոփոխությունները ժամանակավոր են և դարձելի, քանի որ անցնում են հակաբիոտիկային բուժումից հետո։ SPECT-ով արված պատկերներում հայտնաբերվել են կեղևի և ենթակեղևային սպիտակ նյութի անբավարար արյունամատակարարման նշաններ։ Այնուամենայնիվ, SPECT պատկերները ոչ սպեցիֆիկ են, քանի որ դիտվում են հետերոգեն նշաններ։ SPECT պատկերները նեյրոբորելիոզի ժամանակ շատ նման են այն պատկերներին, որոնք դիտվում են Կրեյցֆելդտ-Յակոբի հիվանդության և ուղեղի դատարկ օջախների հատվածներում, ինչը հակասական է դարձնում նաև SPECT-ի կիրառումը[122]։
Կանխարգելում
Պաշտպանիչ հագուստներն են՝ գլխարկը, երկարաթև վերնաշապիկը և երկար տաբատը, որի եզրերը անցկացվում է գուլպաների կամ կոշիկի մեջ։ Բաց գույնի հագուստը տզին ավելի տեսանելի է դարձնում, թույլ տալով հայտնաբերելով այն մինչև մարմնին կպնելը։ Մարդիկ պետք է հատուկ խնամք տանեն ընտանի կենդանիների նկատմամբ՝ կախված նրանց տուն թողնելու հետ, քանի որ նրանք կարող են բերել տզերը տուն։ Փայտի, թփերի, թափված տերևների և բարձր խոտածածկույթի հետ աշխատող անձինք ունեն աշխատանքային պայմաններում Լայմի հիվանդությամբ վարակվելու բարձր ռիսկ։ Գործատուները պետք է փորձեն կանխել աշխատողների վարակումը հատուկ սանիտարալուսավորչական աշխատանքների միջոցով, կապված Լայմի հիվանդության փոխանցման և վարակման ռիսկի հետ, և սովորեցնեն ինքնուրույն հայտնաբերել տզերին աճուկային, անութափոսային հատվածներում և մազերի մեջ։ Ռիսկային գոտիներում աշխատողների աշխատանքային հագուստը պետք է լվացվի տաք ջրում և չորացվի տաք չորանոցում՝ տզերին ոչնչացնելու համար[123]։
Հագուստի վրա ցանված պերմեթրինը սպանում է շփման մեջ գտնվող տզերին և վաճառվում է այդ նպատակով։ Ըստ հիվանդությունների վերահսկման կենտրոնի, միայն դիէթիլտոլուամիդներ են արդյունավետ կերպով վերացնում տզերին[124]։
Կենդանի տերեր
Լայմի և այլ եղնիկների տզերով փոխանցվող հիվանդությունների հաճախականությունը կարելի է նվազեցել՝ մեծապես նվազեցնելով եղնիկների պոպուլյացիան, որոնցից սննդային և վերարտադրողական կախվածության մեջ են գտնվում հասուն տզերը։ Լայմի դեպքերը կտրուկ նվազել են Մեյնի Մոնհեգան կղզում եղնիկների ոչնչացումից հետո[125], և դրան հետևող Կոնեկտիկուտի Մամֆորդ Կոուվի շրջանում եղնիկների վերահսկողությունից հետո[126]։ Պետք է նշել նաև, որ եղնիկների ոչնչացումը երբեմն կարող է բերել տզերի խտության ժամանակավոր աճի[127]։
Որպես օրինակ՝ ԱՄՆ-ում եղնիկների պոպուլյացիայի նվազեցումը մինչև 8-10 եղնիկ քառակուսի մղոնում (Լայմի հիվանդության մեծ տարածումով երկրներում ավելի քան 60 եղնիկ քառակուսի մղոնում) կարող է նվազեցնել տզերի քանակը և Լայմի կամ այլ տզերով փոխանցվող վարակների տարածումը[128]։ Այնուամենայնիվ, այսպիսի կտրուկ նվազեցումը շատ շրջաններում բավական դժվար է ապահովել, և եղնիկների կամ այլ մեծ կաթնասուն տերերի ցածր կամ միջին խտությունը շարունակում է սնել հասուն տզերին, որպեսզի ապահովվի թրթուրների բարձր խտություն։ Ընտանի, այդ թվում գյուղատնտեսական կենդանիների հասարակ անասնաբուժական հսկողությունը ակարիցիդների կիրառումով, կարող է բերել տզերի կողմից մարդկանց վարակվածության նվազման։
Տզերի խայթոցից խուսափելու համար պետք է կիրառվեն տարբեր միջատասպան միջոցներ, օրինակ՝ դիէթիլտոլուամիդային հիմքի նյութեր։ Դիէթիլտոլուամիդային միջատասպանները համարվում են տզերի խայթոցից խուսափելու միջին արդյունավետության միջոցներ[129]։
Եվրոպայում Borrelia burgdorferi-ի հայտնի բնական շտեմարանները 9 փոքր կաթնասուն, 7 միջին չափի և 16 թռչունների տեսակներ են (ներառյալ ճնճղուկանմաններ, ծովային թռչուններ և փասյաններ)[130]։ Այս կենդանիներիը փոխանցում են սպիրոխետները տզերին մասնակցելով եվրոպայում B. burgdorferi-ի բնական շրջանառությանը։ Կա կարծիք նաև տնային մկան և այլ փոքր կրծողների դերի մասին, հատկապես արևելյան Եվրոպայում և Ռուսաստանում[130]։ «Պաթոգենների ամենամեծ քանակը պարունակող շտեմարանը եվրոպական այծյամն է՝ Capreolus capreolus-ը[131]․ «այս տեսակը կարծես թե ամենամեծ շտեմարանը չէ B. burgdorferi-ի համար»,- կարծում է Ջենսոնը և այլք (1992թ․)[132] (անհամապատասխան տեր է B. burgdorferi-ի և TBE վիրուսի համար), բայց այն կարևոր դեր ունի տզերի սնուցման հարցում[133], ինչպես կարմիր եղնիկը և վայրի վարազները (Sus scrofa)[134], որոնցում հայտնաբերվել է մեկ ռիկետսիա և երեք բորելիա[131]» կոինֆեկցիայի բարձր ռիսկով՝ այծյամների պարագայում[135]։ Այնուամենայնիվ, 2000-ականներին եվրոպայի այծյամներում հայտնաբերվել է երկու տեսակի ռիկետսիա և երկու տեսակի բորելիա[134]։
Պատվաստում
Լայմի հիվանդության դեմ կիրառվող ռեկոմբինանտ պատվաստանյութը ստեղծվել է հարուցչի արտաքին մակերեսային սպիտակուց A-ի հիմքով (ospA) ՍմիթԿլայն Բիչամի կողմից։ Ավելի քան 10,000 մարդ ներառող կլինիկական հետազոտություններում LYMErix կոչվող պատվաստանյութը ապահովել է մեծահասակների համար 76%, երեխաների համար 100% պաշտպանական իմունիտետ Բորելիայի նկատմակբ միայն թեթև կամ միջին և անցողիկ կողմնակի երևույթներով[136]։ 1998թ․-ի դեկտեմբերի 21-ին սննդի և դեղերի վերահսկման վարչությունը հաստատեց LYMErix-ի կիրառումը հիմնվելով այս հետազոտության վրա։
Պատվաստանյութի հաստատումից հետո վերջինիս գործնական կիրառման անցումը դանդաղ եղավ տարբեր պատճառներով, օրինակ՝ արժեքը, որը դժվարությամբ էր ձեռք բերվում ապահովագրական ընկերությունների կողմից[137]։ Որոշ ժամանակ անց, հարյուրավոր պատվաստվածներ նկարագրեցին աուտոիմուն և այլ կողմնակի երևույթներ։ Բուժառուների որոշ իրավաբանական օգնության խմբեր միջնորդեցին ԳլաքսոՍմիթԿլայն ընկերությանը դատի տալու հարցում, պնդելով, որ պատվաստանյութը պատճառ է հանդիսացել տարբեր առողջական խնդիրների առաջացման։ Այս պնդումների հիման վրա սննդի և դեղերի վերահսկման վարչությունը և հիվանդությունների վերահսկան կենտրոնը կրկին հետազոտեցին պատվաստանյութը չգտնելով ոչ մի կապ պատվաստման և աուտոիմուն խնդիրների առաջացման մեջ[138]։
Չնայած պատվաստանյութի օգտագործումից առողջական խնդիրների առաջացման ապացույցների բացակայությանը, LYMErix-ի վաճառքը կտրուկ անկում ապրեց և այն հետ կանչվեց ԱՄՆ շուկայից ԳլաքսոՍմիթԿլայնի կողմից 2002թ․-ի փետրվարին[139], պայմանավորված ԶԼՄ-ների բացասական արձագանքով և պատվաստանյութի կողմնակի երևույթների վախով[138][140]։ LYMErix-ի ճակատագիրը բժշկական գրականության մեջ նկարագրվում է, որպես «զգուշացումների հեքիաթ»[140]․ Nature պարբերականում հեղինակը գրում է, - անհիմն հանրային վախը այնպիսի ճնշում գործադրեց պատվաստանյութը հայտնաբերողների վրա, որ տեղի ունեցավ անսպասելին[22]։ OspA պատվաստանյութի գլխավոր հայտնագործող Մաքս Պլանկի ինստիտուտը պատասխանել է Nature պարբերականին․ «սա պարզապես ցույց է տալիս այն, թե ինչքան զայրացնող կարող է աշխարհը լինել․․․ Չկա ոչ մի գիտական իրեղեն ապացույց առաջին OspA պատվաստանյութ՝ LYMErix-ի վաճառքից դուրս մղման համար»[138]։
Շների մոտ Լայմի հիվանդության կանխարգելման համար ստեղծվել և հաստատվել են տարբեր պատվաստանյութեր։ Այս պահին առկա է մոտ 3 պատվաստանյութ։ Ֆորթ Դոդջ լաբորատորիայի կողմից ստեղծված LymeVax-ը պարունակում է անփոփոխ, մահացած սպիրոխետներ։ Ինտերվետ-Շերինգ-Փլյու-ի Galaxy Lyme պատվաստանյութը թիրախավորում է OpsC և OpsA սպիտակուցները։ OspC-ի հակամարմինները կոչնչացնեն ցանկացած մանրէի, որին չի ոչնչացրել OspA հակամարմինը։ Մերիալի կողմից ստեղծված Canine Recombinant Lyme-ը խթանում է OspA-ի նկատմամբ հակամարմինների առաջացումը և տիզը սնվելով պատվաստված շան արյունով ներծծում է հակա-OspA հակամարմիններով լի արյուն, որը սպանում է տզի աղիներում առկա սպիրոխետներին մինչև շանը վարակելը[141]։
Վալնեվայի վեցավալենտ (OspA) սպիտակուցի ենթամիավորների հիմքով ստեղծված պատվաստանյութի թեկնածու VLA15-ը 2017թ․-ի հուլիսին ներկայացվել էր ԱՄՆ-ի սննդի և դեղերի վերահսկման վարչություն դրամաշնորհի, ինչն էլ թույլ տվեց վերջինիս հետազոտությունների իրականացումը[142]։
Տզի հեռացում

Մաշկին կպած տզերը արագ պետք է հեռացվեն, քանի որ 36 ժամվա ընթացքում տզի հեռացումը նվազեցնում է հարուցիչների փոխանցման հավանականությունը[143]։ Հնում կիրառվող տզի հեռացման մեթոդներն անարդյունավետ են, չունեն ոչ մի առավելություն հիվանդության փոխանցման ռիսկի նվազման առումով և հակառակը, կարող են բարձրացնել վարակման կամ հիվանդության առաջացման ռիսկը[144]։ Տզի հեռացման լավագույն մեթոդը ունելիի օգնությամբ առավելագույնս մաշկին մոտ տզի բռնելը և հեռացնելն է առանց թափահարելու, խուսափելով մարմինը ճզմելուց կամ գլուխը պոկելուց[145]։ Հիվանդության փոխանցման հավանականությունը մեծանում տզի մաշկին կպած լինելու ժամանակի հետ, և եթե տիզն ամրացած է եղել ավելի քիչ, քան 24 ժամը, վարակման հավանականությունը խիստ ցածր է։ Սակայն, քանի որ տզերը չափերով փոքր են, հատկապես հարսնյակի փուլում, տզերի հայտնաբերումը դժվարություն է ներկայացնում[143]։ Կլինիկական իմունաբանության և ալերգաբանության ավստրալասիական ընկերությունը խորհուրդ չի տալիս ունելու օգնությամբ տզի հեռացումը, քանի որ եթե անհատը ալերգիկ եղավ, հնարավոր է անաֆիլակտիկ ռեակցիայի հրահրում։ Հակառակը, նրանք խորհուրդ են տալիս առաջնահերթ սպանել տզին՝ օգտագործելով նյութեր, որոնցով տզին միանգամից սառեցնում են և այն չի կարող արտադրել ալերգենով հարուստ թուք, և հետո հեռացնել այն ապահով վայրում, օրինակ՝ հիվանդանոցի շտապ օգնության բաժանմունքում[146]։
Կանխարգելիչ հակաբիոտիկների կիրառում
Հիվանդության փոխանցման հավանականություն մեծանում է տզի կպած լինելու ժամկետի հետ[147]։ Լայմի հիվանդության հարուցիչի փոխանցման համար պահանջվում է 36-ից 48 ժամ, որի ընթացքում այն թքի հետ անցնում է տիրոջ արյուն[147]։ Եթե եղնիկի տիզը հայտնաբերվում է անհատի մաշկին կպած և այն ամրացած է եղել մոտ 36 ժամ կամ լցված է արյունով, ցանկալի է դոքսիցիկլինի մեկ դեղաչափ տալ հիվանդին տզի հեռացնելուց 72 ժամվա ընթացքում, որպեսզի նվազեցվի Լայմի հիվանդության առաջացման հավանականությունը։ Այն խորհուրդ չի տրվում տզի ցանկացած խայթոցից հետո, քանի որ հիվանդության զարգացումը հազվադեպ է լինում․ մեկ էրիթեմա միգրանսի դեպք կանխարգելելու համար պահանջվում է դոքսիցիկլինի կիրառում մոտ 50 անհատի կողմից[4][147]։
Մասնագիտական գործոն
Վարակված տզերի շրջաններում ապրող և դրսում աշխատող անձինք Լայմի հիվանդության ռիսկի խմբում են։ 2010թ․-ին ԱՄՆ-ում Լայմի հիվանդության առավելագույն գրանցում դիտվել է Նյու Ջերսիում, Փենսիլվանիայում, Վիսկոնսինում, Նյու Յորքում, Մասսաչուսեթսում, Կոնեկտիկուտում, Մինեսոտայում, Մերիլենդում, Վիրջինիայում, Նյու Հեմփշիրում, Դելավերում և Մենում։ ԱՄՆ-ի հյուսիսարևելյան և հյուսիսային կենտրոնական նահանգները վարակված տզերի հանդիպման ամենաբարձր ռիսկն ունեն։ Այս և այլ նահանգներում աշխատողների մոտ տզերը կարող են փոխանցել նաև այլ հիվանդություններ։ Փայտով, թփերով, բարձր խոտածածկույթով կամ թափված տերևներով հարուստ աշխատավայրերում տզերի քանակն ավելի շատ է։ Դրսում աշխատողները հատկապես զգույշ պետք է լինեն ուշ գարնանը և ամռանը, որպեսզի պաշտպանեն իրենց տզերից, քանի որ այս ժամանակաշրջանում տզերն առավել ակտիվ են[148]։
Բուժում
Առաջնային բուժումը հակաբիոտիկներն են[4][147]։ Բուժմանը սպեցիֆիկ մոտեցումը կախված է վարակված անհատից և հիվանդության փուլից[147]։ Վաղ տեղայնացված ձևով հիվանդների մեծ մասի համար, որպես առաջին ընտրության միջոց խորհուրդ է տրվում բերանացի դոքսիցիկլինի կիրառումը, քանի որ այն արդյունավետ է ոչ միայն բորելիաների, այլ նաև տզերով փոխանցվող այլ հիվանդությունների դեպքում[147]։ Դոքսիցիկլինը հակացուցված է մինչև 8 տարեկան երեխաներին և կանանց, ովքեր հղի են կամ կրծով կերակրում են[147]․ որպես փոխարինող կարելի է կիրառել ամոքսիցիլին, ցեֆուրոքսիմ աքսետիլ և ազիթրոմիցին[147]։ Վաղ տարածված կամ ուշ փուլերի հիվանդության պարագայում կարող են դրսևորվել նաև սրտային խնդիրներ, ռեֆրակտեր Լայմի արթրիտ կամ նյարդաբանական ախտանիշներ, ինչպես մենինգիտն է կամ էնցեֆալիտը[147]։ Այս դեպքերում առաջին ընտրության միջոց է ներերակային ցեֆտրիաքսոնը[147], իսկ որպես փոխարինող՝ ցեֆոտաքսիմը և դոքսիցիկլինը[147]։
Այս բուժման տևողությունը կազմում է մեկից չորս շաբաթ[147]։ Եթե պահպանվում կամ վերադառնում է հոդի այտուցը, պետք է կիրառվի հակաբիոտիկային բուժման ևս մեկ կուրս[147]։ Սրան հակառակ, հակաբիոտիկների երկարատև՝ ավելի քան 28 օր կիրառումը խորհուրդ չի տրվում, քանի որ բացակայուն են կլինիկական ապացույցների վերջինիս արդյունավետության մասին[147][149]։ IgM և IgG հակամարմինների քանակը բարձր կարող է լինել նույնիսկ հակաբիոտիկային արդյունավետ բուժումից տարիներ հետո[147]։ Քանի որ հակամարմինների քանակը ցույց չի տալիս բուժման արդյունավետությունը, վերջիններիս քանակը չի որոշվում[147]։
Կանխատեսում
Հիվանդության վաղ փուլերում հիվանդությունը հիմնականում բուժելի է[150]։ Սակայն, Լայմի հիվանդության ծանրությունը և բուժումը կարող է դժվարացած լինել ուշ ախտորոշման, հակաբիոտիկային բուժման ձախողման և տզերով փոխանցվող այլ հիվանդության զուգահեռ առկայության պարագայում, ինչպես օրինակ՝ էրլիխիոզը, բաբեշիոզը և իմունիտետի ընկճումը հիվանդի մոտ։
Հայտնի է, որ հիվանդների մինչև 5%-ի մոտ բուժման ավարտին դիտվում է ձգձգվող հոգնածություն, ցավեր, կամ հոդամկանացավ[151]։ Այս ախտանշանները կարող են տևոլ ավելի քան 6 ամիս։ Այս վիճակը կոչվում է Լայմի հիվանդության հետբուժումային համախտանիշ։ 2016թ․-ից սկսած հետազոտություններով այս համախտանիշի պատճառը չի հայտնաբերվել, սակայն այն վարում են ֆիբրոմիալգիայի կամ քրոնիկական հոգնածության համախտանիշի նման[152]։
Շների պարագայում, երկարատև լուրջ կանխատեսումներով կարող է առաջանալ կծիկային հիվանդություն[153], որը երիկամների վնասմամբ ուղեկցվող այնպիսի վիճակ է, որը կարող է բերել քրոնիկական երիկամային հիվանդության[141]։ Շները նույնպես կարող են ունենալ քրոնիկական հոդային հիվանդություն, եթե Լայմը չբուժվի։ Այնուամենայնիվ, շների մոտ Լայմի հիվանդության դեպքերի մեծամասնությունում հակաբիոտիկներով կամ առանց հակաբիոտիկների բուժումն ավարտվում է ամբողջական լավացումով[154]։ Հազվադեպ Լայմի հիվանդությունը մահացու կարող է լինել ինչպես շների, այնպես էլ մարդկանց համար[155]։
Պատմություն
Borrelia burgdorferi գենետիկայի էվոլյուցիան ժամանակակից ուսումնասիրությունների թեմա է դարձել։ Հետազոտություններից մեկում նշվել է որ, Նոր Անգլիայում հետ-գաղութային ֆերմաներից հրաժարվելուն զուգահեռ, անտառավերականգնումներից և 19րդ դարում տեղի ունեցած դեպի Միջին արևմտյան Միացյալ Նահանգներ մեծաքանակ գաղթից առաջ, Լայմի հիվանդությունը հազարավոր տարիներ եղել է Ամերիկայում և տզի ու տիրոջ հետ տարածվել է Հյուսիսարևելյան Միացյալ Նահանգներից դեպի Միջին Արևմտյան Միացյալ Նահանգներ[156]։
Ջոն Ջոսելինը, որ 1638 և կրկին 1663-1670 թվականներին այցելել է Նոր Անգլիա, գրել է․ «Այնտեղ ամռանը թփերից անհամար քանակի տզեր են կախված, որոնք կճեղքեն մարդկանց հագուստները, կսողան նրանց տաբատների մեջ և կարճ ժամանակում մարդուն կվերածեն դիակի։ Ես տեսել եմ նրանց գուլպաները, ովքեր անցել են անտառի միջով, ծածկված դրանցով»[157]։
Վերոնշյալը նույնպես հաստատվել է շվեդացի բուսաբան Պեր Կալմի գրվածքներում, ում Կառլ Լիննեյը ուղարկել էր Ամերիկա, երբ 1749-ին այցելեց Նյու Յորքի այգի այնտեղ նա տեսավ որ այգին լիքն է տզերով։ Երբ Կալմի աշխատանքները 100 տարի անց վերականգնվեցին, անտառն այլևս չկար և Լայմի բակտերիան հավանաբար մեկուսացվել էր հյուսիսարևելյան ափի երկայնքով՝ Վիսկոնսին և Մինեսոտա[158]։
Հնարավոր է առաջին մանրամասն նկարագրությունը, որ մեզ հայտնի է ինչպես Լայմի հիվանդություն, հայտնվել են բարեկրոն Դոկտոր Ջոն Ուոքերի գրվածքներում, 1764-ին Շոտլանդիայի արևմտյան ափից անջատված Ջուրայի կղզի (Deer Island (Եղնիկի կղզի)) այցից հետո[159]։ Նա լավ բացատրում է Լայմի հիվանդության ախտանիշները (նրա խոսքերով «սուր ցավ վերջույթների վերին հատվածներում») և որ, տիզը հանդես է գալիս որպես պարազիտակիր որը, նա նկարագրոմ է որպես, «Ճիճու կարմրավուն գունավորմամբ, սեղմված ձևով և ամեն մի կողմում ունի ոտքերի շարք, որը ներթափանցում է մաշկի մեջ»։ 1717-ին և 18րդ դարի վերջին շատ մարդիկ Մեծ Բրիտանիայի այդ հատվածից գաղթեցին Հյուսիսային Ամերիկա։
Թանգարանային պահպանված նմուշների զննելուց հայտնաբերեցին Borrelia-ի ԴՆԹ 1884-ին Գերմանիայից բերված վարակված Ixodes ricinus տզի մոտ, և Քեյփ Քոդից բերված վարակված մկան մոտ, որը սատկեց 1894-ին[158]։ 2010-ին 5300 տարեկան Էցի մումիայի դիահերձումը բացահայտեց Borrelia burgdorferi -ի ԴՆԹ-ի հաջորդականության առկայություն, դարձնելով նրան ամենահին մարդը ով հիվանդ է եղել Լայմի հիվանդությունով[160]։
Եվրոպական վաղ հետազոտություններում Լայմի հիվանդությունը ներկաացված է մաշկային դրսևորումներով։ Գերմանիա, Բրեսլաու քաղաքում (այժմ Վրոցլավ, Լեհաստան) առաջին հետազոտությունը եղել է 1883-ին, երբ բժիշկ Ալֆրեդ Բուքվալդը նկարագրեց մարդու, ով 16 տարի էր ինչ տառապում էր մաշկային հիվանդությամբ, որն այժմ հայտնի է ինչպես քրոնիկական ապաճական ակրոդերմատիտ[161]։
1909-ի հետազոտական կոնֆերանսում, շվեդացի մաշկաբան Արվիդ Աֆզելիուսը ներկայացրեց զեկույց մեծացող, մատանիանման ախտահարման մասին, որը նա նկատեց մի կնոջ մոտ, որին նախորդել էր ոչխարի տզի խայթոցը։ Նա անվանեց ախտահարումը թափառող էրիթեմա[161]։ Բորելիար լիմֆոցիտոման մաշկային հիվանդություն է, որը առաջին անգամ նկարագրվել է 1911-ին[162]։
Հիվանդության կլինիկական գործընթացների՝ պատճառ, ախտորոշում և բուժում, ընկալումը դժվարա էր[163]։
Տզի խայթոցից հետո առաջացող նյարդաբանական խնդիրները սկսել են հասկանալ 1920-ականներից։ Ֆրանսիացի բժիշկներ Գարին և Բուժադոն նկարագրել էին մի ֆերմերի, ում մոտ տզի խայթոցից հետո դրսևորվել էին զգայական ռադիկուլիտի և թեթև մենինգիտի երևույթներ։ Մեծ, մատանիանման ցանավորումը նույնպես առկա է եղե, պարզապես բժիշկները այն չեն վերագրել մենինգոռադիկուլիտին։ 1930-ին շվեդացի մաշկաբան Սվեն Հելլերստրոմը առաջինն էր, ով առաջարկեց, որ տզի խայթոցից հետո առաջացած նյարդաբանական ախտանիշները և էրիթեմա միգրանսը իրար հետ փոխկապակցված են[164]։ 1940-ականներին Գերմանացի նյարդաբան Ալֆրեդ Բենուորթը, նկարագրեց խրոնիկական լիմֆոցիտային մենինգիտի և պոլիռադիկուլոնևրիտի մի քանի դեպքեր, որոնցից մի քանիսը զուգակցվում էին մաշկի էրիթեմատոզ ախտահարումներով։
Կարլ Լինեյը, ով աշխատում էր Շվեդիայի Կարոլինսկայի համալսարանում, հավատացած էր, որ մաշկի բազմաթիվ ախտահարումները պայմանավորված են սպիրոխետներով։ 1948-ին նա օգտագործեց հատուկ ներկ, որ մանրադիտակով հետազոտի մաշկի տարբեր ախտահարումներում ներառյալ էրիթեմա միգրանսում գնտվող թվացյալ սպիրոխետները[165]։ Չնայած հետագայում պարզվեց որ նրա հետևությունները սխալ էին, բայց դրան հետևեց հետաքրքրություն սպիրոխետների ուսումնասիրության ոլորտում։ 1949-ին Նիլս Թիրեսսոնը, ով նույնպես աշխատել է Կարոլինսկայի համալսարանում, առաջին անգամ պենիցիլինով բուժեց քրոնիկական ապաճական ակրոդերմատիտը[166]։ 1950-ականներին տզի խայթոցի, լիմֆոցիտոմայի, էրիթեմա միգրանսի և Բենուորթի համախտանիշի կապը ընդունվեց ամբողջ Եվրոպայում, բերելով պենիցիլինի համատարած օգտագործմանը Եվրոպայում[167][168]։
1970-ին Վիսկոնսինից մաշկաբան Ռուդոլֆ Սկրիմենտին, 1950-ին Ամերիկյան գիտական ամսագրում Հելլերստրոմի վերահրատարակած հոդվածը նայելուց հետո հիվանդի մոտ ճանաչեց էրիթեմա միգրանս ախտահարումը։ Սա ԱՄՆ-ում էրիթմա միգրանսի առաջին գրանցված դեպքն է։ Հիմնվելով Եվրոպական գրականության վրա, հիվանդին նա բուժեց պենիցիլինով[169]։
Ամբողջական համախտանիշը, որն այժմ հայտնի է ինչպես Լայմի հիվանդություն, չէր ճանաչվում մինչև, 1975-ին հարավարևելյան Կոնեկտիկուտի երեք քաղաքներում, ներառյալ Լայմում և Օլդ Լայմում, որտեղից էլ ծագել է անունը, այն ժամանակ թվացյալ յուվենիլ ռևմատոիդ արթրիտի խմբային դեպքերը[170]։ Հետազոտությունը անցկացվել էր Համաճարակաբանության հետախուզական ծառայության բժիշկներ Դեյվիդ Սնիդմանի և Ալլան Սթիրի կղմից, նաև Եյլի համալսարանից այլոց կողմից, ներառյալ Ստիվեն Մալավիստայի, ով նշվում է հիվանդության հայտնաբերողներից մեկը[171]։ ԱՄՆ-ում հիվանդերի էրիթեմա միգրանսի ճանաչումը բերեց «Լայմ արթրիտի» ճանաչմանը, որպես Եվրոպայում նույն, տզից առաջացած, հիվանդության դրսևորումներից մեկը[70]։
Մինչև 1976 թվականը, B. burgdorferi sensu lato վարակը անվանում էին, կամ հայտնի էր ինչպես տզից առաջացած մենինգոպոլինևրիտ, Գարին-Բուժադոյի համախտանիշ, Բենուարթի համախտանիշ, Աֆզելիուսի հիվանդություն[172], Մոնթակ Նիի կամ ոչխարի տզի տենդ։ 1976-ից սկսած հիվանդությունն հիմնականում անվանում են Լայմի հիվանդություն[173][174], Լայմի բորելիոզ կամ ուղակի բորելիոզ։
1980-ին Սթիրը և այլք, մեծահասակ հիվանդների շրջանում սկսեցին փորձել հակաբիոտիկային սխեմաներ[175]։ Նույն տարում, Նյու Յորք նահանգի առողջապահության վարչության, համաճարակաբան Ջորջ Բենաքը Ժայռոտ լեռի կենսաբանական լաբորատորիայի հետազոտող Վիլլի Բուրգդորֆերին Նյու Յորքի Շելթեր կղզուց, որը հայտնի է որպես Լայմի էնդեմիկ օջախ ինչպես նաև Ժայռոտ լեռի բծավոր տենդի հետազոտման վայր ապահովեց I. dammini [scapularis] տզերով։ Երբ ռիկետսիաների համար հետազոտում էր տզերը, Բուրգդորֆերը նկատեց «վատ ներկվող, երկար, անկանոն սպիրալաձև սպիրոխետներ»։ Հետագա ուսումնասիրությունները ցույց տվեցին սպիրոխետների առկայություն տզերի 60%-ի մոտ։ Բուրգդորֆերը նշեց նրա արդյունքների նմանությունը Եվրոպական գրականության հետ, նրա ըմբռնմամբ ապիրոխետները կարող են լինել էրիթեմա միգրանսի և Լայմի հիվանդության երկար սպասված պատճառը։ Բենաքը նրան Շելթեր կղզուց տրամադրեց ավելի շատ տզերով և Լայմի հիվանդությունով ախտորոշված հիվանդների շիճուկով։ Տեխասի առողջության գիտական կենտրոնի համալսարանի հետազոտող Ալան Բարբորը առաջարկեց փորձաքննություն կատարել, ստեղծել կուլտուրաներ և իմունոքիմիականորեն բնութագրել օրգանիզմը։ Բուրգդորֆերը հետագայում հաստատեց իր հայտնագործությունը `մեկուսացնելով Լայմի հիվանդությամբ հիվանդներին, նույնականացրեց տզի մոտ հայտնաբերած սպիրոխետներին[176]։ 1982-ի հունիսին նա հրապարակեց իր հայտնագործությունները Science ասագրում, և սպիրոխետները անվանվեցին նրա պատվին Borrelia burgdorferi[177]
B. burgdorferi-ի որպես Լայմի հիվանդության պատճառածին ագենտ, փորձարկման համար ընտրվեցին հակաբիոտիկներ, ուղղորդված հակաբիոտիկների նկատմամբ in vitro զգայունության որոշմամբ, որոնք ներառում էին տետրացիկլինային հակաբիոտիկներ, ամոքսացիլին, ցեֆուրոքսիմ աքսիտել, ներերակային և միջմկանային պենիցիլին և ներերակային ցեֆտրիաքսոն[178][179]։Տզի փոխանցման մեխանիզմը նույնպես քննարկման թեմա էր։ B. burgdorferi սպիրոխետներ հայտնաբերվել են տզի թքի մեջ 1987-ին, հաստատելով այն վարկածը որ փոխանցումը տեղի է ունենում թքագեղձերի միջոցով[180]։
Ծանոթագրություններ
Այլ ընթերացնություն
- Richard Ostfeld (2012). Lyme Disease: The Ecology of a Complex System. New York: Oxford University Press. ISBN 978-0199928477.
- Pamela Weintraub (2008). Cure Unknown: Inside the Lyme Disease Epidemic. St. Martin's Press. ISBN 9780312378127.
- Newby, Kris (2019). Bitten: the Secret History of Lyme Disease and Biological Weapons. HarperCollins. ISBN 9780062896278.
Արտաքին հղումներ
- Լայմի հիվանդությունը CDC.gov կայքում
- Լայմի հիվանդույթան թեստեր - Օնլայն լաբորատոր թեստեր
- Լայմի հիվանդությունը NIH.gov կայքում
- Ի՞նչ անել, եթե հայտանաբերել եք տիզ
| Վիքիցեղերն ունի նյութեր, որոնք վերաբերում են «Լայմի հիվանդություն» հոդվածին։ |
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Լայմի հիվանդություն» հոդվածին։ |