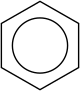
Бензен
Бензен (тривијални назив: бензол), молекулске формуле C6H6, најједноставнији је ароматични угљоводоник. Открио га је Мајкл Фарадеј 1825. године. Основно једињење велике групе органских ароматичних једињења - арена. То је безбојна течност карактеристичног мириса и мале вискозности, густина 0,885 g/cm³, тачка топљења 5,5 °C, тачка кључања 80,2 °C. Гори светлим и јако чађавим пламеном. Отрован је и канцероген и у течном и у гасовитом стању. Добија се при сувој дестилацији угља у коксарама, на подручју некадашње Југославије у Лукавцу и Зеници. Знатне количине се производе и синтетички, каталитичким крековањем алифатичних и нафтенских угљоводоника. У свету је 1975. године произведено 8,92 милиона тона. Употребљава се у хемијској индустрији као растварач, средство за екстракцију и као сировина за друге производе.
| |||
| |||
 | |||
| Називи | |||
|---|---|---|---|
| IUPAC назив Бензен | |||
| Преферисани IUPAC назив Benzene[1] | |||
| Системски IUPAC назив циклохекса-1,3,5-триен | |||
Други називи
| |||
| Идентификација | |||
3Д модел (Jmol) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.685 | ||
| EC број | 200-753-7 | ||
| KEGG[2] | |||
| RTECS | CY1400000 | ||
| UNII | |||
| |||
| |||
| Својства | |||
| C6H6 | |||
| Моларна маса | 78,11 g·mol−1 | ||
| Агрегатно стање | Безбојна течност | ||
| Мирис | ароматичан, сличан бензину | ||
| Густина | 0,8765(20) g/cm³[5] | ||
| Тачка топљења | 5,53 °C (41,95 °F; 278,68 K) | ||
| Тачка кључања | 80,1 °C (176,2 °F; 353,2 K) | ||
| 1.53 g/L (0 °C) 1.81 g/L (9 °C) 1.79 g/L (15 °C)[6][7][8] 1.84 g/L (30 °C) 2.26 g/L (61 °C) 3.94 g/L (100 °C) 21.7 g/kg (200 °C, 6.5 MPa) 17.8 g/kg (200 °C, 40 MPa)[9] | |||
| Растворљивост | растворан у алкохолу, хлороформу, CCl4, диетил етру, ацетону, сирћетној киселини[9] | ||
| Растворљивост у етандиол | 5,83 g/100 g (20 °C) 6,61 g/100 g (40 °C) 7,61 g/100 g (60 °C)[9] | ||
| Растворљивост у етанол | 20 °C, раствор у води: 1,2 mL/L (20% v/v)[10] | ||
| Растворљивост у ацетон | 20 °C, раствор у води: 7,69 mL/L (38,46% v/v) 49,4 mL/L (62,5% v/v)[10] | ||
| Растворљивост у диетилен гликол | 52 g/100 g (20 °C)[9] | ||
| log P | 2,13 | ||
| Напон паре | 12,7 kPa (25 °C) 24,4 kPa (40 °C) 181 kPa (100 °C)[11] | ||
| Конјугована киселина | бензенијум | ||
| λmax | 255 nm | ||
| Магнетна сусцептибилност | −54,8·10−6 cm³/mol | ||
| Индекс рефракције (nD) | 1,5011 (20 °C) 1,4948 (30 °C)[9] | ||
| Вискозност | 0,7528 cP (10°,) 0,6076 cP (25 °C) 0,4965 cP (40 °C) 0,3075 cP (80 °C) | ||
| Структура | |||
| Облик молекула (орбитале и хибридизација) | Тригонално планарна | ||
| Диполни момент | 0 D | ||
| Термохемија | |||
| Специфични топлотни капацитет, C | 134,8 J/mol·K | ||
Стандардна моларна ентропија (S | 173,26 J/mol·K[11] | ||
Стандардна енталпија стварања (ΔfH | 48,7 kJ/mol | ||
Стд енталпија сагоревања (ΔcH⦵298) | 3267,6 kJ/mol[11] | ||
| Опасности | |||
| Главне опасности | потенцијални радни карциноген, запаљив | ||
| Безбедност приликом руковања | HMDB | ||
| ГХС пиктограми |      [12] [12] | ||
| ГХС сигналне речи | Опасност | ||
ГХС извештаји опасности | H225, H304, H315, H319, H340, H350, H372, H410[12] | ||
ГХС изјаве предрострожност | P201, P210, P301+310, P305+351+338, P308+313, P331[12] | ||
| NFPA 704 | |||
| Тачка паљења | −11,63 °C (11,07 °F; 261,52 K) | ||
| 497,78 °C (928,00 °F; 770,93 K) | |||
| Експлозивни лимити | 1,2–7,8% | ||
| Смртоносна доза или концентрација (LD, LC): | |||
LD50 (средња доза) | 930 mg/kg (пацов, орално) | ||
LCLo (најнижа објављена) | 44.000 ppm (зец, 30 min) 44.923 ppm (пас) 52.308 ppm (мачка) 20.000 ppm (човек, 5 min)[14] | ||
| Границе изложености здравља у САД (NIOSH): | |||
PEL (дозвољено) | TWA 1 ppm, ST 5 ppm[13] | ||
REL (препоручено) | Ca TWA 0.1 ppm ST 1 ppm[13] | ||
IDLH (тренутна опасност) | 500 ppm[13] | ||
| Сродна једињења | |||
Сродна једињења | |||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Бензенов прстен
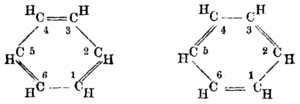
Бензенов прстен је шесточлани прстен који образују атоми угљеника у структури молекула угљоводоника бензола. Основни је структурни састојак органских ароматичних једињења. Слободни електронски парови угљеника у прстену су делокализовани и изнад и испод равни прстена граде делокализоване електронске облаке. Оваква структура је хемијски веома постојана па су једињења која поседују бензенов прстен, и поред постојања незасићених веза, претежно дезактивирана за реакцију адиције. Прстен је пак подложан електрофилном нападу односно електрофилној ароматичној супституцији при којој се очувава ароматичност (посебна пажња се обраћа на редослед увођења супституената због њихових дирекционих утицаја). Добијени деривати имају широку примену.
Историја
Откриће
Реч „бензен” је изведена из „гуменог бензоина” (бензоинске смоле), ароматичне смоле коју су европски фармацеути и парфемери познају од 16. века као производ из југоисточне Азије.[15] Један кисели материјал је изведен из бензоина сублимацијом и назван „цветови бензоина”, или бензојевa киселинa. Угљоводоници који су добијени из бензојеве киселине тако су добили име бензин, бензол или бензен.[16] Мајкл Фарадej је први изоловао и идентификовао бензен 1825. године из уљаног остатка добијеног из производње илуминирајућег гаса, и дао му име бикарбурет водоника.[17][18] Године 1833, Ајлхард Мичерлих га је произвео дестилацијом бензојеве киселине (из гуменог бензоина) и кречњака. Он је назвао то једињење бензин.[19] Године 1836, француски хемичар Аугуст Лоран је ову супстанцу назвао „фен” (франц. phène);[20] та реч је постала корен енглеске речи „фенол”, који је хидроксиловани бензен, и „фенил”, радикал настао апстракцијом атома водоника (слободни радикал H•) из бензена.
Године 1845, Чарлс Мансфилд, радећи под фон Хофманом, изоловао је бензен из каменоугљене смоле.[21] Четири године касније, Мансфилд је почео прву производњу бензена индустријских размера, користећи метод базиран на каменоугљеној смоли.[22][23] Постепено се развио осећај међу хемичарима да су бројне друге супстанце хемијски сродне са бензеном, и да сачињавају засебну хемијску фамилију. Године 1855, Хофман је користио реч „ароматичан” за описивање тих породичних односа, јер је то карактеристично својство многих чланова те породице.[24] Године 1997, бензен је детектован у дубоком свемиру.[25]
Референце
Литература
Спољашње везе
 Медији везани за чланак Бензен на Викимедијиној остави
Медији везани за чланак Бензен на Викимедијиној остави
- ATSDR – Case Studies in Environmental Medicine: Benzene Toxicity
- Benzene
- Benzene Material Safety Data Sheet
- International Chemical Safety Card 0015
- National Pollutant Inventory - Benzene
- NIOSH Pocket Guide to Chemical Hazards
- IARC Monograph: "Benzene"
- Computational Chemistry Wiki
- Couper and Carbon bonds
- Dept. of Health and Human Services: TR-289: Toxicology and Carcinogenesis Studies of Benzene
- Kekule, Couper and dreams of Benzene Архивирано на сајту Wayback Machine (22. мај 2006)
- video podcast (Sir john Cadogan giving a lecture on Benzene since Faraday, in) 1991