வளிமம்
வளிமம் (அல்லது வாயு) (gas) என்பது பொருட்களின் நான்கு இயற்பியல் நிலைகளுள் ஒன்று. திண்மம், நீர்மம், பிளாஸ்மா என்பனவே ஏனைய மூன்று நிலைகளும் ஆகும். ஒரு குறிப்பிட்ட வெப்பநிலையில் திண்மமாக இருக்கும் பொருள் ஒன்று வெப்பநிலையை கூட்டும்போது ஒரு குறிப்பிட்ட வெப்பநிலையில் நீர்மமாக மாறும். மேலும் வெப்பநிலையைக் கூட்டினால் இன்னும் கூடிய ஒரு வெப்பநிலையில் அது வளிம நிலைக்கு மாறும்.

மாந்தர்களும் பிற பல விலங்குகளும் உயிர்வாழ அடிப்படையாகத் தேவைப்படும் ஒரு வகை வளிமம் ஆக்சிசன் (ஒட்சிசன்) எனப்படும். இதை உயிர்வளி என குறிக்கிறார்கள். ஐதரசன் (ஹைடிரஜன்) என்னும் வளிமத்தைத் தமிழில் நீரதை என்றும் வழங்குவதும் உண்டு. எனவே ஆக்சிசன், நைட்ரஜன், ஆர்கான், நியான், ஐதரசன் போன்ற பல பொருட்கள் வளிம நிலையில் உள்ளன.
வாயு அல்லது வளிம நிலை என்பது பருப்பொருளின் நீா்ம மற்றும் பிளாசுமா நிலைகளுக்கு இடைப்பட்ட நிலையாகும்.[1] .
நாம் வாழும் நில உலகில் உள்ள வளிமண்டலத்தில் சற்றேறக் குறைய 78% நைட்டிரசன் (நைதரசன்) என்னும் வளிமமும், 21% உயிர்வளியும் எஞ்சியுள்ள 1% மட்டும் தான் கார்பனீரொட்சைட்டு போன்ற பிற வளிமங்கள்.

தனிம நிலையிலுள்ள வாயுக்கள்
ஐதரசன் (H2), நைட்ரசன் (N2) ஆக்சிசன் (O2) ஹாலஜன்களில் புளோரின் (F2) மற்றும் குளோரின் (Cl2) ஆகியவை மட்டுமே திட்ட வெப்ப அழுத்த நிலையில் ஓரினக் கருவுள்ள பல அணு மூலக்கூறுகளான நிலைப்புத் தன்மையுள்ள தனிம நிலையிலுள்ள வாயுக்கள் ஆகும். இவை தவிர ஒற்றை அணுவைக் கொண்ட மந்த வாயுக்களான ஹீலியம் (He), நியான் (Ne), ஆர்கான் (Ar), கிரிப்டான் (Kr), செனான் (Xe) மற்றும் ரேடான் (Rn) ஆகியவற்றையும் சேர்த்து தனிம நிலையிலுள்ள வாயுக்கள் என அழைக்கப்படுகின்றன. சில நேரங்களில் இவை மூலக்கூறு வாயுக்கள் எனவும் அழைக்கப்படுகின்றன.
இயற்பியல் பண்புகள்

பெரும்பான்மையான வாயுக்கள் நேரடியாக உற்றுநோக்க சிரமமானவையாக இருப்பதால், நான்கு பேரியலான அல்லது கட்புலனாகத்தக்க பண்புகளான அழுத்தம், கன அளவு, துகள்களின் எண்ணிக்கை(மோல்) மற்றும் வெப்பநிலை ஆகியவற்றின் வழியாக வாயுக்கள் விவரிக்கப்படுகின்றன. இந்த நான்கு இயல்புகளும் வெவ்வேறு வேதியியலாளா்களால் இராபர்ட் பாயில், ஜாக்குஸ் சார்லஸ், ஜான் டால்டன், ஜோசப் கே லுாசாக் மற்றும் அமெடியோ அவாகாட்ரோ ஆகியோரால் பலவிதமான வாயுக்களுக்கு வெவ்வேறு சூழ்நிலைகளில் மீண்டும், மீண்டும் ஆய்வுக்குட்படுத்தப்பட்டன. அவா்களின் விரிவான ஆய்வுகள் இறுதியாக நல்லியல்பு வாயுக்களுக்கான வாயுச் சமன்பாடாக, மேற்கூறிய நான்கு பண்புகளுக்குமான கணிதவியல் தொடர்பாக வருவிக்கப்பட்டது.
வாயு மூலக்கூறுகளானவை ஒன்றிலிருந்து மற்றொன்று அதிக இடைவெளியில் இருப்பதால் அவற்றுக்கிடையோன மூலக்கூறுகளுக்கிடையேயான கவா்ச்சி விசை அல்லது பிணைப்பானது திரவங்கள் மற்றும் திண்மங்களை விடவும் வலிமை குறைந்தவையாக காணப்படுகின்றது. மூலக்கூறுகளுக்கிடையேயான கவா்ச்சி விசையானது வாயு மூலக்கூறுகளுக்கிடையேயான நிலை மின்னியல் கவா்ச்சி விசையின் காரணமாக விளைகிறது. ஒத்த மின்சுமையைக் கொண்ட துகள்கள் ஒன்றை ஒன்று விலக்கியும், எதிரெதிர் மின்சுமை கொண்ட துகள்கள் ஒன்றை ஒன்று ஈர்க்கவும் செய்கின்றன. சகப்பிணைப்புத் தன்மையுள்ள வளிமச் சேர்மங்களில் நிகர மின்சுமையானது சுழியாக இருப்பினும் இச்சேர்மங்களில் காணப்படும் நிலையான, சமச்சீரற்ற மின்சுமை பரவலின் காரணமாக அவை வலிமையான மூலக்கூறுகளுக்கிடை கவர்ச்சி விசைக்கு ஆட்படுகின்றன. நிலையற்ற, ஒழுங்கற்ற முறையில் துாண்டப்பட்ட மின்சுமைகளானது மூலக்கூறுகளில் மின் முனைவற்ற சகப்பிணைப்புகளில் காணப்படுகிறது. இத்தகைய துாண்டப்பட்ட மின்சுமைகளால் உருவாக்கப்டும் நிலை மின்னியல் கவா்ச்சி விசையானது வாண்டா்வால்சு விசை என அழைக்கப்படுகிறது. வளிமங்களின் இயற்பியல் பண்புகள் மூலக்கூறுகளுக்கிடைப்பட்ட கவர்ச்சி விசையானது இடைவினையாற்றுவதைப் பொறுத்து ஒரு பொருளுக்குள்ளேயே மாறுபடுகிறது.ஒவ்வொரு வளிமத்தக்குமான தனித்தன்மை வாய்ந்த இயற்பியல் பண்புகள் மூலக்கூறுகளுக்கிடைப்பட்ட கவா்ச்சி விசை இடைவினை புரிவதைப் பொறுத்தே அமைகிறது.[2][3] இந்த முடிவு, அயனிப்பிணைப்பு மற்றும் சகப்பிணைப்பால் உருவாக்கப்பட்ட சேர்மங்களின் கொதிநிலையானது ஒப்பிட்டுப்பார்க்கப்பட்டதால் கிடைத்ததாகும்.[4]
பருப்பொருட்களின் இதர நிலைகளை ஒப்பிடும் போது வளிமமானது குறைவான அடா்த்தி மற்றும் பாகுநிலையைக் கொண்டுள்ளது. அழுத்தம் மற்றும் வெப்பநிலை ஒரு குறிப்பிட்ட கன அளவு வரை மூலக்கூறுகளில் பாதிப்பை ஏற்படுத்துகின்றன.
அளவிடக்கூடிய அல்லது பேரியல் பண்புகள்
ஒரு வாயு நிலையை விளக்குவதற்கு தேவைப்படும் நான்கு காரணிகள், அளவிடக்கூடிய பண்புகள் எனப்படும். கன அளவு V, அழுத்தம் P, வெப்பநிலை T மற்றும் மோல்களின் எண்ணிக்கை n ஆகியவை அளவிடக்கூடிய பண்புகளாகும்.
அழுத்தத்தின் விளைவு
வாயு அல்லது வளிம நிலையில் மூலக்கூறுகள் எண்ணிக்கை அதிகமாக காணப்படும். வாயு மூலக்கூறுகள் ஒழுங்கின்றி இயங்கக்கூடிய தன்மை கொண்டவை. மூலக்கூறுகளுக்கிடையே உள்ள மோதல்களை விட கொள்கலனில் அடிக்கடி மோதிக் கொள்கின்றன. மோதலானது மீட்சித்தன்மை கொண்டிருப்பதால் இத்தகைய மோதல்களால் ஆற்றல் இழப்பு ஏற்படுவதில்லை. ஓரலகு பரப்பின் மீது செயல்படும் விசை அழுத்தம் எனப்படும். கொள்கலனில் சுவரில் ஓரலகு பரப்பில் ஒரு விநாடியில் நிகழும் மோதலில் ஏற்படும் மூலக்கூறுகளின் எண்ணிக்கையைப் பொருத்ததாகும். அதிக எண்ணிக்கையில் மூலக்கூறுகள் சுவரின் ஓரலகு பரப்பில் ஒரு விநாடியில் மோதலை நிகழ்த்தும் போது வாயுவின் அழுத்தமானது அதிகரிக்கும்.[5]
வெப்பத்தின் விளைவு
வாயுவின் இயக்க ஆற்றலுக்கான சமன்பாடு ½mv2 ஆகும். m என்பது மூலக்கூறின் நிறை, v என்பது திசைவேகம். வாயுவை வெப்பப்படுத்தும் போது, வெப்பநிலை உயர்வின் காரணமாக மூலக்கூறுகளின் திசைவேகம் அதிகரிக்கின்றது. இதன் காரணமாக வாயுவின் இயக்க ஆற்றலும் அதிகரிக்கும். இயக்க ஆற்றல் அதிகரிப்பின் காரணமாக மூலக்கூறுகள் கொள்கலனின் சுவரில் ஏற்படும் மோதல் அதிகரிக்கிறது. அதன் காரணமாக, குறிப்பிட்ட கன அளவுள்ள நிலையில் வெப்பநிலையை அதிகரிக்கும் போது அழுத்தமும் அதிகரிக்கும்.[6]
கன அளவின் விளைவு
ஒரு வாயுவின் கன அளவு அதைக்கொண்டுள்ள கொள்கலனின் கன அளவிற்குச் சமமாகும். வாயுக்களின் இயக்கவியற் கொள்கைகள் இதனைத் தெளிவுபடுத்துகிறது. கொள்கலத்தின் கன அளவுடன் ஒப்பிடும் போது வாயு மூலக்கூறுகளின் கன அளவு புறக்கணிக்கத்தக்கதாகும். வாயுவின் கன அளவை அதன் அழுத்தம், வெப்பநிலை மற்றும் மோல்களின் எண்ணிக்கை ஆகியவற்றிலிருந்து நிா்ணயிக்கலாம்.[6]
மோல்களின் எண்ணிக்கை
வாயுவின் மீதான அழுத்தம் மற்றும் கன அளவின் விளைவுகள் மோல்களின் எண்ணிக்கையோடு நேர்விகிதத் தொடர்பில் இருக்கும். மோல்களின் எண்ணிக்கை “n' உயரும் போது கொள்கலத்தின் சுவரில் மோதும் மூலக்கூறுகளின் எண்ணிக்கையும் அதிகரிக்கும். இதன் காரணமாக, வாயுவின் அழுத்தம் உயா்கிறது. வாயுவின் மோல்களின் எண்ணிக்கை உயரும் போது அதன் கன அளவும் அதிகரிக்கும்.[6]
அடர்த்தி
அடர்த்தியை குறிக்கப்பயன்படும் குறியீடு ρ (rho) ஆகும். இதன் SI அலகு கிலோகிராம்/கன மீட்டர் ஆகும். வாயு மூலக்கூறுகளானது ஒரு கொள்கலனில் கட்டற்ற முறையில் இயங்குவதால் அதன் நிறையானது அடர்த்தியாலேயே அடையாளப்படுத்தப்படுகிறது. ஒரு பொருளின் அடர்த்தி என்பது ஓரலகு கன அளவுள்ள பொருளின் நிறை எனப்படுகிறது. வாயுக்களைப் பொறுத்தமட்டும் அடர்த்தியானது பரந்துபட்ட அளவெல்லைக்குள் மாறக்கூடியது. ஏனென்றால், வாயு மூலக்கூறுகளானது அழுத்தம் மற்றும் கன அளவு கட்டுப்படுத்தப்பட்ட சூழ்நிலையில் ஒன்றோடு ஒன்று நெருக்கமாக இயங்கும் வாய்ப்புள்ளது. அடர்த்தியில் ஏற்படும் இந்த மாறுபாடானது அமுக்கப்படும் தன்மை (compressibility) என அழைக்கப்படுகிறது. அழுத்தம் மற்றும வெப்பநிலையைப் போன்று அடர்த்தியும் ஒரு நிலையமைவு மாறியாகும்.
நுண்ணியல் பண்புகள்
ஒரு சக்தி வாய்ந்த நுண்ணோக்கியால் வாயுவை ஒருவா் உற்றுநோக்கினால் (மூலக்கூறுகள் அல்லது அணுக்கள் அல்லது அயனிகள்) போன்ற துகள்களின் தொகுப்பைக் காண முடியும். இவை குறிப்பிட்ட வடிவம் மற்றும் கன அளவுக்குட்படாது தாறுமாறான இயக்கத்தில் இருப்பதைக் காணலாம். வாயுவின் துகள்களானது ஒன்றோடொன்று மோதிக்கொள்ளும் போதும் கொள்கலனின் பக்கங்களோடு மோதும் போதும் தங்களது திசையை மாற்றிக்கொள்கின்றன. நல்லியல்பு வாயுவைப் பொறுத்தவரை, இந்த மோதல்கள் முற்றிலும் மீட்சித்தன்மை உடையவை. வாயுவின் அடிப்பைடைத் துகள்களைப் பற்றிய இந்த கருத்தியலானது மூலக்கூறுகளின் இயக்கவியல் கொள்கை எனப்படுகிறது. இந்தக் கொள்கையின் எடுகோள்களை இயக்கவியல் கொள்கை என்ற பகுதியில் காணலாம்.
வாயுக்களின் இயக்கவியற் கொள்கை
இயக்கவிற் கொள்கை யானது வாயுக்களின் அளவிடத்தக்க அல்லது பேரியல் பண்புகளை அவற்றின் மூலக்கூறுகளின் இயைபு மற்றும் இயக்கம் ஆகியவற்றின் வழியாக உள்ளார்ந்து பார்க்கிறது. உந்தம் மற்றும் இயக்க ஆற்றல் ஆகிவற்றின் வரையறையிலிருந்து தொடங்கி,[7] கோண உந்த அழிவின்மை விதி மற்றும் கன சதுரத்தின் வடிவவியல் தொடர்புகள் ஆகியவற்றைப் பயன்படுத்தி வெப்பநிலை, அழுத்தம் ஆகியவற்றை மூலக்கூறு ஒன்றின் இயக்க ஆற்றலேர்ட தொடர்புபடுத்துகிறது. இந்தக் கொள்கையானது இந்த இரு பண்புகளின் சராசரி மதிப்புகளை வழங்குகிறது. மேலும், இந்தக் கொள்கையானது, ஒரு அமைப்பில் உள்ள வாயுவானது எவ்வாறு மாற்றங்களுக்கு தன்னை ஆட்படுத்திக் கொள்கிறது என்பதை விளக்குகிறது. உதாரணமாக, தனிச்சுழி வெப்பநிலையில் உள்ள ஒரு வாயுவானது வெப்பப்படுத்தும் போது அதன் அக ஆற்றலானது உயா்த்தப்படுகிறது. ஒரு வாயுவானது வெப்பப்படுத்தப்படும் போது, அதன் துகள்களின் வேகமானது வெப்பநிலை அதிகரிக்க, அதிகரிக்க அதிகரிக்கிறது. இதன் விளைவாக, மோதல்களின் எண்ணிக்கையானது(மூலக்கூறுகளுக்கிடையேயும், கொள்கலத்தில் சுவா்களோடும்) அதிகரிக்கிறது. ஒரு குறிப்பிட்ட கால இடைவெளிக்குள் ஏற்படும் மோதல்களின் எண்ணிக்கை அதிகரிக்கும் போது அழுத்தமும் அதிகரிக்கப்படுகிறது.
பிரௌணியன் இயக்கம்

பிரௌணியன் இயக்கமானது ஒரு பாய்பொருளின் துகள்களில் ஏற்படும் கட்டற்ற இயக்கத்தை விளக்க முற்படும் கணிதவியல் கோட்பாடாகும். படத்தில் காட்டப்பட்டுள்ள பச்சை மற்றும் இளஞ்சிவப்பு நிற வாயுத்துகள்களின் நகர்படம் வாயுக்களின் விரவல் மற்றும் எண்ட்ரோபி மாற்றத்தை விளக்குகிறது. இந்த நிகழ்வுகளானது துகள் கொள்கையின்படியும் விளக்கப்படுகிறது.
மூலக்கூறுகளுக்கிடைப்பட்ட விசை

மூலக்கூறுகளின் துகள்களுக்கிடையேயான அந்தந்த நேரங்களிலான கவா்ச்சி விசை மற்றும் விலக்க விசைகள் வாயுக்களின் இயக்கவியலில் ஒரு குறிப்பிட்ட தாக்கத்தை விளைவிக்கின்றன. இயற்பிய வேதியியலில் இந்த விசையானது வாண்டர்வால்சு விசை எனவும் அழைக்கப்படுகிறது. இந்த விசையானது பாகியல் தன்மை, இயக்க வீதம் ஆகிய இயற்பியல் பண்புகளை தீா்மானிப்பதில் முக்கிய பங்காற்றுகிறது. சில குறிப்பிட்ட நிலைகளில் இந்த விசைகளை புறக்கணிக்கும் போது ஒரு இயல்பு வாயுவானது நல்லியல்பு வாயுவைப் போன்று கருதப்படுவதை அனுமதிக்கிறது. இந்த அனுமானமானது நல்லியல்பு வாயு விதிகளைப் பயன்படுத்தி பல கணக்கீடுகளை எளிமையாக்க உதவுகிறது.
இந்த விதிகளின் முறையான பயன்பாடானது இயக்கவியல் மூலக்கூறு கொள்கை அவசியமாகிறது. வாயுவின் துகள்களானவை காந்த விசை அல்லது மூலக்கூறுகளுக்கிடையேயான விசையைக் கொண்டிருக்கும் போது அவை தங்களுக்கிடையேயான தொலைவு குறைவதன் காரணமாக ஒரு மூலக்கூறு மற்றொரு மூலக்கூறின் மீது படிப்படியாக தாக்கத்தை உண்டாக்குகிறது.
வளிமம் பற்றிய விதிகள்
பாயில் விதி
1662 ஆம் ஆண்டில் ராபர்ட் பாயில் என்பவர் வாயுக்களின் கன அளவிற்கும், அழுத்தத்திற்கும் உள்ள தொடர்பை பின்வருமாறு கூறினாா். பாயில் விதியானது சில நேரங்களில் பாயில்-மாியோட்டே விதி எனவும் அழைக்கப்படுகிறது.[8] “மாறாத வெப்பநிலையில், ஒரு குறிப்பிட்ட நிறையுள்ள வாாயுவின் அழுதத்தமும் (P), அதன் கன அளவும் (V) ஒன்றுக்கொன்று எதிர்விகிதத் தொடர்பைப் பெற்றுள்ளன.[9][10]
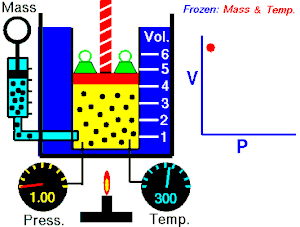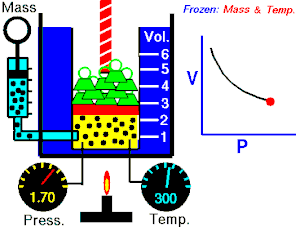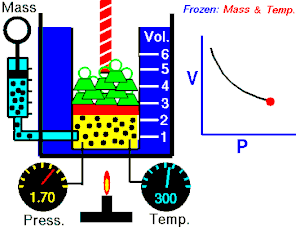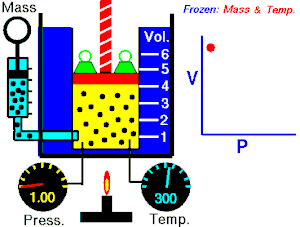
பாயில் விதியானது கணிதவியலின்படி பின்வருமாறு குறிப்பிடப்படலாம்.
அல்லது
P என்பது அழுத்தம், V என்பது கன அளவு , மற்றும் k ஒரு மாறிலி
இந்த சமன்பாட்டிலிருந்து வாயுவின் கன அளவு அதிகரிக்கும் போது வாயுவின் அழுத்தமானது குறைகிறது. இதைப்போன்றே கன அளவு குறையும் போது அழுத்தம் அதிகரிக்கிறது.
சார்லசு விதி
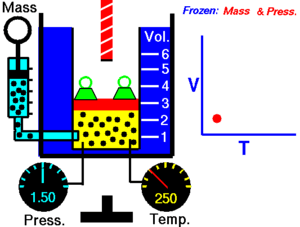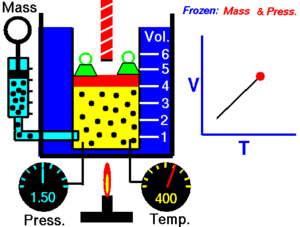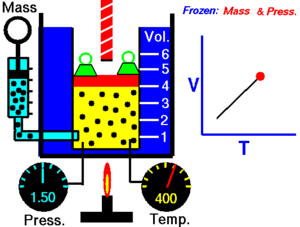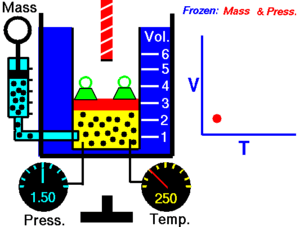
மாறாத அழுத்தத்தில், வெப்ப நிலையைப் பொறுத்து வாயுவின் கன அளவு மாறுபடுவதை சார்லசு விதி விளக்குகிறது
இவ்விதிப்படி, மாறாத அழுத்தத்தில் ஒரு குறிப்பிட்ட நிறையுள்ள வாயுவின் கன அளவு அதன் தனி வெப்பநிலைக்கு நேர் விகிதத்திலிருக்கும்.
இந்தத் தொடர்பானது கணிதவியல் சமன்பாடாக பின்வருமாறு குறிப்பிடப்படுகிறது.
or
where:
- V வாயுவின் கன அளவு,
- T வாயுவின் வெப்பநிலை (கெல்வின் அலகில்),
- k மாறிலி.
இந்த விதியானது வெப்பநிலை அதிகரிக்கும் போது ஒரு வாயு எவ்வாறு விாிவடைகிளது என்பதை விளக்குகிறது. மாறாக, வெப்பநிலையில் ஏற்படும் குறைவானது கன அளவில் குறைவை ஏற்படுத்துகிறது. இரண்டு வேறுபட்ட நிலைகளில் ஒரு பொருளின் நிலைகளை ஒப்பிட இந்த விதியானது பின்வருமாறு எழுதப்படலாம்.
இந்த சமன்பாடானது, தனி வெப்பநிலையானது அதிகரிக்கப்படும் போது வாயுவின் கன அளவு அதிகரிக்கிறது.





