Ebola (betegség)
Az ebola vagy ebola vérzéses láz egy súlyos, magas halálozással járó fertőző betegség, melyet az Ebolavirus nemzetségbe tartozó Ebola-vírusok okoznak, melyek a marburg-vírushoz hasonlóan a Filovírusok (Filoviridae) családjába tartoznak.[2] A betegség eleinte klasszikus vírusfertőzés tüneteivel jelentkezik (pl. láz, izomfájdalmak), majd kialakulnak a vérzéses lázra jellemző tünetek, mint a hasmenés, hányás, fokozott vérzékenység, végül többszervi elégtelenség és keringési sokk alakul ki.[3] Kezelése eleinte nem volt megoldott, specifikus terápia nem állt rendelkezésre, azonban már a 2014-es nyugat-afrikai Ebola-járványt követően sikeresen teszteltek Ebola-ellenes védőoltásokat.[4] A beteg elkülönítése mellett támogató, szupportív kezeléseket (pl. folyadékpótlás) alkalmaznak. A betegség halálozása kezdetben 50-90 százalék körüli volt, de 2019-ben megtalálták és engedélyezték is az ebola ellenszerét, amivel a betegség halálozási rátája 6 százalékra csökkent.[5] Potenciális biológiai fegyvernek tartják, mivel az egyik legvirulensebb emberi kórokozó.[6]
| Ebola | |
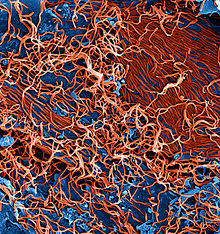
![Az ebolavírus keresztmetszeti képe. A fehérjeburokba zárt RNS-molekula önálló anyagcserére képtelen. A vírus nukleokapszidját a fertőzött sejtek membránjából származó lipidburok veszi körül, amibe beleágyazva virális glikoproteinek találhatók[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/8/87/178-EbolaVirusProteins_EbolaProteins.png/250px-178-EbolaVirusProteins_EbolaProteins.png) | |
| Az ebolavírus keresztmetszeti képe. A fehérjeburokba zárt RNS-molekula önálló anyagcserére képtelen. A vírus nukleokapszidját a fertőzött sejtek membránjából származó lipidburok veszi körül, amibe beleágyazva virális glikoproteinek találhatók[1] | |
| Szinonimák | Ebola vérzéses láz |
| Latinul | Ebola febris haemorrhagica |
| Angolul | Ebola virus disease, Ebola hemorrhagic fever |
| Osztályozás | |
| BNO-10 | A98.4 |
| BNO-9 | 065.8 |
| Főbb tünetek | |
| Adatbázisok | |
| DiseasesDB | 18043 |
| MedlinePlus | 001339 |
| eMedicine | med/626 |
| MeSH ID | D019142 |
A Wikimédia Commons tartalmaz Ebola témájú médiaállományokat. | |
Etimológia

A vírust a Kongói Demokratikus Köztársaság (egykori nevén Zaire) területén található Ebola folyó völgye után nevezték el (a folyót az őslakosság saját nyelvén Legbala néven emlegeti), ami közel található az első 1976-os ismert járványkitöréshez, egy flamand nővérek által vezetett misszionárius kórházhoz Yambuku faluban.[7][8]
Története
A betegség a Kongói Demokratikus Köztársaságban található Ebola folyóról kapta a nevét, ahol először okozott járványt 1976-ban.[9][10] A vírus azóta Afrika különböző pontjain többször is feltűnt, főleg Kelet-Közép-, Közép- és Nyugat-Afrikában, az Ebola és a Kongó folyók környékén, a Kongó területén, a Viktória-tó környékén, Dél-Szudánban, Ugandában, Gabonban, Elefántcsontparton, Guineában, Sierra Leonéban és Libériában. A betegség zoonózis, állatról terjed emberre. Megbetegíti a majmokat és más emlősöket is, azonban a vírus természetes gazdája nem ismert.[11]
A 2014-es Nyugat-afrikai Ebola-járvány a vírus 1976-os azonosítása óta a legsúlyosabb fertőzés mind a megbetegedések, mind az áldozatok számát tekintve.
A kórokozó

A betegség okozói az Ebolavirus nemzetségbe tartozó Ebola-vírusok, melyek közül jelenleg öt ismert.[7] Az Ebola-vírusok a Filovírusok családjába tartoznak, a család másik fontos képviselője az ugyancsak vérzéses lázat okozó Marburg-vírus. A Filovírusok, így az Ebola-vírusok is, lineáris, nem-szegmentált, negatív egyszálú RNS-t tartalmaznak, amihez kovalensen nem kapcsolódnak fehérjék.[7] A virális genom kb. tizenkilenc kilobázis hosszúságú és hét gént tartalmaz, ezek 3'-5' irányban az NP, a VP35, a VP40, a GP, a VP30, a VP24 és az L gének.[12] A különböző típusú Ebola-vírusok nukleotid szekvenciái különböznek egymástól, és változó mennyiségű génátfedést tartalmaznak.
Egy vírust akkor sorolnak az Ebola-vírusok közé, ha a Filovírusok kritériumain kívül az alábbiaknak is megfelel:[7]
- Több génátfedést (angolul gene overlap) is tartalmaz
- A genom negyedik génje (GP) négy fehérjét kódol, a szolubilis glikoprotein (sGP) és az abból proteolítikus hasítással keletkező Δ-peptid az elsődlegesen átírt termékek, míg az ún. tüske glikoproteinek (angolul spike glycoprotein, GP1,2) és a másodlagos szolubilis glikoprotein (ssGP) az elsődlegesen átírt virális RNS módosításával (kotranszkripciós módosítás) jönnek létre
- A fertőzőképesség maximuma a nagyjából 805 nanométer hosszúságú virionok esetén tapasztalható
- A vírus genomja nukleotid szinten legalább 50 százalékban eltér a Marburg-vírusokétól, és legalább 50 százalékban azonos a zairei Ebola-víruséval
- A vírus virionjain található antigének szinte semmilyen keresztreaktivitást nem mutatnak a Marburg-vírusokéval
Szerkezete

Mint minden Filovírus, az Ebola-vírusok virionjai is fonalas szerkezetűek, melyek elektronmikroszkóppal vizsgálva változatos alakban (U, 6, feltekert, kiegyenesedett) láthatóak.[13] A virionok átlagosan 80 nanométer szélesek, a hosszuk változó, az átlagos hosszúságuk 974 és 1086 nanométer közé esik, de sejttenyészetben megfigyeltek már 14,000 nanométer hosszú viriont is.[14] A vírus nukleokapszidját a fertőzött sejtek membránjából származó lipidburok veszi körül, amibe beleágyazva virális glikoproteinek találhatók.
Osztályozása
Az Ebola-vírus és a Marburg-vírus nemzetséget eredetileg a ma már nem létező Filovírus nembe sorolták. 1998 márciusában a Gerincesek Vírusai Albizottság indítványozta a Nemzetközi Vírustaxonómiai Bizottságnál (ICTV), hogy változtassák a Filovírus nemet Filovírus családra, két külön nemzetséggel: Ebola-szerű vírusok és Marburg-szerű vírusok. Az indítványt 2001 áprilisában Washingtonban elfogadták, majd 2002 júliusában Párizsban is. 2000-ben egy Washingtonban készített indítvány eredményeként az Ebola-szerű vírusokból és a Marburg-szerű vírusokból Ebola-vírus és Marburg-vírus lett.
Az Ebolavirus nemzetségbe jelenleg öt faj tartozik, az Ebola-vírus (EBOV, korábban zairei Ebola vírus, ZEBOV), a Szudán-vírus (SUDV, korábban szudáni Ebola vírus, SEBOV), A Taï erdő-vírus (angolul: Taï forest virus, TAFV, korábbi nevén elefántcsontparti Ebola vírus, CIEBOV), a Bundibugyo-vírus (BDBV, korábban Bundibugyo Ebola vírus, BEBOV) és a Reston-vírus (RESTV, korábbi nevén Reston Ebola vírus, REBOV).[7][16] Az ötből négy az emberre veszélyes kórokozó, a Reston-vírus különböző állatokban (sertés, majom) vérzéses lázat okoz, azonban emberi megbetegedést nem idéz elő.[17]
A zairei Ebola-vírus (EBOV; előtte ZEBOV)
- A Zaire-vírus, más néven zairei Ebola-vírus (EBOV) rendelkezik a legnagyobb halálozási aránnyal, ami akár 90 százalékos is lehet, az átlagos halálozási arány körülbelül 83 százalék volt 27 év alatt (1976-2003). A legtöbb járványt ez a típus okozza, az első 1976. augusztus 26-án tört ki Yambukuban.[18] Mabalo Lokela, egy 44 éves tanár volt az első feljegyzett beteg. A tünetek maláriára hasonlítottak, és ennek megfelelően a későbbi páciensek kezelésként kinint kaptak. A fertőzés átvitelét valószínűleg Lokela injekciós tűjének fertőtlenítés nélküli újrahasználata okozhatta. A további fertőzések a nem megfelelő felszerelésnek és nővéri ellátásnak, a hiányos óvintézkedéseknek (pl. gumikesztyű hiánya), illetve a hagyományos temetkezési szertartásoknak volt köszönhető.
A szudáni Ebola-vírus (SUDV; előtte SEBOV)
- Ez a vírus az Ebola második ismert szubtípusa, ami a Zaire-vírussal egy időben jelent meg, és eleinte azzal azonosnak gondolták. Valószínűsíthető, hogy egy pamutgyár dolgozói között jelent meg először a szudáni Nzaraban, annak egyik dolgozója kerülhetett kapcsolatba a vírus hordozójával. A tudósok válaszul több gerinces állat- és rovarfajt is leteszteltek, ennek ellenére egynél sem találták meg a vírust. A hordozó továbbra is ismeretlen, feltehetően denevérek a gazdái.[19] A nem megfelelő nővéri ellátás szintén elősegítette a járvány terjedését. A legutóbbi járványkitörés 2012-ben történt Ugandában.[20]
A restoni Ebola-vírus (RESTV; előtte REBOV)

- Majom-vérzéseslázvírusa (SHFV) által okozott járványkitörés során fedezték fel közönséges makákókban 1989-ben a Hazleton Laboratories létesítményében (napjainkban Covance Laboratories). Az eredeti restoni (Virginia, Egyesült Államok) megjelenését követően felbukkant Pennsylvaniában, Texasban és az olaszországi Siena városában is. A fertőzött állatok minden esetben egy Fülöp-szigeteki intézettől származtak. Később egy Fülöp-szigeteki sertéstelepen sertéseket is megfertőzött.[21][22] Emberek tünetmentesen megfertőződtek ugyan a vírussal, de betegséget egyikükben sem okozott, eddig kizárólag állatokat (majmokat és sertéseket) betegített meg. Ennek ellenére biztonsági szempontból a legmagasabb, négyes szintű organizmusként van besorolva.
Az elefántcsontparti Ebola-vírus (TAFV; előtte CIEBOV)
- A vírust 1994. november 1-jén fedezték fel az elefántcsontparti Taï erdőben, két elpusztult csimpánz tetemének boncolását követően. A boncolás során a szívben barnásan elszíneződött folyékony vért találtak, a szerveken szemmel észlelhető elváltozás nem volt, bár egy másik boncolásnál folyékony vérrel teli tüdőt találtak. A csimpánzszövetek tanulmányozása az 1976-os emberi megbetegedésekhez hasonló eltéréseket mutatott. Később, 1994-ben még több halott csimpánzt fedeztek fel, amikben molekuláris módszerekkel az Ebola-vírus jelenlétét igazolták. A fertőzés forrása valószínűleg a csimpánzok által zsákmányolt vörös kolobuszmajmok (Procolobus badius) húsa lehetett. Az egyik tudós a boncolások során megfertőződött a vírussal, ami után egy héttel a Dengue-lázhoz hasonló tüneteket produkált, majd Svájcba szállították, hogy ott lássák el. Két hét múlva elengedték a kórházból és hat héttel a fertőzés után teljesen felépült.[23]
A bundibugyoi Ebola-vírus (BDBV; előtte BEBOV)

- 2007. november 24-én az Ugandai egészségügyi minisztérium megerősítette egy ebolajárvány kitörését Bundibugyo körzetben. Miután a mintákban a vírus jelenlétét a United States National Reference Laboratories és a CDC is megerősítette, az Egészségügyi Világszervezet bejelentette az új faj létezését. 2008. február 20-án az ugandai kormányzat hivatalosan bejelentette a járvány végét Bundibugyoban, az utolsó fertőzött beteget 2008. január 8-án bocsátották haza.[24] Uganda hivatalosan 116 esetet erősített meg, akik az új fajta Ebola-vírussal fertőződtek, közülük 39-en haltak meg, ami 34 százalékos halálozási arányt jelent.[25] 2012-ben a Kongó Demokratikus Köztársaságban ismét felbukkant a vírus, akkor 77 betegből 36 haláleset történt.[26]
A vírus hordozói, terjesztői

A vírusok természetes hordozója még nem ismert,[11] a legvalószínűbb terjesztői a denevérek lehetnek, de növények és ízeltlábúak is felmerültek. Kiderítették, hogy az 1976-os zairei járvány kiindulási helyének számító pamutgyárban jelentős denevérpopuláció lakott.[19] Egyes nyugat-afrikai országokban, mint Guineában a helyi gasztronómia részét képezi a gyümölcsevő denevérek húsának fogyasztása, mely által szintén terjedhet a vírus.[27] Kísérletesen 19 gerinces és gerinctelen állatot, illetve 24 féle növényt is beoltottak Ebola-vírussal, de az egyedül a denevéreket fertőzte meg.[28] A vírusgazdákra jellemző módon a fertőzött denevérek nem betegedtek meg a vírustól.

Egy 2002 és 2003 között végzett kutatásban 1030 állatot, köztük 679 denevért gyűjtöttek be Gabon és a Kongói Köztársaság területéről, ebből 13 gyümölcsevő denevérben sikerült kimutatni a vírus RNS-ét.[30] Jó néhány gyümölcsevő denevérfajban (Epomops franqueti, Hypsignathus monstrosus, Myonycteris torquata, Micropteropus pusillus, Mops condylurus, Rousettus aegyptiacus) mutatták ki a vírusfertőzés laborjeleit, így jelenleg ezek számítanak a vírus legvalószínűbb természetes rezervoárának.[31][32] Elpusztult főemlősök tetemeiben is kimutatták a vírusokat, azonban a körükben tapasztalt magas halálozás valószínűtlenné teszi őket, mint gazdákat.[19] Az embert minden bizonnyal nem közvetlenül a vírust hordozó denevérek betegítik meg, hanem a vírustól időnként szintén megbetegedő főemlősök, amik kapcsolatba kerülnek az emberrel.[33] A járványok ezt követően az emberek közötti terjedéssel alakulnak ki, azonban a vírus nem képes tartósan fönnmaradni az emberi népességben. Ugyanakkor ismert, hogy a denevéreket a helyi lakosság élelemként is fogyasztja, elsősorban Nyugat-Afrikában.
Patogenezis

A betegség patogenezisére vonatkozóan a legtöbb adat főemlősökön végzett állatkísérletekből származik. A fertőzés korai szakában a vírus elsődleges célpontjai a mononukleáris fagocita rendszer (angolul: Mononuclear phagocyte system, MPS) sejtjei, elsősorban a monociták és dendritikus sejtek, amiken keresztül eljut a lépbe, a májba és a nyirokcsomókba.[34][35] A sejtekbe való bejutásban a vírus felszínén található glikoproteineknek (GP1,2) van a legfontosabb szerepe, amik különböző sejtfelszíni struktúrákhoz (pl. lektinekhez, integrinekhez, a TIM-1 molekulához) kapcsolódnak és a vírus felvételét indító jeleket továbbítanak a sejteknek.[36] A fertőzött immunsejtekben a vírus szaporodik, illetve a sejtek vándorlásával szétterjed a szervezetben. A vírusfertőzött dendritikus sejtek nem aktiválódnak, ami hozzájárul a vírus elleni immunválasz késlekedéséhez, viszont a makrofágokat aktiválja, aminek hatására azok nagy mennyiségű gyulladásos citokint (pl. TNFα, IL-6, IL-8) termelnek,[37] ami a későbbi súlyos szisztémás reakciók kialakulásának egyik legfontosabb, központi lépése.[3][34] Miután ezekben a sejtekben szaporodott, a vírus másodlagos célpontjai a fibroblasztok és az ereket belülről bélelő endotélsejtek, amik a szervezet legkülönfélébb szerveiben is megtalálhatók (pl. here, máj, vese).[38] A vírus közvetlenül is károsítja ezeket a sejteket, amit az aktivált immunsejtek által termelt citokinek hatása tovább fokoz. Mindez végül az érrendszer integritásának megbomlásához, a vazomotor funkciók csökkenéséhez és súlyos véralvadási zavarokhoz vezet.[39]
A filovírusok gyakorlatilag az összes sejttípust képesek megfertőzni,[36] az egyedüli kivételt ez alól a limfociták képezik, amik valószínűleg nem rendelkeznek olyan sejtfelszíni molekulákkal, amik lehetővé tennék a vírus bejutását.[36] Ennek ellenére, a vírusfertőzés indirekt módon a limfociták apoptózisát váltja ki, a betegben limfocitopénia alakul ki.[40] A limfociták fokozott pusztulása meggyengíti az adaptív immunrendszert és hozzájárul a vírussal szembeni immunválasz elégtelenségéhez. Az Ebola-vírus ezenkívül képes meggátolni a vírusfertőzések elleni védekezésben fontos szerepet játszó interferonok termelését és funkcióját.[41]
Külön kiemelendő az ún. Niemann-Pick C1 (NPC1) fehérje szerepe a vírus sejtekbe való bejutásában. A fehérje egy, a sejtek felszínén található koleszterin csatorna, aminek veleszületett mutációja a C típusú Niemann-Pick betegséget okozza, ami egy ritka neurodegeneratív kórkép.[42] Újabb kutatások alapján a fehérje nélkülözhetetlennek tűnik a vírus bejutásához a gazdasejtbe,[43][44] C típusú Niemann-Pick betegek sejtjein végzett in vitro vizsgálatokban a fertőzés nem jött létre. Kimutatták, hogy a fehérje mutációja esetén a virális glikoproteinek képtelenek a virion burkát fuzionáltatni a sejtmembránnal, ami megakadályozza a virális nukleokapszid bejutását a célsejtbe.[44]
A fertőzés módja

A vírus természetben való előfordulása, esetleges átterjedése az emberre részleteiben nem ismert. Valószínűsíthetően fertőzött állattal való érintkezés útján kerülhet át az emberbe. Az emberek közötti terjedése a fertőzött személy vérével vagy más testnedveivel (pl. nyál, ondó) való közvetlen kapcsolat útján történik, vagy a fertőzött orvosi eszközökön keresztül (pl. injekciós tűkkel). A szájon át történő vagy a szem kötőhártyáján keresztüli fertőzés is valószínű, és főemlősökön végzett állatkísérletekben igazolt mechanizmus.[45] Cseppfertőzéssel természetes körülmények között nem terjed, de laboratóriumban létrehozott 0,8-1,2 mikrométer átmérőjű partikulumként fertőzőképes,[46] így a cseppfertőzés potenciális lehetősége miatt A kategóriás biológiai fegyvernek minősül.[47] Aeroszolként állatkísérletekben a zairei Ebola-vírust is fertőzőnek találták.[48]
A vírus terjedését segíthetik a helyi szokások is. Járványt indíthat el a halotti szertartás, mert Afrikában ez együtt jár a halottal való közvetlen érintkezéssel: a halott lemosásával, megcsókolásával stb. Emellett a nem megfelelő higiéniás szabályok, az egészségügyi személyzet által esetenként újrahasznált eszközök is kedveznek a terjedésének.
Tünetek, kórlefolyás
A különböző típusú Ebola-vírusok által okozott megbetegedések klinikai megjelenésüket tekintve némiképp különböznek egymástól. A fertőzés után 2-25 nap lappangási időt követően jelentkeznek a betegség első tünetei. Az átlagos lappangási idő 4-10 nap,[3] a zaire típusú vírusnál egy 2011-es tanulmányban 13 napnak találták.[49] A betegség hirtelen kezdettel, a vírusfertőzésekre általánosan jellemző, influenza-szerű tünetekkel indul, mint a rossz közérzet, láz, fejfájás, torokfájás, izomfájdalom és izomgyengeség. A később megjelenő tünetek utalnak a több szervrendszeri érintettségre, hiszen a torokgyulladás, köhögés, mellkasi fájdalom, nehézlégzés a légzőrendszer, az étvágytalanság, hányinger, hasi fájdalom és a hasmenés az emésztőrendszer, a fejfájás, zavartság, majd a később bekövetkező kóma az idegrendszer, míg a nyálkahártyákon majd a bőrön is megjelenő pontszerű vérzések, a testszerte kialakuló vizenyő és a vérnyomás csökkenése a véralvadás és az érrendszer érintettségét jelzi.[3]
A betegség tetőpontján, az első tünetektől számított 5-7. napon, kialakulnak a vérzéses lázra (febris haemorrhagica) jellemző tünetek.[3] Laboratóriumi módszerekkel mindegyik betegben kimutatható a vérkeringés és véralvadás valamilyen mértékű zavara,[50] a súlyosabb vérzéses tünetek megjelenése azonban kedvezőtlenebb kimenetelt valószínűsít. Az injekciós szúrások helyéről, illetve a nyálkahártyákról (bélrendszer, orr, fogíny, hüvely) származó vérzéseket a betegek 40-50 százalékában tapasztalnak. A bőrön pontszerű bevérzések (petechia), véraláfutások (ecchymosis), nagyobb vérömlenyek (haematoma) a betegek kb. felében vannak jelen.[50] A nyálkahártyavérzésekre utal a véres széklet (melaena), a vérhányás, vagy vér felköhögése a légutakból. A súlyos vérzések ritkák, rendszerint az emésztőrendszerben alakulnak ki.[51] A vérzésekből származó vérveszteség általában nem jelentős, a halált nem ez, hanem az ezzel párhuzamosan kialakuló többszervi elégtelenség (máj, vese) okozza, ami a szervezet folyadékháztartásának felborulása, az alacsony vérnyomás, a véralvadási zavarok (pl. disszeminált intravaszkuláris koaguláció, DIC) és a szövetekben elszórtan kialakuló elhalások (necrosis) következtében alakul ki.[3]
A túlélők teljesen felépülhetnek a betegségből, a gyógyulási fázis azonban hosszú lehet, akár hetekig vagy hónapokig tarthat. A lábadozás alatt gyakori tünet a fejfájás, fogyás, ízületi fájdalmak, hajhullás, a tartós vérszegénység (anaemia).[52] Hetekkel a betegséget követően is kialakulhat a betegben szem-érhártya-gyulladás (uveitis) vagy heregyulladás (orchitis),[53] és még hetekig jelen lehet a beteg testnedveiben (pl. ondó) a vírus.[54]
Diagnosztika
A betegség diagnosztikájában alapvető a pontos anamnézis felvétele, különös tekintettel az olyan részletekre, hogy hol járt és milyen környezeti hatásoknak volt kitéve a beteg (pl. érintkezett-e vadállatokkal). Problémát jelent, hogy a betegség korai fázisában tapasztalt tüneteket sok más betegség is okozhatja, különösen azokon az afrikai területeken, ahol az Ebola is előfordul. Fertőző betegségek közül a többi vírus által okozott vérzéses láz, a Plasmodium falciparum okozta malária, a hastífusz, és a sigellózis is okozhat hasonló tüneteket. Ezek mellett felmerülhet még az akut promielocitás leukémia, hemolitikus urémiás szindróma, kígyómarás vagy a warfarin túladagolás is.[55] Pusztán a klinikai tünetek alapján az Ebolát nem lehet elkülöníteni a Marburg-vírus okozta vérzéses láztól,[3] a végső diagnózist laboratóriumi vizsgálatok szolgáltatják. Ezek közé tartozik az ELISA, mellyel a vírus antigénjeit, vagy a betegben a vírus ellen termelt ellenanyagokat mutatják ki a beteg vérszérumából,[56] vagy a RT-PCR, amivel a vírusra jellemző RNS szakaszok azonosíthatók.[57]
Kezelés

A betegségnek jelenleg nincsen specifikus kezelése, a terápia gyakorlatilag a támogató kezelésekre korlátozódik.[58] Figyelembe véve az érintett területek infrastrukturális és egészségügyi lehetőségeit, ennek biztosítása is komoly kihívást jelenthet.[58] Mivel a betegség kezdeti tünetei nem jellegzetesek és a rendelkezésre álló laboratóriumi háttér is sokszor szegényes, a betegséget eleinte sokszor félrediagnosztizálják, a lázas beteget elkülönítés nélkül antibiotikummal vagy malária ellenes szerrel kezelik.[58]
Ebola esetén a beteget mindenképpen elkülönítik. Tüneti kezelésként fájdalomcsillapítókat, lázcsillapítókat, nyugtatókat, prokoagulánsokat és hányáscsökkentő gyógyszereket alkalmaznak, amennyiben rendelkezésre állnak.[58] A folyadékpótlás a kezelés egyik központi eleme, amennyiben lehetséges, a szájon át történő folyadékbevitelt preferálják, mivel így a vérzékeny és fertőző beteget nem kell megszúrni.[59]
Kísérleti terápiák
Az 1995-ös járványban, ami a Kongói Demokratikus Köztársaságban zajlott, nyolc ebolás tüneteket mutató betegnek a vírus elleni antitesteket tartalmazó vért adtak. A vérkészítmények öt, a fertőzést túlélő, már lábadozó személytől származtak.[60] A nyolc betegből hét túlélte a betegséget, ami a szokásos halálozási aránynál jóval kedvezőbbnek tűnt.[60] Az antitestekkel végzett állatkísérletek ígéretes, de némiképp ellentmondásos eredményeket hoztak idáig,[3] ugyanis nem minden fajból nyert antitestek védték meg a főemlősöket a kísérletekben, többek között egy rekombináns humán antitest is hatástalannak bizonyult.[61]
Brincidofovir
ZMapp
2014 augusztusában a nyugat-afrikai járvány során megfertőzött két amerikai betegnek kísérleti jelleggel egy fejlesztés alatt álló, akkor még hivatalosan nem bejegyzett ZMapp nevű gyógyszert adtak, ami három monoklonális antitest keverékét tartalmazta.[62] A szert korábban emberben még nem tesztelték, a rendkívüli helyzetre való tekintettel alkalmazták a két betegnél. Az eddig nyilvánosságra került adatok alapján a szer hatásos volt.[63]
cAd3-ZEBOV
Egy másik terápiás megközelítés a virális RNS-polimeráz enzimet kódoló L gén semlegesítése, melyhez az RNS-interferencia jelenségét próbálják kihasználni. Főemlősökön végzett állatkísérletekben a módszert hatásosnak találták.[64] Egy másik, 2010-ben megjelent tanulmányban a VP24 és VP35 ellen tervezett foszforodiamidát-morfolino oligomereket (PMO) vizsgáltak, amelyek rágcsálókban és makákókban is hatásosnak bizonyultak.[65]
TKM-Ebola
A kutatók eltérő hatásmechanizmusú, az ebola betegséget gyógyszerrel legyőző terápiával kísérleteznek. Ezek közül nagyon ígéretes a kanadai Tekmira Pharmaceuticals cég TKM-Ebola nevű szere. A gyógyszer kikapcsolja az Ebola-vírusnak azokat a génjeit, amelyek az RNS-interferenciáért felelősek.[66]
Megelőzése

Hatékony kezelés híján a fertőzés megelőzése alapvető fontosságú. A betegek és a betegségben elhunytak testnedvei fertőzőek, a velük való közvetlen érintkezés kerülendő, ezért a betegség lehetőségére az ellátóknak minél előbb gondolniuk kell, és aszerint kell a beteggel bánniuk. A betegeket el kell különíteni, a személyzet megfelelő védőfelszerelésekkel (védőruha, védőszemüveg, kesztyű) ellátva érintkezhet csak a beteggel. A rendszeres kézmosást és fertőtlenítést is fontosnak tartják, ugyanakkor cikkekben arról számolnak be a kint dolgozó egészségügyi szakemberek, hogy erre nehéz rábeszélni a helyieket, hiszen sokszor még elegendő ivóvíz sem áll a rendelkezésükre.[67] Részben a szükséges eszközök, részben a nem megfelelő higiéniás gyakorlat miatt a nagyobb járványok általában a szegényebb, elmaradottabb területeken alakultak ki, ahol nem álltak rendelkezésre jól felszerelt kórházak illetve jól képzett egészségügyi dolgozók. A helyi temetkezési szokások, különösen amik balzsamozással is járnak, szintén elősegíthetik a járványok terjedését, mivel az abban résztvevők közvetlen kapcsolatba kerülnek a holttestekkel. A tetemeket gyorsan és biztonságosan (vízhatlan zsákban, mésszel) kell eltemetni, még akkor is, ha az ellenkezik az adott nép temetkezési szokásaival.
Védőoltás
Az Ebola ellen sokáig nem állt rendelkezésre hatékony védőoltás.[68][69] Többféle megközelítéssel is próbálkoztak, ezek közül a DNS-vakcinák tűntek a legígéretesebbnek. Az egyik kutatásban virális fehérjéket kódoló plazmidokkal oltottak be majmokat, amikkel a kísérleti állatokban sikerült védettséget elérniük.[70] Ezenkívül kísérletekben használtak többek között adenovírusokat is, mint Ebola-vírus fehérjéket kódoló vektorokat.[71] A védőoltások hatékonyságát és biztonságosságát emberekben még vizsgálják.[72]
A 2014-es nyugat-afrikai Ebola-járvány nagy nemzetközi pánikot keltett és felgyorsította az Ebola-ellenes védőoltások fejlesztését. Ennek eredményeként több, nyugaton kifejlesztett vakcinát is sikeresen teszteltek a térségben. Az egyik oltás egy rekombináns vezikuláris sztomatitisz vírust (rVSV) tartalmaz, melyben megtalálható a ZEBOV egyik felszíni glikoproteinje, ami az oltott egyénben utóbbi ellen immunválaszt vált ki. A vakcinát Guineában tesztelték, 7651 ember bevonásával, és 100 százalékos hatékonyságot tapasztaltak, 6 nappal az oltás beadását követően az oltott egyének közül senki sem betegedett meg.[4] A kísérleti védőoltás sikeréről 2015 júliusában az Egészségügyi Világszervezet is beszámolt.[73]
Eddig regisztrált ebolás megbetegedések
| Év | Ország | Típus | Emberi megbetegedések száma | Halálesetek | Halálozás (%) | Rövid leírás |
|---|---|---|---|---|---|---|
| 1976 | Kongó (volt Zaire) | ZEBOV | 318 | 280 | 88% | Yambukuban és környékén zajlott. A betegség közvetlen érintkezéssel és fertőzött orvosi eszközök használatával terjedt. A vírus első dokumentált megjelenése.[18] |
| 1976 | Szudán | SEBOV | 284 | 151 | 53% | Nzara és Maridi környékén fordult elő. A betegek közvetlen érintkezésével terjedt a kórházakban. Az ellátók közül is többen megbetegedtek.[74] |
| 1977 | Zaire (Kongói Demokratikus Köztársaság) | ZEBOV | 1 | 1 | 100% | Tandala faluból utólagosan jelentett eset.[75] |
| 1979 | Szudán | SEBOV | 34 | 22 | 65% | Ismét Nzara és Maridi városokban alakult ki, ahol a korábbi szudáni járvány is zajlott.[76] |
| 1989 | Amerikai Egyesült Államok | REBOV | 0 | 0 | 0% | Reston-vírussal fertőzött Fülöp-szigetekről importált majmokból izolálták a vírust Virginában és Pennsylvaniában.[77] |
| 1990 | Amerikai Egyesült Államok | REBOV | 4 (tünetmentes) | 0 | 0% | Ismét a Fülöp-szigetekről származó fertőzött majmokat különítettek el Virginiában és Texasban. Négy emberben kimutatták a vírus ellen termelt ellenanyagokat, de egyikük sem betegedett meg.[78] |
| 1989–1990 | Fülöp-szigetek | REBOV | 3 (tünetmentes) | 0 | 0% | A közönséges makákók körében magas halálozással járó megbetegedés tört ki abban az intézményben, ahonnan az USA-ba került állatok is származtak.[79] Három dolgozóban kimutattak vírus ellenes ellenanyagokat, de egyikük sem betegedett meg.[80] |
| 1992 | Olaszország | REBOV | 0 | 0 | 0% | Reston-vírussal fertőzött majmokat különítettek el Sienában. A majmok ugyanabból a Fülöp-szigeteki intézményből származtak, ahonnan az USA-ba is fertőzött állatok kerültek. Emberi fertőzés nem történt.[81] |
| 1994 | Gabon | ZEBOV | 52 | 31 | 60% | Mékoukában és más, mélyen az esőerdőben található aranybányák területén alakult ki. Eleinte sárgaláznak gondolták, 1995-ben ebolaként azonosították.[82] |
| 1994 | Elefántcsontpart | CIEBOV | 1 | 0 | 0% | Egy vad csimpánzt boncoló kutató betegedett meg a Taï erdőben. A beteget Svájcban látták el.[23] |
| 1995 | Zaire (Kongói Demokratikus Köztársaság) | ZEBOV | 315 | 250 | 79% | Kikwit városában fordult elő. A járvány egy az erdőben dolgozó munkástól indult, majd a családján és a kórházi betegeken keresztül terjedt.[83] |
| 1996. január–április | Gabon | ZEBOV | 37 | 21 | 57% | Mayibout környékén fordult elő. Egy, az erdőben talált elpusztult csimpánzt ettek a helyiek. 19, az állatot feldolgozó ember betegedett meg, a többi fertőzés az ő családtagjaikban alakult ki.[82] |
| 1996. július – 1997. január | Gabon | ZEBOV | 60 | 45 | 75% | Booué-ban tört ki, a forrása egy erdőben dolgozó vadász volt. A betegség a fertőzött személyekkel való közvetlen érintkezéssel terjedt. Egy vírussal fertőzött elpusztult csimpánzt találtak az erdőben.[82] |
| 1996 | Dél-afrikai Köztársaság | ZEBOV | 2 | 1 | 50% | Egy egészségügyi szakember visszatért Johannesburgba, miután ebolás betegeket látott el Gabonban. Megbetegedett, elkülönítették, az őt ápoló nővér megfertőződött és meghalt.[84] |
| 1996 | Amerikai Egyesült Államok | REBOV | 0 | 0 | 0% | Reston-vírussal fertőzött Fülöp-szigetekről származó majmokat különítettek el Texas államban. Emberi fertőzés nem történt.[85] |
| 1996 | Fülöp-szigetek | REBOV | 0 | 0 | 0% | Egy majmokat exportáló intézményben azonosították a Reston vírust. Emberei fertőzés nem történt.[86] |
| 2000–2001 | Uganda | SEBOV | 425 | 224 | 53% | Gulu, Masindi és Mbara megyékben tört ki járvány. A fertőzés szempontjából legnagyobb kockázatot a betegek temetésén való részvétel, a fertőzött családtaggal való érintkezés, és a fertőzött beteg megfelelő óvintézkedések nélküi ellátása jelentette.[87] |
| 2001. október – 2002. március | Gabon | ZEBOV | 65 | 53 | 82% | Gabon és a Kongói Köztársaság határán tört ki járvány.[88] |
| 2001. október – 2002. március | Kongói Köztársaság | ZEBOV | 57 | 43 | 75% | Gabon és a Kongói Köztársaság határán tört ki ismét járvány. Első alkalommal jelentettek megbetegedést Kongóból.[88] |
| 2002. december –2003. április | Kongói Köztársaság | ZEBOV | 143 | 128 | 90% | Cuvette Ouest régió Mbomo és Kéllé megyéjében alakult ki járvány.[89] |
| 2003. november–december | Kongói Köztársaság | ZEBOV | 35 | 29 | 83% | Mbomo megye Mbomo és Mbandza falujában történtek megbetegedések.[90] |
| 2004 | Szudán | SEBOV | 17 | 7 | 41% | A dél-szudáni Yambo megyében jelent meg a betegség. Az ebolával egy időben és helyen kanyaró járvány is volt, utólag sok ebolásnak vélt esetről kiderült, hogy valójában a kanyaró okozta a betegséget.[91] |
| 2007 | Kongói Demokratikus Köztársaság | ZEBOV | 264 | 187 | 71% | A járvány a Nyugat-Kasai tartományban tört ki.[92] |
| 2007. december – 2008. január | Uganda | BDBV | 149 | 37 | 25% | A járvány a nyugat-ugandai Bundibugyo megyében tört ki. A Bundibugyo-vírus (BDBV) első leírása.[25] |
| 2008. november | Fülöp-szigetek | REBOV | 6 (tünetmentes) | 0 | 0% | Fülöp-szigeteki járvány, az első eset, hogy a vírust sertésekben észlelték. A sertéstelep hat dolgozójában kimutatták a Reston-vírus ellenes ellenanyagokat, de egyikük sem betegedett meg.[21][22] |
| 2008. december – 2009. február | Kongói Demokratikus Köztársaság | ZEBOV | 32 | 14 | 45% | A Nyugat-Kasai tartományban található Mwekában és Lueboban alakult ki járvány.[93] |
| 2012. június–augusztus | Uganda | SEBOV | 24 | 17 | 71% | A nyugat-ugandai Kibale megyében jelentettek ebolás megbetegedéseket.[20] |
| 2012. június–november | Kongói Demokratikus Köztársaság | BDBV | 77 | 36 | 47% | Az Orientale tartományban tört ki járvány.[26][94] |
| 2013. december– | Guinea Libéria Sierra Leone Nigéria Szenegál | ZEBOV | 25500 | 10500 | 49% | Az eddigi legnagyobb ebola járvány jelenleg is tart Guineában, és átterjedt a szomszédos államok közül Sierra Leonéba, Libériába, Nigériába és Szenegálba is.[95] |
| 2014. augusztus–november | Kongói Demokratikus Köztársaság | SEBOV | 66 | 49 | 76% | Az Egyenlítői tartományban tört ki járvány, a WHO álláspontja szerint a nyugat-afrikai járvánnyal nincs kapcsolatban.[96] |
| 2021. január-február | Guinea | Az egyik áldozata a járványnak egy ápolónő volt, aki 2021. január végén kapta el a betegséget és február elsején volt a temetése. A temetés után néhány nappal több jelenlévőnél is mutatkoztak a tünetek, amiket laboratóriumi vizsgálat meg is erősített.[97] |
Jegyzetek
Források
- Ádám-Béládi-Gergely-Kétyi-Nász-Pusztai-Szabó: Orvosi mikrobiológia, egyetemi tankönyv, Budapest, Semmelweis Kiadó, 1993
- Balázsy Sándor-Naár Zoltán: Mikrobiológiai alapok, főiskolai tankönyv, Nyíregyháza, Bessenyei György Könyvkiadó, 2003 ISBN 963-9385-70-0
- Jurányi Róbert-Vogronics Péterné: Mikrobiológiai és parazitológiai gyakorlatok, Budapest Medicina, 2002 ISBN 963-242-681-9
- Michael B.A. Oldstone: Vírusvadászok, Typotex, 2002 ISBN 963-9326-18-6
- Axmann Ágnes: Fertőző és trópusi betegségek, amelyek előfordulhatnak egzotikus utazásaink során, Budapest, Alexandra, 2002 ISBN 963-368-198-7
- Richard Preston: Halálzóna – Ebola: a gyilkos vírus, Budapest, Európa Könyvkiadó, 1995 ISBN 963-07-5832-6 – A restoni víruskitörés története
- Klenk, Hans-Dieter. Marburg and Ebola Viruses (Current Topics in Microbiology and Immunology) (angol nyelven). Berlin: Springer-Verlag Telos (1999. január 1.). ISBN 978-3-540-64729-4
- Ebola and Marburg viruses: molecular and cellular biology (Limited preview) (angol nyelven), Wymondham, Norfolk, UK: Horizon Bioscience (2004). ISBN 978-0-9545232-3-7
- Kuhn, Jens H.. Filoviruses: A Compendium of 40 Years of Epidemiological, Clinical, and Laboratory Studies. Archives of Virology Supplement, vol. 20 (Limited preview) (angol nyelven), Vienna: SpringerWienNewYork (2008). ISBN 978-3-211-20670-6
- Level 4: Virus Hunters of the CDC (Limited preview), Horvitz, Leslie Alan, Updated [3rd] (angol nyelven), Barnes & Noble [1996] (1999. June). ISBN 978-0-7607-1208-5−
- Pattyn, S. R.. Ebola Virus Haemorrhagic Fever [archivált változat] (Full free text), 1st (angol nyelven), Amsterdam: Elsevier/North-Holland Biomedical Press (1978). ISBN 0-444-80060-3. Hozzáférés ideje: 2010. december 11. [archiválás ideje: 2010. december 11.] Archiválva 2010. december 11-i dátummal a Wayback Machine-ben−
- Ebola and Marburg Viruses: A View of Infection Using Electron Microscopy (angol nyelven). Columbus, Ohio: Battelle Press (2004). ISBN 978-1-57477-131-2
Kapcsolódó szócikkek
További információk
- Centers for Disease Control and Prevention – Cdc.gov
- Kétyi I 2001. Két „egzotikus” vírus: a Marburg és az Ebola Archiválva 2013. március 19-i dátummal a Wayback Machine-ben – Természet Világa, 132. évf. 6. sz. (2001. június), 275. o.
- Kávéstermoszban érkezett az ebolás vér Európába – Megszólalt a felfedező Archiválva 2014. augusztus 14-i dátummal a Wayback Machine-ben – Válasz.hu, 2014. augusztus 12.
| Az itt található információk kizárólag tájékoztató jellegűek, nem minősülnek orvosi szakvéleménynek, nem pótolják az orvosi kivizsgálást és kezelést. A cikk tartalmát a Wikipédia önkéntes szerkesztői alakítják ki, és bármikor módosulhat. |



