Hidrazin
Hidrazin (diazan) neorgansko jedinjenje je sa formulom N2H4. On je bezbojna zapaljiva tečnost sa mirisom sličnom amonijaku. Hidrazin je veoma toksičan i veoma je nestabilan, osim ako se njime rukuje u rastvoru. Godine 2002. je proizvedeno oko 260.000 tona.[12] Hidrazin se uglavnom koristi kao agens za formiranje pene u pripremi polimernih pena, a nalazi i znatnu primenu kao prekurzor za polimerizacione katalizatore i lekove. Osim toga, hidrazin se koristi u raznim raketnim gorivima i za pripremu gasnih prekurzora koji se koriste u vazdušnim jastucima. Hidrazin se koristi u nuklearnim i konvencionalnim električnim centralama u sistemima vodene pare kao sakupljač kiseonika, kojim se kontrolišu koncentracije rastvorenog kiseonika radi redukovanja korozije.
| |||
| |||
 Hydrazine hydrate | |||
| Nazivi | |||
|---|---|---|---|
| Sistemski IUPAC naziv Hidrazin[2] | |||
| Drugi nazivi | |||
| Identifikacija | |||
3D model (Jmol) | |||
| 3DMet | B00770 | ||
| Bajlštajn | 878137 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.560 | ||
| EC broj | 206-114-9 | ||
| Gmelin Referenca | 190 | ||
| KEGG[3] | |||
| MeSH | Hydrazine | ||
| RTECS | MU7175000 | ||
| UNII | |||
| UN broj | 2029 | ||
| |||
| Svojstva | |||
| N 2H 4 | |||
| Molarna masa | 32,0452 g mol−1 | ||
| Agregatno stanje | Bezbojna tečnost | ||
| Gustina | 1,021 g cm−3 | ||
| Tačka topljenja | 2 °C; 35 °F; 275 K | ||
| Tačka ključanja | 114 °C; 237 °F; 387 K | ||
| log P | 0,67 | ||
| Napon pare | 1 kP (na 30,7°C) | ||
| Kiselost (pKa) | 8,10[6] | ||
| Baznost (pKb) | 5,90 | ||
| Indeks refrakcije (nD) | 1,46044 (na 22°C) | ||
| Viskoznost | 0,876 cP | ||
| Struktura | |||
| Oblik molekula (orbitale i hibridizacija) | Trougano piramidalni na N | ||
| Dipolni moment | 1,85 D[7] | ||
| Termohemija | |||
| Standardna molarna entropija S | 121,52 J K−1 mol−1 | ||
Std entalpija formiranja (ΔfH⦵298) | 50,63 kJ mol−1 | ||
| Opasnosti | |||
| Bezbednost prilikom rukovanja | ICSC 0281 | ||
| GHS grafikoni |      | ||
| GHS signalna reč | Opasnost | ||
| H226, H301, H311, H314, H317, H331, H350, H410 | |||
| P201, P261, P273, P280, P301+310, P305+351+338 | |||
EU klasifikacija (DSD) | |||
| R-oznake | R45, R10, R23/24/25, R34, R43, R50/53 | ||
| S-oznake | S53, S45, S60, S61 | ||
| NFPA 704 | |||
| Tačka paljenja | 52 °C (126 °F; 325 K) | ||
| 24 to 270 °C (75 to 518 °F; 297 to 543 K) | |||
| Eksplozivni limiti | 1.8–99.99% | ||
| Letalna doza ili koncentracija (LD, LC): | |||
LD50 (LD50) | 59–60 mg/kg (oralno u pacovima, miševima)[10] | ||
LC50 (LC50) | 260 ppm (pacov, 4 hr) 630 ppm (pacov, 1 hr) 570 ppm (pacov, 4 hr) 252 ppm (miš, 4 hr)[11] | ||
| SAD zdravstvene granice izlaganja (NIOSH): | |||
PEL (dozvoljivo) | TWA 1 ppm (1.3 mg/m3) [koža][9] | ||
REL (preporučeno) | Ca C 0.03 ppm (0.04 mg/m3) [2-sata][9] | ||
IDLH (neposredna opasnost) | Ca [50 ppm][9] | ||
| Srodna jedinjenja | |||
Srodna jedinjenja | Amonijak | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
| Reference infokutije | |||
Molekulska struktura i osobine
Hidrazin formira monohidrat koji ima veću gustinu (1,032 g/cm3) od anhidratnog materijala.
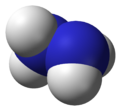
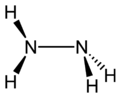
Hidrazin se može formirati iz dva molekula amonijaka uklanjanjem jednog vodonika po molekulu. Svaka H2N-N podjedinica je piramidalnog oblika. N-N rastojanje je 1,45 Å (145 pm), i molekul poprima gauche konformaciju.[13] Rotaciona barijera dva puta veća od etana. Ova strukturna svojstva su slična gasovitom vodonik peroksidu, koji poprima zakrivljenu antiklinalnu konformaciju, i takođe ima jaku rotacionu barijeru.
Hidrazin ima bazna (alkalna) hemijska svojstva, slična amonijaku:
- N2H4 + H2O → [N2H5]+ + OH−
sa vrednostima:[14]
- Kb = 1,3 x 10−6
- pKa = 8,1
(za amonijak Kb = 1,78 x 10−5)
Hidrazin se teško deprotonuje:[15]
- [N2H5]+ + H2O → [N2H6]2+ + OH− Kb = 8.4 x 10−16
Toplota sagorevanja hidrazina u kiseoniku (vazduhu) je 194,1 x 105 J/kg (9345 BTU/lb).[16]
Reference
Literatura
- Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. стр. 361. ISBN 978-1-903996-65-2.
Vidi još
Spoljašnje veze
- The Late Show with Rob! Tonight’s Special Guest: Hydrazine (PDF) – Robert Matunas
- Hydrazine - chemical product info: properties, production, applications.
- Hydrazine toxicity
- CDC - NIOSH Pocket Guide to Chemical Hazards