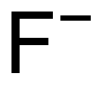புளோரைடு
புளோரைடு (Fluoride /ˈflʊəraɪd/ [3] /ˈflɔːraɪd/ /ˈflɔːraɪd/)[3]) என்பது F− என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட புளோரினின் ஒற்றை அணு எதிர்மின் அயனியாகும். இதனுடைய உப்புகளும் கனிமங்களும் வேதியியலில் முக்கியமான வினைப்பொருள்களாகவும் தொழிற்சாலை வேதிப்பொருள்களாகவும் கருதப்படுகின்றன. புளோரோ கார்பன்களுக்கான ஐதரசன் புளோரைடை உற்பத்தி செய்யப் பயன்படுவது இதனுடைய பிரதான பயனாகக் கருதப்படுகிறது. புளோரைடு அயனியின் மின்சுமை மற்றும் அளவை ஒப்பிடுகையில் இது ஐதராக்சைடு அயனியின் மின்சுமை மற்றும் அளவை ஒத்ததாக உள்ளது. பூமியில் பல்வேறு கனிமங்கள் வடிவில் புளோரைடு அயனி கிடைக்கிறது என்றாலும் குறிப்பாக புளோரைட்டாக அதிக அளவில் கிடைக்கிறது. தண்ணீரில் மிகச்சிறிதளவே இது காணப்படுகிறது. தனித்துவமான கசப்புச் சுவையைக் கொண்ட புளோரைடு அயனி அதன் உப்புகளுக்கு எந்தவிதமான நிறத்தையும் அளிப்பதில்லை.
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர் புளோரைடு[1] | |||
| இனங்காட்டிகள் | |||
| 16984-48-8 | |||
| ChEBI | CHEBI:17051 | ||
| ChEMBL | ChEMBL1362 | ||
| ChemSpider | 26214 | ||
Gmelin Reference | 14905 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | C00742 | ||
| ம.பா.த | புளோரைடு | ||
| பப்கெம் | 28179 | ||
SMILES
| |||
| பண்புகள் | |||
| F− | |||
| வாய்ப்பாட்டு எடை | 19.00 g·mol−1 | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH | −333 கியூ மோல்−1 | ||
| நியம மோலார் எந்திரோப்பி S | 145.58 யூல்/மோல் K (வாயு நிலை)[2] | ||
| தொடர்புடைய சேர்மங்கள் | |||
| ஏனைய எதிர் மின்னயனிகள் | |||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| Infobox references | |||
பெயரிடல்
புளோரைடு அயனிகளைக் கொண்டுள்ள சேர்மங்களிலிருந்து புளோரைடு அயனிகள் பிரிகை அடைவதில்லை. புளோரைடுகளுக்கு இடப்படும் பெயர்கள் இந்த சூழலை வேறுபடுத்துவதில்லை. உதாரணமாக கந்தக எக்சாபுளோரைடு மற்றும் கார்பன் டெட்ராபுளோரைடு சேர்மங்கள் சாதாரண நிபந்தனைகளில் புளோரைடு அயனிகளுக்கான ஆதாரமூலமாக இருப்பதில்லை. ஐயுபிஏசி பெயரிடும் முறையில் இதற்கு முறையான பெயராக வைக்கப்பட்டிருப்பது புளோரைடு என்ற பெயராகும்.ஐயுபிஏசி இன் சேர்க்கைப் பொருள்களுக்கான பெயரிடல் அடிப்படையில் இப்பெயர் தீர்மானிக்கப்பட்டுள்ளது. இருப்பினும், பிணைப்பில் கவனம் செலுத்தாத ஐயுபிஏசி இன் கூட்டமைவு பெயரிடலிலும் இப்பெயர் பயன்படுத்தப்படுகிறது, கரையும்போது புளோரைடை வெளியிடுகின்ற சேர்மங்களை விவரிக்கவும் புளோரைடு என்ற பெயர் பயன்படுத்தப்படுகிறது, ஐதரசன் புளோரைடு என்ற பெயரும் முறைப்படுத்தப்படாத பெயரிடும் திட்டத்தின் ஒரு பெயராகும்.
தோற்றம்

இயற்கையில் பல புளோரைடு கனிமங்கள் அறியப்படுகின்றன, ஆனால் மிக முக்கியமான வர்த்தக முக்கியத்துவம் கொண்டிருப்பது புளோரைட்டு (CaF2) என்ற கனிமம் ஆகும், கிடைக்கும் புளோரைடு கனிம எடை அளவில் இது 49% என்பது குறிப்பிடத்தக்கதாகும். மென்மையான, வண்ணமயமான இக்கனிமம் உலகம் முழுவதும் காணப்படுகிறது
மிகவும் புதிய மற்றும் உப்புநீர் ஆதாரங்களில் குறைவான செறிவுடன் புளோரைடு இயற்கையாகவே காணப்படுகிறது. கடல்நீரில் பொதுவாக 0.86 முதல் 1.4 மி.கி / லிட்டர் என்ற வரம்பில் சராசரியாக 1.1 மி.கி / லிட்டர் என்ற அளவில் புளோரைடு காணப்படுகிறது [4].
ஒப்பீட்டளவில் கடல்நீரில் குளோரைடின் செறிவு சுமார் 19 கிராம் / லிட்டர் ஆகும். புளோரைடின் இக்குறைவான செறிவானது காரமண் புளோரைடு வகைச் சேர்மங்களின் கரைதல் தன்மையில் பிரதிபலிக்கிறது. உதாரணம்: CaF2 புத்தம் புதிய நீரில் உள்ள புளோரைடு அயனியின் அடர்த்தி குறிப்பிடத்தக்க அளவில் வேறுபடுகிறது. நதிகள் அல்லது ஏரிகள் போன்ற மேற்பரப்பு நீரில் பொதுவாக 0.01-0.3 பிபிஎம் அதாவது மில்லியன் பகுதிகளுக்கு இத்தனை பகுதிகள் என்ற அளவில் காணப்படுகிறது [5].
நிலத்தடி நீரில் இந்த அடர்த்தி மேலும் வேறுபடுகிறது. அவ்விடத்தில் காணப்படும் புளோரைடு கனிமங்களைப் பொறுத்து இந்த அடர்த்தி மாறுபடுகிறது. உதாரணமாக கனடாவின் சில பகுதிகளில் 0.05 மி.கி / லிட்டர் எனவும் சீனாவின் சில பகுதிகளில் 8மி.கி /லிட்டர் எனவும் மாறுபடுவது கண்டறியப்பட்டுள்ளன. பொதுவான மட்டங்களில் புளோரைடு அயனியின் செறிவு அரிதாக10மி.கி /லிட்டர் எனவும் கண்டறியப்பட்டுள்ளது [6].
- தான்சானியா போன்ற சில நாடுகளில் குடிநீரில் அபாயகரமான அளவுக்கு மேல் புளோரைடு கலந்துள்ளது. இதனால் அங்கெல்லாம் கடுமையான உடல்நலக் கேடுகள் உண்டாகின்றன.
- உலக அளவில் 50 மில்லியனுக்கும் அதிகமான மக்கள் தண்ணீர் ஆதார மூலங்களிலிருந்து குடி தண்ணீரைப் பெறுகின்றனர், அவற்றில் இயற்கையாகவே "உகந்த நிலைக்கு" நெருக்கமாக புளொரைடு உள்ளது [7].
- பிற பகுதிகளில் கிடைக்கும் புளோரைடின் அளவு மிகக் குறைவு ஆகும். எனவே புளோரினேற்றம் செய்து அந்நீரின் புளோரைடு அளவை கிட்டத்தட்ட மில்லியனுக்கு 0.7-1.2 பகுதிகள் வரை உயர்த்த வேண்டியுள்ளது.
அனைத்து தாவரங்களிலும் சிறிதளவு புளோரைடு காணப்படுகிறது. மண் மற்றும் தண்ணீரிலிருந்து இப்புளோரைடு உறிஞ்சப்படுகிறது.சில தாவரங்கள் தங்கள் சூழலில் இருந்து புளோரைடை ஈர்த்துக் கொள்கின்றன. அனைத்து வகையான தேநீர் இலைகளிலும் புளோரைடு காணப்படுகிறது. இருப்பினும், முதிர்ந்த இலைகளில் அதே தாவரத்தின் இளம் இலைகளில் இருப்பதைக்காட்டிலும் 10 முதல் 20 மடங்கு புளோரைடு அதிகமாகக் காணப்படுகிறது [8][9][10].
வேதிப்பண்புகள்
காரத்தன்மை
புளோரைடு ஒரு காரத்தைப் போல செயற்படும் தன்மை கொண்டது ஆகும். இது புரோட்டானுடன் (H+) சேர்ந்து சேர்மங்களை உருவாக்கும்.
F− + H+ → HF
இந்த நடுநிலையாக்கல் வினையில் புளோரைடின் இணை அமிலமான ஐதரசன் புளோரைடு உருவாகிறது.நீரிய கரைசலில் புளோரைடின் pKb மதிப்பு10.8 ஆகும். எனவே இது ஒரு வலிமை குறைந்த காரமாகும். வலிமை குறைந்த காரமாக இருப்பதால் போதுமான அளவுக்கு ஐதரசன் புளோரைடாக மாறுவதற்குப் பதிலாக புளோரைடு அயனியாக தொடர்ந்து இருக்க முயல்கிறது. தண்ணீரில் இதன் வேதிச்சமநிலை பின்வரும் சமன்பாட்டில் இடது பக்கத்தில் காட்டப்படுகிறது.
- F− + H2O
 HF + HO−
HF + HO−
இருப்பினும், தொடர்ச்சியாக ஈரப்பதத்துடன் நீடித்திருக்கும் தொடர்பில், கரையக்கூடிய புளோரைடு உப்புகள் தொடர்புடைய ஐதராக்சைடு அல்லது ஆக்சைடாக சிதைவடைகின்றன. ஐதரசன் புளோரைடு வெளியேறுகிறது. ஆலைடுகளில் புளோரைடு மட்டும் இத்தனித்துவப் ப்ண்பை பின்பற்றுகிறது. கரைப்பானின் தன்மைக்கேற்ப வேதிச்சமநிலையை வலதுபுறத்திற்கு மாற்றுவதில் ஒரு வியத்தகு விளைவைக் கொண்டிருப்பதாக் சிதைவு விகிதம் பெரிதும் அதிகரிக்கிறது.
புளோரைடு உப்புகளின் கட்டமைப்பு
புளோரைடைப் பெற்றிருக்கும் உப்புகள் ஏராளமான மற்றும் எண்ணற்ற வேதியியல் கட்டமைப்புகளை ஏற்றுகொள்கின்றன. குறிப்பாக புளோரைடு எதிர்மின் அயனி நான்கு அல்லது ஆறு நேர்மின் அயனிகளால் சூழப்பட்டிருக்கிறது. சோடியம் புளொரைடும் சோடியம் குளோரைடும் இதெ கட்டமைப்பை ஏற்கின்றன. ஒரு நேர்மின் அயனிக்கு ஒன்றுக்கு மேற்பட்ட எதிர்மின் அயனிகளைப் பெற்றிருக்கும் சேர்மங்களின் கட்டமைப்பு குளோரைடுகளின் கட்டமைப்பிலிருந்து விலகுகின்றன. புளோரைடின் பிரதான கனிமமான புளோரைட்டின் கட்டமைப்பில் இவ்விலகல் விவரிக்கப்படுகிறது. இங்கு Ca2+ நேர்மின் அயனி எட்டு F− மையங்களால் சூழப்பட்டுள்ளது. CaCl2,வில் ஒவ்வொரு Ca2+ அயனியும் ஆறு Cl− மையங்களால் சூழப்பட்டுள்ளது.