ホウ素
ホウ素(ホウそ、硼素、英: boron、羅: borium)は、原子番号5の元素である。元素記号はB。原子量は 10.81。
| |||||||||||||||||||
| 外見 | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
黒色の固体 | |||||||||||||||||||
| 一般特性 | |||||||||||||||||||
| 名称, 記号, 番号 | ホウ素, B, 5 | ||||||||||||||||||
| 分類 | 半金属 | ||||||||||||||||||
| 族, 周期, ブロック | 13, 2, p | ||||||||||||||||||
| 原子量 | 10.811(7) | ||||||||||||||||||
| 電子配置 | [He] 2s2 2p1 | ||||||||||||||||||
| 電子殻 | 2, 3(画像) | ||||||||||||||||||
| 物理特性 | |||||||||||||||||||
| 色 | 黒色 | ||||||||||||||||||
| 相 | 固体 | ||||||||||||||||||
| 密度(室温付近) | 2.08 g/cm3 | ||||||||||||||||||
| 融点 | (β菱面体晶)2453 K, 2180 °C, 3956 °F | ||||||||||||||||||
| 沸点 | (β菱面体晶)3923 K, 3650 °C, 6602 °F | ||||||||||||||||||
| 融解熱 | 50.2 kJ/mol | ||||||||||||||||||
| 蒸発熱 | 480 kJ/mol | ||||||||||||||||||
| 熱容量 | (25 °C) 11.087 J/(mol·K) | ||||||||||||||||||
| 蒸気圧 | |||||||||||||||||||
| |||||||||||||||||||
| 原子特性 | |||||||||||||||||||
| 酸化数 | 4[1], 3, 2, 1 (酸性酸化物) | ||||||||||||||||||
| 電気陰性度 | 2.04(ポーリングの値) | ||||||||||||||||||
| イオン化エネルギー | 第1: 800.6 kJ/mol | ||||||||||||||||||
| 第2: 2427.1 kJ/mol | |||||||||||||||||||
| 第3: 3659.7 kJ/mol | |||||||||||||||||||
| 原子半径 | 90 pm | ||||||||||||||||||
| 共有結合半径 | 84±3 pm | ||||||||||||||||||
| ファンデルワールス半径 | 192 pm | ||||||||||||||||||
| その他 | |||||||||||||||||||
| 結晶構造 | 六方晶系 | ||||||||||||||||||
| 磁性 | 反磁性 | ||||||||||||||||||
| 電気抵抗率 | (20 °C) ~106Ω⋅m | ||||||||||||||||||
| 熱伝導率 | (300 K) 27.4 W/(m⋅K) | ||||||||||||||||||
| 熱膨張率 | (25 °C) (βボロン)5-7 μm/(m⋅K) | ||||||||||||||||||
| 音の伝わる速さ (微細ロッド) | (r.t.) 16200 m/s | ||||||||||||||||||
| モース硬度 | 9.3 | ||||||||||||||||||
| CAS登録番号 | 7440-42-8 | ||||||||||||||||||
| 主な同位体 | |||||||||||||||||||
| 詳細はホウ素の同位体を参照 | |||||||||||||||||||
| |||||||||||||||||||
名称
元素名はアラビア語で「ホウ砂」を意味する「Buraq(ブラーク)」に由来する。ホウ素 (Boron) の名称は、ホウ砂を意味する[2]アラビア語の بورق (buraq) もしくはペルシャ語の بوره (burah) に起源があるとされる[3]。中国語では10世紀の「日華本草」にペルシャ語の音写としてホウ砂のことを「蓬砂」とした記述がみられ、14世紀には日本に伝来して「硼砂」と記されている[4]。
概要
単体は高融点かつ高沸点な硬くて脆い固体であり、金属元素と非金属元素の中間の性質を示す半金属である。1808年にゲイ=リュサックとルイ・テナールの2人の共同作業およびハンフリー・デービーによってそれぞれ個別に単体の分離が行われた。
ホウ素は同じ第13族元素であるアルミニウムなどよりも第14族元素である炭素やケイ素に類似した性質を示す。結晶性ホウ素は化学的に不活性であり耐酸性が高く、フッ化水素酸にも侵されない。ホウ素の化合物は通常+3価の酸化数を取り、ルイス酸としての性質をもつハロゲン化物や、ホウ酸塩鉱物中で見られるホウ酸塩、三中心二電子結合と呼ばれる特殊な結合様式を取るボランなどがある。ホウ素には13の既知の同位体があり、天然に存在するホウ素は80.1 %の11Bと19.9 %の10Bからなっている。
ホウ素は地殻中の存在率が比較的低い元素であるが、鉱床を形成するため容易に採掘可能であることから人類による利用の歴史は長く、古くから釉薬として使われていた。現代ではガラス向けの用途に使われることが多く、2011年のホウ酸塩消費量のおよそ60 %がガラス用として消費されている。その他、半導体のドーパントや超硬度材料、音響材料、殺虫剤などに利用される。
植物にとってホウ素は細胞壁を維持するために必要な必須元素であり、ホウ素の欠乏によって成長障害が引き起こされる。動物にとっても必須元素であると考えられているが、その生物学的な役割はよく知られていない。ヒトや動物に対しては食塩と同程度に無毒な物質であるが、植物では高濃度のホウ素を含む土壌で葉の壊死などの障害が発生し、昆虫に対しては強い毒性を示す。
歴史

ホウ素化合物の存在は数千年前にはすでに知られており、西チベットの砂漠から産出したホウ砂はサンスクリット語でチンカルと呼ばれていた。西暦300年ごろの中国ではすでに釉薬としてホウ砂が利用されており、8世紀のペルシアの錬金術師であるジャービル・ブン・ハイヤーンはホウ砂について言及していたとされている。13世紀には、マルコ・ポーロによってホウ砂釉薬を用いた陶磁器がイタリアへと持ち帰られた。1600年ごろにはアグリコラによって冶金学における融剤としての用途が記されている。現代においてホウ素の最大の用途ともなっているガラス向けの用途は、1758年に出版されたドッシーによる「技芸の侍女」において初めて言及されているが、当時はホウ砂が高価だったこともありごく一部のガラスに使われていたに過ぎない[5]。
1774年、イタリアのトスカーナ州州都フィレンツェ近郊のラルデレロで産出する地熱蒸気にホウ酸が含まれていることが分かり、ホウ酸工場が設立されて重要なホウ素資源として利用されたが、19世紀にはアメリカ大陸で大規模なホウ酸塩鉱物の鉱床が発見されたためその地位はアメリカに取って代わられた。ホウ素の生産が終了したあと、ラルデレロでは高温の地熱蒸気を利用した地熱発電が行われている[4][6]。ホウ素を含む鉱石としては、イタリアのサッソで発見された希少鉱石のサッソライトがある。サッソライトは1827年から1872年までの間ヨーロッパにおけるホウ砂の主要な資源として利用されていたが、その後こちらもアメリカ産のものに取って代わられた[7][8]。ホウ素化合物は1800年代まではあまり利用されることがなかったが、「ホウ砂王」とも呼ばれるフランシス・マリオン・スミスのPacific Coast Borax Companyが初めてホウ素化合物の大量生産を行い安価で提供し、普及させた[9]。その後、光学ガラスの大規模生産が始まると、ホウ砂はガラス工業において大量に消費されるようになっていった[4]。
ホウ素に関する初期の研究としては、1702年に報告されたホウ砂と硫酸を反応させることによるホウ酸の合成や、1741年に報告されたホウ素が緑色の炎色反応を示すことの発見、1752年に報告されたホウ酸とナトリウムを反応させることによるホウ砂の合成などがある[4]。単体のホウ素はジョセフ・ルイ・ゲイ=リュサックとルイ・テナールの2人[10]と、ハンフリー・デービー[11]がそれぞれ同時期に個別に単離に成功したが、それまでは単一の元素とは認められていなかった。1808年にデービーは、ホウ酸溶液に電気を通して電気分解することによって、一方の電極上に茶色の沈殿が生成されると記している。デービーはそれ以降の実験において、ホウ酸を電気分解する代わりにカリウムで還元させる方法を用いた。デービーはホウ素が新しい元素であることを確かめるために十分な量のホウ素を単離し、この元素をboraciumと命名した[11]。ゲイ=リュサックとテナールは、ホウ酸を還元するために高温で鉄と反応させる方法をとった。彼らはまた、ホウ素を酸素で酸化させることによってホウ酸を合成し、ホウ酸がホウ素の酸化生成物であることを示した[10][12]。イェンス・ベルセリウスは、1824年にホウ素の元素としての性質を同定した[13]。その後、多くの化学者によって純粋なホウ素を単離しようと試みられてきたが、そのほとんどは不純物を多く含んだものであり、比較的高純度なものであってもホウ素の純度は85 %を下回っていたと考えられている。これに初めて成功したのはアメリカの化学者であるエゼキエル・ワイントローブであると考えられており、1909年に三塩化ホウ素を電弧中で水素還元させるという方法で純粋なホウ素を単離した[14][15][16][17]。
性質
物理的および化学的性質
ホウ素には複数の同素体があり、物性値は同素体によって異なる値を示すが、全体として高融点かつ高沸点な硬くて脆い固体である[18]。たとえば融点はアモルファスホウ素で2300 °C[19]、β菱面晶ホウ素で2180 °C[20]であり、沸点はβ菱面晶ホウ素で3650 °Cである[20]。アモルファスホウ素は2550 °Cで昇華する[19]。β菱面晶ホウ素のモース硬度は9.3[21]。比重はα菱面晶ホウ素が2.46、β菱面晶ホウ素が2.35である[19]。

単体のホウ素は金属元素と非金属元素の中間の性質を示す半金属元素であり、安定した共有結合を形成するという点では、同じ第13族元素であるアルミニウムやガリウムなどの金属元素よりもむしろ炭素やケイ素と類似した性質を示す[22]。これはホウ素の第一イオン化エネルギーが8.296 eVと非常に高いためイオン化しにくく、2s22p1の最外殻電子がsp2混成軌道を形成する方がエネルギー的に有利であることに起因する[23]。単体ホウ素におけるホウ素同士の結合もまた共有結合性が強いため、自由電子として導電性に寄与できる電子が少なく、導電性を示すものの導電性は低いという半金属に特有な性質が現れる原因となる[24]。また、このような電気的特性を有するため単体ホウ素は半導体としての性質を示す[25]。
結晶性ホウ素は化学的に不活性であり、フッ化水素酸や塩酸による煮沸に対しても耐性を示す。微細粉末は熱濃過酸化水素や熱濃硝酸、熱硫酸もしくは熱クロム酸混液に対して徐々に侵される[15]。ホウ素の酸化率は結晶化度、粒径、純度および温度に依存する。ホウ素は室温では空気と反応しないが、高温では燃焼して酸化ホウ素を形成する[26]。
ホウ素はハロゲン化によって三ハロゲン化物を形成する。
三塩化ホウ素は通常、酸化ホウ素から合成される[26]。
化合物
ホウ素の化合物は通常+3価の形式酸化数を取る。これらには酸化物、硫化物、窒化物およびハロゲン化物が含まれる[26]。
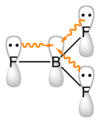
三ハロゲン化物は平面三角形構造を取る。それらの化合物はホウ素上に6つの電子しか持たないためオクテット則を満たしておらず、ルイス酸として働き、ルイス塩基のような電子対供与体と即座に反応する。たとえば三フッ化ホウ素 (BF3) はフッ化物イオン (F−) と反応してテトラフルオロホウ酸塩アニオン (BF4−) を与える。三フッ化ホウ素は石油化学産業において触媒として利用される。三ハロゲン化ホウ素は水と反応してホウ酸を形成する[26][27]。

ホウ素は地球上の自然中においてはさまざまな種類の+3価の酸化物として見られ、しばしばほかの元素と結合している。100種類以上のホウ酸塩鉱物でホウ素は+3価のホウ素を含んでいる。これらのホウ酸塩鉱物はいくつかの点でケイ酸塩鉱物と類似しているが、SiO4の四面体構造が構造の基本単位となっているケイ酸塩とは異なり、ホウ酸塩はBO4の四面体構造だけでなく、BO3の平面三角形構造の基本単位も多く見られる[28]。典型的な例としては、一般的なホウ酸塩鉱物の一つであるホウ砂における四ホウ酸アニオンがある(左図)。四ホウ酸アニオン中のホウ素は平面三角形構造と四面体構造の2種類の構造をとっており、四面体構造を取っているホウ素は負の電荷を有している。この負の電荷は、たとえばホウ砂におけるナトリウム(Na+)のような金属陽イオンとの間で釣り合っている[26]。
ボラン
ボランはホウ素と水素の化合物であり、BxHyの組成式で表される。ボランの構造にはB-H-Bのような水素による橋架け構造が含まれており、通常の化学結合における原子価の考え方ではその結合が説明できず、三中心二電子結合のような特殊な結合様式をとっている[29][30]。ボランの構造は正二十面体構造のホウ素クラスターを基本単位として考えることができ、ホウ素数の少ないボランも正二十面体構造からいくつかのホウ素原子が脱落した構造としてとらえることができる[31]。ボランのいくつかは異性体が存在し、たとえばジヒドロデカボラン (B10H16) はホウ素が5原子集まったクラスター2つからなっており、2つのクラスターの結合の方法によって3つの構造異性体が存在する[32]。
最も単純なボランはBH3であるが単離することはできず、ジボラン (B2H6) がその他のボランおよびボラン誘導体を合成する際の前駆体として利用される[31][33]。ホウ素数の少ないボランは空気との反応性が高く自然発火するが、ホウ素数6のヘキサボラン以上では空気中で安定に存在する[34]。ボランのうち重要なものにはペンタボランB5H9およびデカボランB10H14があり、それらはジボランB2H6の熱分解によって生成される[29]。多数のボランアニオンが知られており、テトラヒドロホウ酸イオン (BH4−) およびその誘導体([BH3CN]−など)は金属塩して還元などの用途に広く利用されている[35]。また、ホウ素数の多い多面体型ボランアニオンとしては[B12H12]2−などがあり、反応性などについて広く研究されている[36]。
ボランの誘導体としては、ボラン中のBH−と等電子的なCH基が置換したカルバボランがあり、ボランとアセチレンの反応によって合成される[37]。ほかに硫黄、リン、砒素なども、ホウ素と置換してカルバボランに類似したヘテロボラン誘導体を形成する[38]。カルバボランは強塩基と反応してカルバボランアニオンとなり[39]、たとえばB9C2H112−はシクロペンタジエニルアニオンに類似しており遷移金属との間でフェロセン様の錯体を形成する[40]。また、ハロゲンやアミン、アルキル基などはボランの水素を置換してボラン誘導体を形成する[41]。
窒化ホウ素
窒化ホウ素はさまざまな構造をとり、それらはダイヤモンドやカーボンナノチューブを含む炭素の同素体に似た構造をとる。ダイヤモンド様の構造をした窒化ホウ素は立方晶窒化ホウ素と呼ばれ、ホウ素原子はダイヤモンドの四面体構造における炭素原子の位置に存在しているが、4つのB-N結合のうちの1つは配位結合と見ることができる。すなわち、三フッ化ホウ素の場合と同様に、3つの窒素原子とホウ素原子が結合することで3つのB-N結合と1つの空軌道が形成され、窒素の2つの電子がルイス塩基としてホウ素上の空軌道へ供与されることで、4つ目のB-N結合が形成されることとなる。立方晶窒化ホウ素はダイヤモンドに匹敵する硬さを有しているため研磨剤に用いられる。黒鉛様の六方晶窒化ホウ素 (h-BN) は、正の電荷を持つホウ素と負の電荷を持つ窒素が交互に配列した平面構造が層状に積み重なった構造をとる。そのため、六方晶窒化ホウ素とグラファイトはともに層間の滑りによる潤滑性を示すという類似した性質もあるものの、非常に異なった性質も示す。たとえば、黒鉛は優れた熱伝導性および電気伝導性を示すが[42]、h-BNは平面方向の熱伝導性および電気伝導性が比較的乏しい[43][44]。
金属ホウ化物
ホウ素は非常に多くの元素との間でホウ化物を形成するが、特に金属元素との間で形成されるホウ化物は金属的な性質を示すことが多いことから、ホウ素自身は非金属元素であるものの、しばしばホウ素合金として扱われる[45]。金属ホウ化物は一般的に高硬度、高融点、低反応性といった性質を示す[46]。金属ホウ化物の多くはホウ素と金属元素をともに溶融もしくは焼結させることによって合成することが可能であり、ホウ化鉄やホウ化クロムなどの工業的製造法としては高純度なものは得られにくいものの、大量生産が可能なテルミット反応などの直接還元法が利用されている[47]。金属ホウ化物は、ホウ素原子と金属原子との間に化学量論的な関係が見られないことが多い。これは、金属原子が形成する立体構造の空隙に遊離したホウ素原子が取り込まれた構造をとるものや、逆にホウ素が形成する立体構造の空隙に遊離した金属原子が取り込まれた構造をとるものが多く存在するためである[48]。金属ホウ化物として重要なものにホウ化鉄(フェロボロン)があり、Fe2BやFeB、Fe2B5などが知られている[49]。ホウ化鉄は製鉄の原料として焼入れや溶接に関する性能向上に利用される[50]。ホウ素はこのような二元化合物のみならず、複数の金属元素との間に多元化合物を形成することも知られている[51]。代表的なものに、非常に強力な磁力を有するネオジム磁石として利用されるネオジム-鉄-ホウ素の三元化合物であるNd2Fe14Bがある[52]。
有機ホウ素化合物
数千種類に及ぶ有機ホウ素化合物の存在が知られており、代表的なものにトリエチルボランやボロン酸のようなアルキルホウ素化合物、ボラジン誘導体のような複素環式化合物などが存在する。アルキルホウ素化合物はハロゲン化ホウ素とグリニャール試薬を用いて合成され、アリールホウ素化合物も同様に合成することができる。トリアルキルホウ素を含むアルキルボランは、ヒドロホウ素化反応によってボランから合成される[53]。トリエチルボランなどのトリアルキルホウ素化合物は、空気中で酸素と反応して自然発火する自然発火性物質であるが、一方でトリフェニルボランのようなトリアリールホウ素化合物は空気中で燃焼しない[54]。ハロゲン化ホウ素は4倍モル当量のアルキル化剤もしくはアリール化剤と反応させると、トリアルキルもしくはトリアリールホウ素からさらに反応が進行して、テトラアルキルもしくはテトラアリールホウ酸イオンが生成される。このような化合物としてはテトラフェニルホウ酸ナトリウムやテトラメチルホウ酸リチウムなどがあり、テトラフェニルホウ酸ナトリウムはカリウムやルビジウムなどの重アルカリ金属元素を分離するのに用いられる[53]。
同素体

ホウ素には7つの同素体が存在しており、それらは結晶およびアモルファスの構造をとる。よく知られているものにα-菱面体、β-菱面体、β-正方晶があり、特殊な条件下ではα-正方晶やγ-斜方晶のような形もとる。アモルファスの同素体には、微細な粉末状のものとガラス状のものの2つが知られている[55][56]。標準状態において最も安定なものはβ-菱面体晶であり、ほかの同素体は全て準安定状態である[46]。少なくとも14以上の同素体が報告されているが、前述の7つ以外の同素体は弱い論拠に基づいたものであったり実験的に立証できなかったりするため、それらは単一の同素体ではなく複数の同素体の混合物や不純物によって安定化した構造であると考えられている[57][56][58][59]。
| 層 | α | β | γ | β |
|---|---|---|---|---|
| 結晶形 | 菱面体晶 | 菱面体晶 | 斜方晶 | 正方晶 |
| 原子数/単位格子[59] | 12 | 105‒108 | 28 | 192 |
| 密度/(g/cm3)[60][61][62][63] | 2.46 | 2.35 | 2.52 | 2.36 |
| ビッカース硬度/GPa[64][65] | 42 | 45 | 50–58 | |
| 体積弾性係数/GPa[65][66] | 224 | 185 | 227 | |
| バンドギャップ/eV[65][67] | 2 | 1.6 | 2.1 | ~2.6[68] |
同位体
天然に存在するホウ素は2種類の安定同位体からなっており、11Bが80.1%、10Bが19.9%を占める。天然存在比11B/10Bの値と実測の11B/10Bの値の差として定義される質量差δ11Bは自然水域において−16‰〜+59‰の広い範囲で変動する。ホウ素には13種の既知の同位体があり、半減期の最も短い7Bは、陽子放出およびアルファ崩壊によって3.5×10−22 sの半減期で崩壊する。ホウ素の同位体分離は、B(OH)3および[B(OH)4]−の交換反応によって制御される。ホウ素の同位体はまた、熱水系や熱水変質岩において水層から鉱石結晶が析出する際にも分離される。たとえば熱水変質岩の粘土上では10B(OH)−
4イオンが析出することで海水から優先して除去され、その結果として大洋性地殻や大陸性地殻と比較して海水中の11B(OH)3濃度が大規模に高められている可能性がある。このような同位体比の違いは同位体特性としての働きをするかもしれない[69]。エキゾチック原子核である17Bは中性子ハローを示す(すなわち液滴模型から予測されるよりも大きな原子半径を示す)[70]。
10Bは良質な熱中性子捕獲材である。10Bの天然存在比はおよそ20%ほどでしかないため、原子力産業においては天然ホウ素を濃縮して純粋な10Bとして利用しており、ほぼ純粋な11Bが利用価値の低い副生物として生じる。
分析
定性分析

ホウ素を含む試料を炎で熱すると緑色の炎色が観測されるため、ホウ素の定性分析には炎色反応が利用される。この反応においては、銅やバリウムなども類似した緑色の炎色を示して妨害となるため、炭酸ナトリウムで妨害元素を分離するなどの前処理が必要となる。また、フッ化ホウ素の200 °Cにおける炎色は鋭敏であるため、試料にフッ化カルシウムと硫酸を加えて試料中のホウ素をフッ化ホウ素とすることで微量の試料でも定性することが可能となり、およそ10 μg程度の検出限界が得られている。ほかの定性方法としては、1,2,5,8-テトラヒドロキシアントラキノン(キナザリン)とホウ素との反応によって生じる青色の発色が利用される[71]。
定量分析
ホウ素の定量分析には、マンニトール法やクルクミン法、アゾメチンH法、メチレンブルー吸光光度法、誘導結合プラズマ発光分析法 (ICP-AES) および質量分析法 (ICP-MS) などが主に用いられており[72][73]、日本工業規格においてはホウ酸などの試薬の純度分析にはマンニトール法が、工場排水の試験方法などには吸光光度法やICP法が公定法として規定されている[74]。吸光光度法では反応時間や妨害成分の問題が、ICP法では高価な装置が必要になるなどの問題があるため、高価な装置を必要とせず迅速に測定が可能な方法として電気化学的な定量分析法の開発も行われている[75]。
マンニトール法は、ホウ酸とD-(-)-マンニトールとの反応によって定量的に発生する水素イオンの量を、水酸化ナトリウム溶液などのアルカリ溶液を用いて中和滴定を行うことによって定量する分析法である[76]。ホウ素含有量の高い試料に適しており、ホウ酸や四ホウ酸ナトリウムなどの純度を分析するのに用いられる。マンニトール法は鉄やリンなどの共存元素による妨害を受けやすく、また中和滴定であるため酸やアルカリが存在している場合は先に一度中和しておく必要があるため、複雑な前処理が必要となることもある[72]。たとえば鉄鋼中のホウ素の分析にマンニトール法を用いる場合では、まず試料を酸溶解させたあとにメタノールと反応させ、ホウ酸メチルとして蒸留を行ってほかの成分からホウ素を分離し、得られた留出液を蒸発乾固させて生じる残留物を硫酸で溶解させ、硫酸酸性となっている試料溶液のpHを水酸化ナトリウムで中和してpH調整するという前処理が行われる[76]。
クルクミン法、アゾメチンH法、メチレンブルー吸光光度法はいずれも、ホウ素が発色試薬と錯体を形成することによって生じる発色の度合いを吸光度として吸光光度計を用いて測定し、ホウ素濃度が既知の溶液を発色させた場合の吸光度と比較することでホウ素濃度を定量する分析法である[77][72]。クルクミン法はクルクミンがホウ素と反応して形成されるロソシアニンの赤色の発色を利用した分析法であり、分析感度は高いもののフッ素など妨害となる元素が多い[72][78]。アゾメチンH法はアゾメチンHとホウ素の錯形成反応を利用した分析法であり、クルクミン法と比べて分析感度は低いものの妨害となる元素が少なく、妨害となる元素もEDTAによりマスキングすることができる[79][72]。メチレンブルー吸光光度法は、フッ化水素酸の存在下でホウ素とメチレンブルーが反応して形成されるメチレンブルー-テトラフルオロホウ酸錯体を溶媒抽出によって分離して吸光度を測定する分析法であり、クロム酸イオンなどが妨害要因となる[75][80]。
ICP-AES法は低濃度の試料においても高感度かつ簡便にホウ素濃度の定量分析を行うことができるが、装置価格は非常に高価である[75]。通常は182.64 nmもしくは249.77 nmの発光波長が利用されるが、後者では高感度であるものの鉄の妨害を受け、前者は鉄の妨害を受けないものの低感度である。また、試料の分解中にホウ素が揮発することもあり誤差要因となる[81]。
また、ホウ素中におよそ20 %ほど含まれている10Bの熱中性子吸収能が非常に大きいことを利用して、熱中性子線を試料に照射して熱中性子線密度の変化を測定することでもホウ素の定量分析が可能である。非破壊かつ迅速に連続分析を行うことができるため、排水中のホウ素濃度のモニタリングなどに応用されている[82][83]。
構造解析
11Bは3/2の核スピンを持つため、核磁気共鳴分光法によって構造解析を行うことができる。11Bは天然存在比がおよそ80 %と高いため、S/N比の大きな高感度な測定結果が得られるが、スピン数が1より大きな四極子核であるため幅広かつ複雑なスペクトルとなり分解能は低い[84]。また、10Bは熱中性子吸収能が高いため通常はホウ素の中性子回折は行えないが、同位体分離によって11Bのみからなる分析試料を作成することで中性子回折による構造解析を行うこともできる[85]。ホウ素化合物の分子構造解析には赤外分光法やラマン分光法が利用される[86]。例えば赤外分光法では、B-H結合は2500 cm−1に、B-N結合は1400 cm−1にそれぞれ吸収が現れる[87]。
分布

ホウ素は原子番号の小さな元素であるにもかかわらず、宇宙においては存在度が著しく低い元素であり、その存在度は1982年のAndersおよびEbiharaらの報告でケイ素原子1×106個に対して21個と見積もられている(ヘリウムで2.8×109、鉄で9.0×105)[88]。宇宙におけるホウ素の存在度が著しく低いのは、ビッグバン原子核合成や恒星内元素合成ではリチウム原子がヘリウム原子と核融合してホウ素原子を形成するよりも早く、リチウム原子が水素原子により核分裂してヘリウム原子に分解してしまい、ホウ素原子がほとんど合成されないことに起因する。自然に存在するホウ素の同位体比から、太陽系に存在しているホウ素は宇宙線による核破砕および超新星爆発時に起こるニュートリノ反応の2つの核合成経路によって生成したものと考えられている[89]。
ホウ素の地殻中の存在率もまた比較的低く、その存在率は酸化ホウ素としておよそ0.001 %である(地殻中の元素の存在度も参照)。しかしながら、その存在率の低さに反してホウ素はホウ酸塩の形で鉱床を形成して局所的に濃縮されるため容易に採掘可能であることから、古くから人類に利用されてきた[90]。このようなホウ素の濃縮は、マグマの冷却による火成岩の形成過程や、マグマから揮発放散したホウ素の堆積などによって引き起こされる。そのため、火山におけるマグマの噴出孔近辺や火山性の温泉、湖沼などにおいても、しばしばホウ素の濃縮が見られる[91]。また、岩石の風化作用によって乾燥地帯にも濃縮される[92]。ホウ素は地球上において単体の形では存在しておらず、常に酸素と結合してホウ砂やホウ酸、ホウ酸塩、コールマン石、ケルナイト、ウレキサイトなどの形で存在している。このようなホウ素を主成分として含む鉱物は100種類以上存在している。また、ホウ素はそのイオン半径からケイ素やアルミニウム、ベリリウム、リンなどに置換されやすく、数多くの鉱物中に微量元素としても存在している[93]。海水中のホウ素濃度はおよそ4–5 mg/Lであり、場所や深度による差異は比較的小さい[94]。
アメリカ地質調査所が2015年に発表したMineral Commodity Summariesでは、技術的・経済的に採掘可能なホウ素鉱石の可採埋蔵量は全世界でおよそ2億1000万トンと見られている[95]。ホウ素は火山活動や乾燥気候に起因して濃縮されるため、ホウ素の鉱床はアルプス・ヒマラヤ造山帯やアンデス山脈などの火山帯や乾燥地帯などに偏在しているが、経済的に利用可能な鉱床は限られている[95][92]。世界最大のホウ酸塩鉱床はエスキシェヒル、キュタヒヤ、バルケスィルを含むトルコの中-西部に存在しており[96][97][98]、トルコは6000万トンのホウ素鉱石を埋蔵する世界最大のホウ素埋蔵国である[99][95]。アメリカはトルコに次ぐ4,000万トン[95]の埋蔵量を有しており[95]、カリフォルニア州のモハーヴェ砂漠には世界最大の露天掘りホウ砂鉱山が存在する[100][101]。その他のホウ素埋蔵国としては、ロシア(4000万トン)、チリ(3500万トン)、中国(3200万トン)などがある[95]。
生産
ホウ素化合物の生産はホウ酸塩が容易に入手可能なため、単体ホウ素を経由せずに生産される。
初期の単体ホウ素の合成方法は、ホウ酸をマグネシウムもしくはアルミニウムを用いて還元することによって生産されていた。しかしこの方法では純粋な単体ホウ素を得ることができず、常に金属ホウ化物が不純物として混在した。純粋な単体ホウ素は、揮発性のハロゲン化ホウ素を高温条件下で水素還元させることによって得られる。半導体産業で用いられる超高純度ホウ素は、高温条件下でのジボランの分解によって合成され、その後ゾーンメルト法やチョクラルスキー法によってさらに精製される[102]。
ホウ素の同位体である10Bは高い中性子吸収能を有するが、天然ホウ素中の同位体存在率はおよそ20 %でしかないため、同位体を分離して10Bを濃縮する必要がある。その方法としては、蒸留法や化学的交換法があり、蒸留法では低沸点のホウ素化合物であるハロゲン化ホウ素を用いた低温蒸留が、化学的交換法では有機ホウフッ化化合物を用いた気液交換反応が利用される[103]。また、蒸留法と化学的交換法を組み合わせた化学交換蒸留法という方法も開発されており[85]、現代の濃縮ホウ素の生産のほとんどは化学交換蒸留法によって行われている[104]。
市場動向
2014年の世界のホウ素の生産量は鉱石ベースで372万トンであり、そのうち177万トンはトルコで生産された[95]。B2O3換算での世界のホウ酸塩の生産能力は2008年には年間200万トン以下であったが、2012年はおよそ年間220万トンまで増加している[99]。アメリカ地質調査所が2015年に発表したMineral Commodity Summariesでは、ホウ酸塩の世界需要はアジアや南米での需要の伸びに牽引されて継続的に増加すると予測されている。また、ヨーロッパなどでは地球温暖化対策として建築物のエネルギー収支を改善するために建築基準がより厳しく改正されたため、断熱ガラス用途のホウ素の需要が伸びるとも予想されており、それらに伴って世界的なホウ酸塩の生産量は増加すると見られている[95]。
世界で産業利用されているおもなホウ素鉱石はコールマン石、ウレキサイト、ホウ砂、ケルナイトの4つであり、この4種類の鉱石でホウ素生産の90 %が賄われている。これらの鉱石は主にナトリウム含有量の差によって使い分けられており、たとえばウレキサイトはホウ酸の、ホウ砂は四ホウ酸ナトリウムの原料として利用されている[95]。ホウ素の主要な用途の一つであるガラス向けにはナトリウム含有量が低いことが求められるため、主要な4鉱石の中で唯一ナトリウム塩でなくカルシウム塩 (CaB6O11) を主成分としているコールマン石が有用な原料として利用されている。しかしながらコールマン石には不純物として多くのヒ素も含有されているため、近年の環境規制の強化に伴ってその処理が問題となっている。たとえば、アメリカのニューメキシコ州マグダレナ近郊では高品質のコールマン石が産出されるが、ヒ素含有量の多さのため鉱山建設が幾度も延期されている。このようなヒ素処理の問題は、ホウ素生産量の伸びを制限する要因にもなっている[99]。
ホウ素の主要な生産者は、アメリカの「リオ・ティント」グループとトルコの国営企業である「Eti Mine Works」の2社である。リオ・ティントはカリフォルニアにある露天掘りの鉱山からホウ砂およびケルナイトを生産しており、2012年にはこの鉱山のみで世界のホウ素生産量の25 %を賄っている。Etiはトルコ全域におけるホウ素鉱石の採掘権を有しており、2012年の世界のホウ素生産量の50 %弱を賄っている[99]。中国には3,200万トンのホウ素鉱石が埋蔵されていると見積もられているが[95]、アメリカやトルコで産出するホウ素鉱石がおよそ25–30 %のB2O3を含むのに対して、中国産のものではおよそ8.4 %とB2O3含有量が少なく低品位である[105]。そのため、高品質なホウ酸塩の急速な需要増を補うために、中国の四ホウ酸ナトリウムの輸入量は2000年から2005年までに100倍も増加し、同期間中のホウ酸の輸入量も年に28 %ずつ増加した[106][107]。アメリカ地質調査所のMineral Commodity Summaries (2015) においても、中国の輸入量は2015年以降も増加していくと予測されている[95]。
用途
ホウ素が単体で使用されることは少ないが、化合物や合金の形でさまざまに利用されている[108]。
身近な用途で使用される場合は、ホウ砂やホウ酸の状態であることが多い。ホウ砂はガラスの原料や防腐剤、金属の還元剤、溶接溶剤や研磨剤、火の抑制剤などに使われ、教育の現場では、ホウ砂と洗濯糊などを用いてスライムを作成する子ども向けの科学実験工作がしばしば行われる[109]。ホウ酸塩や過ホウ酸塩は目の洗浄剤[110]、うがい薬や鼻スプレーなど口腔衛生のための医薬品[111]、ホウ酸団子としてゴキブリ駆除[112]などに使われる。
ガラスおよびセラミックス

ガラスはホウ素の主要な用途の一つであり、2011年におけるホウ酸塩消費量のおよそ60 %がガラス繊維を含むガラス用途であった。ホウケイ酸ガラスは一般的に5–30 %の酸化ホウ素を含んでおり、熱膨張率が低いため熱衝撃に対する耐性が高い。また、ホウ素をガラスに添加することで溶融状態におけるガラスの流動性が向上するため、ガラスを成型する際の生産性が向上する[113]。ホウケイ酸ガラスの主要な商標としてデュランおよびパイレックスがあり、熱衝撃に対する抵抗性を利用して主に実験用のガラス器具や、一般用の調理器具、耐熱皿などに用いられる[114]。
ホウ素繊維(ガラス長繊維)は軽量かつ高強度であるため、繊維強化プラスチックのような複合材料の強化材として利用される。主に航空宇宙分野における構造体に用いられ、一般消費者向けとしてはゴルフクラブや釣り竿のような一部のスポーツ用品にも使われている[115][116]。また絶縁材や耐火材としても用いられており、ガラス繊維用途のホウ素の消費量は全体のおよそ45 %に及ぶ[113]。このようなホウ素繊維は、化学気相蒸着法によってタングステン繊維の上にホウ素を堆積させることによって製造される[117][118]。
ホウ素繊維(ガラス短繊維)はグラスウールとして冷蔵庫や建材などにおいて断熱材として用いられる[50]。ガラス短繊維はレーザーアシストCVD法によって製造され、収束したレーザービームの並進によってサブミリメートルサイズの螺旋状のホウ素結晶のような複雑な構造さえも作り出すことができる。そのような構造は弾性係数450 MPa、剪断ひずみ3.7 %、破断応力17 GPaといった良好な機械的性質を示し、セラミックスもしくはMEMSの強化に用いることができる[119]。
音響機器
密度が小さく、ヤング率が大きく、音の伝わる速さが16200 m/sとアルミニウムの約2.6倍以上であることから、音響材料としてはベリリウム以上に理想的な素材として知られている[120]が、高融点かつ展延性が非常に低いため技術的に加工が難しい素材であり、実用化されたのは1980年以降である[121]。
- レコード針のカンチレバーにおいては品川無線[122]やオーディオテクニカ[123]、デノン[124]などより商品化されている。
- ダイヤトーンでは炭化ホウ素 (B4C) をスピーカーの高・中音域ユニットの振動板に用いている[125]。
- デノンはボロン長繊維を使用したボロンファイバー振動板を低域ユニットに使用していた。高域ユニットの振動板としても、αボロン化合物が使用されたが、チタンやジュラルミンベースに溶射する形を取っていた[126]。
半導体
ホウ素はケイ素、ゲルマニウム、炭化ケイ素などの半導体のドーパントとして用いられる。ホウ素は3つの価電子を有しているため、4つの価電子を有するケイ素のようなホスト原子中で電荷を運ぶ正孔として機能してP型半導体が形成される。古典的なホウ素のドープ方法としては、高温での原子拡散が利用されていた。このプロセスではホウ素源として固体の酸化ホウ素や液体の三臭化ホウ素、気体の三フッ化ホウ素やジボランなどを利用することができる。しかしながら1970年代以降、大部分はホウ素源として三フッ化ホウ素を利用するイオン注入法に取って代わられた[127]。三塩化ホウ素ガスもまた半導体産業において重要な化合物であるが、それはドープでなく金属および金属酸化物のプラズマエッチングのために用いられる[128]。トリエチルボランはホウ素源として化学気相成長の反応器に注入され、ホウ素を含有した硬質炭素膜やダイヤモンド膜(ダイヤモンドライクカーボン)、窒化ケイ素-窒化ホウ素膜などにおけるプラズマ堆積法に利用される[129]。
磁石
ホウ素は最も強い永久磁石の一つであるネオジム磁石 (Nd2Fe14B) を構成する元素の一つであり、ネオジム磁石中のホウ素の含有量は1 %ほどである。ネオジム磁石はさまざまな電子機器や電子デバイス、核磁気共鳴画像法 (MRI) のような医用画像処理システム、比較的小型な電動機およびアクチュエータに用いられている。たとえば、ハードディスクドライブやCDプレーヤー、DVDプレーヤーなどにおいては、ヘッド駆動機構を小型化するためにネオジム磁石が利用される。また、携帯電話向けにスピーカーを小型化するためにもネオジム磁石が用いられる[130][131][132]。
超硬度材料

いくつかのホウ素化合物は非常に高硬度であることで知られている。炭化ホウ素および立方晶窒化ホウ素の粉末は研磨剤として広く用いられており、また金属ホウ化物は化学蒸着もしくは物理蒸着法によって被覆材として用いられる。金属および合金にホウ素イオンを導入する方法としては、イオン注入法もしくは収束イオンビームによるイオンビーム堆積法、レーザ合金化法などが利用され、その結果として表面抵抗や微小硬さが著しく増加する。このようにホウ化物に被覆された素材はダイヤモンド被覆された素材に代わるものであり、それらホウ化物の表面はバルクのホウ化物と類似した性質を有している[133]。
炭化ホウ素
炭化ホウ素は、酸化ホウ素を炭素とともに電気炉で熱分解することによって得られるセラミックス材料である。
炭化ホウ素の構造はほぼB4Cのみであるものの、炭素量は化学量論比よりも明確に低い値を示す。これは炭化ホウ素の非常に複雑な構造に起因しており、炭化ホウ素はホウ素がB12クラスターとして存在しているB12C3の分子式で表される構造を取るものの、3つの炭素原子のうちの1つはホウ素原子に置換されやすいため、炭素原子数の少ない単位クラスターが混在した構造となる。また、正八面構造のB6クラスターも混在しており、炭素量が少なくなる要因となる。このような構造に起因して、炭化ホウ素は単位重量あたりの構造強さに優れている。そのため、炭化ホウ素は戦車などの装甲やボディアーマーのほか、多くの構造材として利用される。炭化ホウ素(特に10B)は、長寿命な放射性核種を生成することなく中性子を吸収する能力を有しているため、原子力発電所において発生する中性子線の吸収材として有用である。そのため、10B濃度を制御した炭化ホウ素が原子炉における遮蔽材や制御棒などに利用される。制御棒としての利用においてはその表面積を増やすためにしばしば粉末状で用いられ、また粉末を焼結させた円筒のペレット状でも用いられる[134][135]。
その他の超高硬度ホウ素化合物
- ヘテロダイヤモンドはBCNとも呼ばれ、ダイヤモンドの高硬度と立方晶窒化ホウ素の優れた耐熱性を併せ持つ多結晶材料である[136]。鉄と反応しやすいダイヤモンドとは異なり鉄との反応性が低いことから、研磨剤としての有用性が期待されている[137]。
- 窒化ホウ素は炭素と等電子的であり、六方晶窒化ホウ素 (h-BN) はグラファイトに類似した六角形構造を、立方晶窒化ホウ素 (c-BN) はダイヤモンドに類似した構造を取る。h-BNは高温領域で用いられる構造材や潤滑油に利用される。c-BNは優れた研磨剤として利用され、ボラゾンの商標で知られている[138]。c-BNはダイヤモンドに次ぐ硬度を有しており、化学的安定性はダイヤモンドよりも優れている[139]。
- 二ホウ化レニウム (ReB2) は大気圧下で容易に生産することが可能な超高硬度材料である[140]。ReB2の硬さはその六角形の層状構造に起因してかなりの異方性を示す。その硬さは炭化タングステンや炭化ケイ素、チタン、二ホウ化ジルコニウムなどに匹敵する。その高硬度かつ高融点な性質から、高温領域で用いる構造材などの用途が検討されている[141]。
- ホウ化アルミニウムマグネシウム-ホウ化チタン複合材料 (AlMg14-TiB2) は高硬度かつ耐摩耗性に優れた性質を有しており、高温や磨耗に晒される構造材のための被覆材もしくはバルクのままで利用される[142]。
| 素材 | ダイヤモンド | 立方晶-BC2N | 立方晶-BC5 | 立方晶-BN | B4C | ReB2 |
|---|---|---|---|---|---|---|
| ビッカース硬さ (GPa) | 115 | 76 | 71 | 62 | 38 | 22 |
| 破壊靭性(MPa m1/2) | 5.3 | 4.5 | 9.5 | 6.8 | 3.5 |
建築
ホウ素系薬品で処理をした古新聞紙が、「セルロースファイバー」という名称で断熱材として使用される。吸湿性を持つ天然繊維系断熱材として注目されている。ホウ素系薬品で処理することにより、撥水性、難燃性、駆虫作用が得られる。日本の大手ハウスメーカーで採用例は少ないが、アメリカでは家庭用断熱材の40 %前後のシェアを占める[145]。充填工法で施工されるために、専門の吹き込み用機器が必要なこと、改築の際に壁・天井に充填されたセルロースファイバーが障害になる、吹き込み後の沈み込みの可能性などの問題を指摘する声がある[146]。
原子力
ホウ素の同位体のうち10B は非常に大きな中性子吸収断面積を持つ。この特性を生かし、原子炉内において中性子の吸収のため制御棒に使用される[147]。化合物であるホウ酸は一次冷却水に溶かし込んで加圧水型原子炉の余剰反応度制御に使われる[148]。微量のホウ素添加を行った金属による放射性物質運搬容器も使用される[149]。
有機化学
ホウ素の有機化学への利用はH・C・ブラウンによって系統的に研究が行われ、ブラウンはその業績によって1979年にノーベル化学賞を授与された。ブラウンの研究した還元剤としての水素化ホウ素ナトリウムやヒドロホウ素化は、現在でも有機合成上、盛んに利用されている。ブラウンの研究室で学んだ鈴木章もまた、有機ホウ素化合物を用いた鈴木・宮浦カップリングの研究で2010年にノーベル化学賞を授与されている。この反応を利用すると多様な変換が可能になるため、有機ホウ素化合物は複雑な化合物の前駆体として利用されている[150]。
トリエチルボランは発火しやすく燃焼速度も早いため、ジェット燃料に利用される[151]。
生物
植物の必須元素の一つであり、98 %は細胞壁に存在することから、細胞壁の合成、細胞膜の完全性の維持、糖の膜輸送、核酸合成、酵素の補酵素などに関係していると予想されているが、まだ解明されてはいない[152]。植物中でホウ素輸送を行う物質は2002年(平成14年)に初めて同定された[153]。
一方、高濃度のホウ素は植物の成長を阻害する[154]ため、土壌中のホウ素含有量が高いオーストラリア南部などでは農業が困難となっている[155]。植物の遺伝子を改変することで、ホウ素耐性を持たせる研究が進められている[156]。
生物学的役割
ホウ素は主に植物の細胞壁を維持するのに必要である重要な栄養素である。土壌中におけるホウ素の欠乏は植物に対して全体的な成長障害を引き起こすが(適切な細胞壁構造の構築が行えなくなるのでホウ素が切れた場合は壊滅的な影響を及ぼす。)、逆に土壌中のホウ素分率が1×10−6を越えても葉の周辺や先端の壊死といった過剰障害を引き起こす。特にホウ素に敏感な植物では、土壌中のホウ素分率が8×10−7を越えると同様の症状が現れることがあり、土壌中のホウ素分率が1.8×10−6を越えると、ホウ素に耐性を示すような植物を含むほとんどの植物において過剰障害の兆候が現れる。ホウ素分率が2.0×10−6を越える土壌で正常に生育できる植物はほとんどなく、一部は生存できないこともある。植物組織中のホウ素分率が200×10−6を越えると過剰障害の兆候が現れる[157][158][159]。
ホウ素はおそらく全ての哺乳類にとって必須であると考えられているが、動物におけるホウ素の生物学的役割はよく知られていない。たとえば、精製してホウ素を除去した食品を与え、空気中の塵を濾過することによってホウ素欠乏症を誘発させたラットでは体毛への影響が出ることが知られており、ホウ素は超微量元素としてネズミの最適な健康状態を維持するために必要である。動物におけるホウ素の摂取は広く食糧に由来しており、その必要摂取量はラットにおける試験からの推測によって非常に少量であると考えられている[160]。
1989年以降、ホウ素が人間を含む動物にとって栄養素として生物学的な役割を持つのではないかという議論が起こった[161]。アメリカ合衆国農務省が閉経後の女性に対して1日3 mgのホウ素を投与する実験を行った結果、ホウ素の補給がカルシウムの排出を44 %抑え、エストロゲンおよびビタミンDを活性化させるという結果が示され、骨粗鬆症を抑制する可能性が示唆された。しかし、これらの影響が栄養素としての効果なのか、医薬品としての効果なのかということは判別できなかった。アメリカ合衆国国立衛生研究所は「正常なヒトの食事におけるホウ素の1日当たりの総摂取量の範囲は2.1–4.3 mgである」と述べた[162][163]。
角膜ジストロフィーの珍しい型である先天性角膜内皮ジストロフィー2型は、ホウ素の細胞内濃度を調整している輸送体をコード化するSLC4A11遺伝子における突然変異と関連している[164]。しかし、2013年のDiego G. Ogandoらの報告によれば、SLC4A11とホウ素輸送の関係は否定されており、SLC4A11はNa+-OH−(H+)およびNH4+に対する透過性を持った輸送体であるとされている[165]。
健康問題と毒性
単体ホウ素、酸化ホウ素、ホウ酸、ホウ酸塩および多くの有機ホウ素化合物は、急性毒性に限って見ると、ヒトおよび動物にとっては食塩と同程度に無毒である。動物に対する半数致死量 (LD50) は体重1 kgあたりおよそ6 gであり、LD50が体重1 kgあたり2 g以上となる物質は一般に無毒であるとされている。ヒトに対する最小致死量ははっきりとしていない。事件を除く1日4 gのホウ酸の摂取は報告されているが、それを超える量の摂取では有毒であると考えられている。50日間継続して1日0.5 g以上のホウ酸を摂取すると下痢など消化器系の不良が生じ、ほかの毒性も示唆される[166]。中性子捕捉療法のために行われるホウ酸20グラムの単回投与では、著しいほかの毒性が生じることなく使用されている。魚類は飽和ホウ酸溶液中で30分間生存することができ、ホウ酸ナトリウム溶液中ではより長く生存できる[167]。ホウ酸は、昆虫に対しては動物に対してよりも毒性が強く、通常殺虫剤として利用される[168]。
ボランのような水素化ホウ素やそれに類似したガス状の化合物は毒性を示す。ホウ素自体はほかの単体ホウ素やホウ素化合物と同様に本質的には有毒ではないが、その毒性は化学構造に起因する[7][8]。
ボランは可燃性かつ有毒であるため、取り扱いには特別な操作が必要となる。水素化ホウ素ナトリウムは強い還元性を持つ物質であるため、水や酸、酸化剤などと反応して火災や爆発を起こす危険性がある[169]。ハロゲン化ホウ素は腐食性を有する[170]。
出典
参考文献
和書
- F・A・コットン、G・ウィルキンソン『コットン ウィルキンソン 無機化学(上)』中原勝儼(原書第四版)、培風館、1987年。ISBN 4563041920。
- 斉藤一夫 著、柴田雄次、木村健二郎 監修 編『無機化学全書 X-2 ホウ素、炭素、ゲルマニウム』丸善、1965年。
- 櫻井武、鈴木晋一郎、中尾安男『ベーシック無機化学』化学同人、2003年。ISBN 4759809031。
- 村上雅人『元素を知る事典: 先端材料への入門』海鳴社、2004年。ISBN 9784875252207。
- 第16回ホウ素ホウ化物および関連物質国際会議組織委員会 編 編『ホウ素・ホウ化物および関連物質の基礎と応用』シーエムシー出版、2008年。ISBN 978-4882319559。
- 宇野良清、木村薫 「第1編 第1章 1 ホウ素固体の物理的性質」、3-28頁。
- 白井光雲 「第1編 第1章 3 高圧における固体ホウ素の性質」、34-46頁。
- 中村勝光 「第1編 第2章 5 窒化ホウ素」、123-139頁。
- 宍戸統悦、岡田繁 「第1編 第3章 1 ホウ素の製造方法」、151-156頁。
洋書
- Donohue, J. (1982). The structures of the elements. Malabar, Florida: Robert E. Krieger. ISBN 0898742307
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic chemistry (3rd ed.). Harlow: Pearson Education. ISBN 978-0-13-175553-6
- Wiberg, N. (2001). Inorganic chemistry. San Diego: Academic Press. ISBN 0-12-352651-5




