Vakcína proti covidu-19
Vakcína proti covidu‑19 je určená k boji proti viru SARS-CoV-2, způsobující nemoc covid-19.

Ještě před pandemií covidu-19 existoval zavedený soubor poznatků o struktuře a funkci koronavirů způsobujících onemocnění jako je těžký akutní respirační syndrom (SARS) a blízkovýchodní respirační syndrom (MERS). Tyto znalosti urychlily vývoj různých vakcinačních platforem na počátku roku 2020.[1] Zpočátku se vakcíny proti SARS-CoV-2 zaměřovaly na prevenci symptomatických, často závažných onemocnění.[2] Dne 10. ledna 2020 byla prostřednictvím globální vědecké iniciativy GISAID sdílena data o genetické sekvenci viru SARS-CoV-2 a 19. března oznámil světový farmaceutický průmysl významný závazek řešit covid-19.[3]
Vakcínám proti covidu-19 se obecně přisuzuje role při snižování závažnosti a úmrtnosti způsobené covidem-19.[4][5] Mnoho zemí zpočátku zavedlo plány postupné distribuce, které upřednostňovali osoby s nejvyšším rizikem komplikací, jako jsou starší lidé, a osoby s vysokým rizikem expozice a přenosu, jako jsou zdravotničtí pracovníci.[6]
Do 8. března 2023 bylo na základě oficiálních zpráv národních zdravotnických agentur po celém světě podáno 13,32 miliard dávek vakcíny proti covidu-19. K 31. lednu 2022 bylo vyrobeno 11,7 mld. dávek vakcín, z toho 5,0 mld. v Číně, 2,5 mld. v Evropské unii, 1,8 mld. v Indii, 1,1 ,mld. ve Spojených státech amerických a 430 mil. ve Švýcarsku. Mezi největší výrobce patřily Pfizer (2,6 mld. dávek), AstraZeneca (2,6 mld.), Sinovac (2,5 mld. dávek), Sinopharm (2,3 mld.) a Moderna (750 mil.).[7]
V Evropské unii, a tedy i v České republice, se k březnu 2023 očkuje vakcínami Pfizer–BioNTech, Moderna, Oxford-AstraZeneca, Janssen, Novavax[8] a Valneva.[9]
Plánování a investice
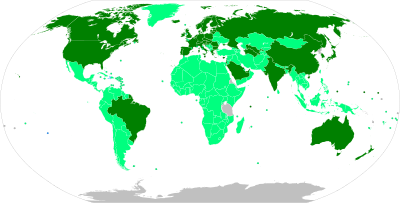
Vývoj vakcín proti covidu-19, který probíhá od počátku roku 2020, se vyznačuje zvláště v západním světě spoluprací některých firem nadnárodního farmaceutického průmyslu a rozvojem biotechnologických společností v mnoha zemích.[10] Podle Koalice pro inovace v připravenosti na epidemie (CEPI) zahrnuje geografická distribuce vývoje vakcín proti covidu-19 organizace v Severní Americe, které mají přibližně 40 % světového výzkumu vakcín na covid-19, zatímco 30 % výzkumu se děje v Asii a Austrálii, 26 % v Evropě včetně Ruska a několik procent v Jižní Americe a Africe.[10][11]
Již první fáze testování vakcín u lidí vyžadují značné kapitálové náklady farmaceutických firem, které se odhadují na 14 až 25 milionů dolarů pro typickou I. fázi klinické studie, ale možná až 70 milionů dolarů.[12][13] Pro srovnání: během epidemie eboly v západní Africe v letech 2013–2016 bylo v naléhavém vývoji 37 kandidátů na vakcíny, ale pouze jeden nakonec uspěl jako licencovaná vakcína, což znamenalo celkové náklady na potvrzení účinnosti v II. až III. fázi studií přibližně 1 miliardy dolarů.[12]
Mezinárodní organizace
Iniciativa skupiny největších ekonomik světa (G20)
Iniciativou skupiny největších ekonomik světa G20 byla dne 24. dubna 2020 vyhlášena akce nazvaná Access to COVID-19 Tools (ACT) Accelerator (Zrychlení přístupu k nástrojům proti covidu-19, ACT).[14] Výzva k této akci byla zveřejněna současně se Světovou zdravotnickou organizací (WHO).[15]
Dne 10. září 2020 uspořádaly Organizace spojených národů (OSN) a Evropská unie (EU) první zasedání rady „akcelerátoru“, které bylo přislíbeno 2,7 miliardy z 35 miliard amerických dolarů nezbytných k zajištění vývoje a výroby 2 miliard dávek vakcín proti covidu-19, 245 milionů ošetření lidí a 500 milionů testů, které iniciativa považovala za nutné k rychlému zastavení pandemie a urychlení globálního hospodářského oživení.[16] Andrew Witty a Ngozi Okonjo-Iweala ze Světové banky byli získáni pro funkce zvláštních velvyslanců WHO pro akcelerátor ACT.[17] V období vlády prezidenta Donalda Trumpa Spojené státy americké stáhly svou finanční podporu WHO a nepodporovaly tento akcelerátor.[18]
Akcelerátor je mezioborová podpůrná struktura, která má partnerům umožnit sdílení zdrojů a znalostí. Skládá se ze čtyř pilířů, z nichž každý je řízen dvěma až třemi spolupracujícími partnery:[19]
- Vakcíny (také nazývané „COVAX“)
- Diagnostika
- Terapeutika
- Spojka zdravotnických systémů
Vakcíny a COVAX
| Dárce | Příspěvek |
|---|---|
 Spojené státy americké Spojené státy americké | 2 500 |
 Německo Německo | 1 093 |
 Spojené království Spojené království | 735 |
 Evropská unie Evropská unie | 489 |
 Japonsko Japonsko | 200 |
 Kanada Kanada | 181 |
| Nadace Billa a Melindy Gatesových | 156 |
 Saúdská Arábie Saúdská Arábie | 153 |
 Norsko Norsko | 141 |
 Francie Francie | 122 |
 Itálie Itálie | 104 |
 Austrálie Austrálie | 61 |
 Španělsko Španělsko | 61 |
 Nizozemsko Nizozemsko | 37 |
 Rakousko Rakousko | 32 |
| Reed Hastings a Patty Quillinová | 30 |
 Švédsko Švédsko | 24 |
| Anonymní nadace | 22 |
 Švýcarsko Švýcarsko | 22 |
 Nový Zéland Nový Zéland | 12 |
 Kuvajt Kuvajt | 10 |
 Katar Katar | 10 |
| Shell | 10 |
 Jižní Korea Jižní Korea | 10 |
| TikTok | 10 |
 Dánsko Dánsko | 8 |
 Belgie Belgie | 5 |
 Irsko Irsko | 5 |
 Singapur Singapur | 5 |
| Wise | 5 |
 Řecko Řecko | 2 |
 Island Island | 2 |
 Kolumbie Kolumbie | 1 |
| KSRelief | 1 |
 Lucembursko Lucembursko | 1 |
| Mastercard | 1 |
 Estonsko Estonsko | 0,1 |
 Monako Monako | 0,1 |
 Bhútán Bhútán | 0,01 |
| Celkem | 8 429,21 |
Nadnárodní spolupráce, včetně Světové zdravotnické organizace (WHO), Koalice pro inovace v připravenosti na epidemie (CEPI), GAVI, Gatesovy nadace a vlád, vytvořila akcelerátor přístupu k nástrojům covid-19 (ACT), aby získala finanční podporu, zrychlený výzkum a vývoj, výrobu a globálně spravedlivý přístup k testům, léčením a licencím vakcín proti covidu-19, které jsou ve specifickém vývojovém programu nazvaném „pilíř COVAX“.[21][22] Cílem pilíře COVAX je usnadnit udělování licencí pro několik vakcín proti covidu-19, ovlivňovat spravedlivé ceny a poskytovat stejný přístup až k 2 miliardám dávek do konce roku 2021 na ochranu předních zdravotnických pracovníků a osob s vysokým rizikem infekce covidu-19, zejména v zemích s nízkými a středními příjmy.[23][24]
V průběhu roku 2020 došlo k zásadním změnám v celkovém úsilí při vývoji vakcín na covid-19. Od počátku roku rostla spolupráce nadnárodního farmaceutického průmyslu s národními vládami a rostl počet rozmanitost biotechnologických společností zaměřených na vakcínu proti covidu-19.[10] Podle CEPI zahrnuje obecná geografická distribuce vývoje vakcín organizace v Severní Americe, kde probíhá přibližně 40 % světového výzkumu vakcín, ve srovnání s 30 % v Asii a Austrálii, 26 % v Evropě a několika projekty v Jižní Americe a Africe.[10]
První zemí světa, která díky tomuto programu získala vakcíny, se stala Ghana, do které dne 24. února 2021 dorazilo 600 tisíc dávek vakcíny AZD1222 od firmy AstraZeneca a Oxfordské univerzity.[25][26]
Finanční příspěvky
V prosinci 2020 bylo pro celý akcelerátor ACT získáno 2,4 miliardy amerických dolarů, přičemž devět kandidátů na vakcíny bylo financováno z programů COVAX a CEPI – jde o největší portfolio vakcín proti covidu-19 na světě – se 189 zeměmi, které se zavázaly k plánu případného nasazení.[27][28]
Na začátku roku 2020 uskutečnila WHO televizní akci, která zvýšila přísliby ve výši 8,8 miliardy dolarů od čtyřiceti zemí na podporu rychlého vývoje vakcín.[29] V prosinci Gatesova nadace věnovala WHO dalších 250 milionů dolarů akcelerátoru ACT na „podporu dodávek nových testů, léčby a vakcín proti covidu-19, zejména v zemích s nízkými a středními příjmy“ v průběhu roku 2021, čímž se celková částka daru na potlačení covidu-19 od nadace zvýšila na 1,75 miliardy dolarů.[30][31]
Globální výzkumná spolupráce pro připravenost na infekční onemocnění (GLoPID-R) úzce spolupracuje s WHO a členskými státy na stanovení priorit pro financování konkrétního výzkumu potřebného pro vakcínu na covid-19 a koordinuje mezinárodní finanční a výzkumné organizace s cílem udržovat aktuální informace o pokrocích očkování a zamezení duplicitního financování.[32]
Koalice pro inovativní epidemickou připravenost
Koalice pro inovativní epidemickou připravenost (CEPI), nadnárodní organizace založená v roce 2017, spolupracuje s mezinárodními zdravotnickými úřady a vývojáři vakcín na vývoji vakcín pro prevenci epidemií.[24] CEPI vytvořila fond v hodnotě 2 miliard dolarů v globálním partnerství mezi veřejnými, soukromými, filantropickými a organizacemi občanské společnosti pro zrychlený výzkum a klinické testování devíti kandidátů na vakcínu proti covidu-19 s cílem v období 2020–2021 podporovat několik kandidátských vakcín vývoj k licencování.[10][27][33] Spojené království, Kanada, Belgie, Norsko, Švýcarsko, Německo a Nizozemsko již poskytly Koalici počátkem května 915 milionů dolarů.[29][34] Gatesova nadace, soukromá charitativní organizace zabývající se výzkumem a distribucí vakcín, věnovala 250 milionů dolarů na podporu Koalici pro výzkum a podporu veřejného vzdělávání u vakcíny proti covidu-19.[35][36]
V průběhu pandemie v roce 2020 financovala CEPI vývoj devíti kandidátů na vakcíny v portfoliu, které bylo záměrně rozděleno mezi různé technologie vakcín, aby se minimalizovalo obvykle vysoké riziko selhání spojené s vývojem vakcín.[27][37] V prosinci 2020 CEPI podporovala výzkumné organizace a programy vakcín Oxford–AstraZeneca, Clover Biopharmaceuticals (SCB-2019), CureVac (Zorecimeran/CVnCoV), Inovio (INO-4800), Pasteurův ústav (MV-SARS-CoV-2), Moderna, Novavax, SK bioscience (GBP 510) a Hongkongská univerzita.[27][38][39]
Vývoj
Pozadí
Před covidem-19 nikdy nebyla vakcína proti infekční nemoci vyrobena za méně než několik let a neexistovala žádná vakcína pro prevenci infekce lidského koronaviru.[40] Vakcíny však byly vyrobeny proti několika zvířecím chorobám způsobeným koronaviry, včetně viru infekční bronchitidy ptáků z roku 2003, psího koronaviru a kočičího koronaviru.[41] Předchozí projekty zaměřené na vývoj vakcín proti virům z čeledi Coronaviridae, které působí na člověka, byly zaměřeny na těžký akutní respirační syndrom (SARS)[42] a blízkovýchodní respirační syndrom (MERS). Vakcíny proti SARS a MERS[43] byly testovány na zvířatech.
Podle studií publikovaných v letech 2005 a 2006 byla identifikace a vývoj nových vakcín a léčivých přípravků k léčbě SARS v té době prioritou vlád a agentur veřejného zdraví po celém světě.[44][45][46] K roku 2020 neexistovala žádná léčba ani ochranná vakcína proti SARS, která by se prokázala jako bezpečná a účinná u lidí.[47][48]
Neexistuje ani prokázaná vakcína proti MERS.[49] Když začal převládat MERS, věřilo se, že stávající výzkum SARS může poskytnout užitečnou šablonu pro vývoj vakcín a terapeutik proti infekci MERS-CoV.[47][50] Od března 2020 byla k dispozici jedna vakcína proti MERS (založená na DNA), která dokončila I. fázi klinických studií na lidech[51] a tři další, přičemž všechny jsou vakcínami s virovými vektory: dvě s adenovirovými vektory (ChAdOx1-MERS, BVRS-GamVac) a jedna s MVA-vektorem (MVA-MERS-S).[52]
Raný vývoj

Poté, co byl koronavirus detekován v prosinci 2019,[53] byla dne 11. ledna 2020 zveřejněna genetická sekvence SARS-CoV-2 (ten, co způsobuje nemoc covid-19), což vyvolalo okamžitou mezinárodní reakci s cílem připravit se na vypuknutí a urychlit vývoj vakcíny.[11][54][55]
V únoru 2020 Světová zdravotnická organizace (WHO) uvedla, že neočekává, že vakcína proti těžkému akutnímu respiračnímu syndromu koronaviru 2 (SARS-CoV-2), viru způsobujícímu covid-19, bude k dispozici za méně než 18 měsíců.[56] Rychle rostoucí míra infekce covid-19 na celém světě na počátku roku 2020 stimulovala mezinárodní spojenectví a vládní úsilí o naléhavé organizování zdrojů na výrobu více vakcín ve zkrácených termínech,[57] přičemž čtyři kandidáti na vakcíny vstoupili v březnu do fáze testování na lidech.[11][33]
V dubnu 2020 odhadla WHO celkové náklady na vývoj sady tří nebo více vakcín s různými technologiemi a distribucí na 8 mld. amerických dolarů.[57]
Do dubna 2020 pracovalo v této virtuální zlaté horečce „téměř 80 společností a institutů v 19 zemích“.[58] Ještě v dubnu CEPI odhadovala, že až šest kandidátů na očkování proti covidu‑19 by mělo být vybráno mezinárodními koalicemi pro vývoj ve II. a III. fáze klinických studií a tři by měly být usměrněny prostřednictvím regulace a zajištění kvality případných licencí s celkovými náklady nejméně 2 mld. dolarů.[10][33][40] Další analýza odhadla, že 10 kandidátů bude potřebovat současný počáteční vývoj, než bude vybráno několik vybraných pro konečnou cestu k licencování.[40]
V červenci 2020 se britské Národní centrum kybernetické bezpečnosti, kanadský Komunikační bezpečnostní ústav a americké Agentura pro kybernetickou a infrastrukturní bezpečnost (CISA) a Národní bezpečnostní agentura (NSA) shodly, že ruští státem podporovaní hackeři se možná pokoušeli ukrást výzkumy léčby a vakcín proti covidu-19 akademickým a farmaceutickým institucím v dalších zemích; Rusko to popřelo.[59]
Stlačená časová osa
Naléhavost vytvoření vakcíny proti covidu-19 vedla ke stlačeným harmonogramům, které zkrátily standardní časovou osu vývoje vakcín, v některých případech kombinovaly kroky klinických studií během měsíců, což je proces, který obvykle trvá postupně několik let.[35] Hodnoceno je několik kroků v rámci celé vývojové cesty, včetně úrovně přijatelné toxicity vakcíny (její bezpečnosti), cílení na zranitelné populace, potřeby průlomů v účinnosti vakcíny, trvání ochrany proti očkování, speciálních systémů podávání (jako je orální nebo nosní podání, spíše než injekcí), dávkový režim, charakteristiky stability a skladování, povolení pro nouzové použití před formální licencí, optimální výroba pro rozdělení na miliardy dávek a šíření licencované vakcíny.[40][60] Časové osy pro provádění klinického výzkumu postupného procesu vyžadujícího obvykle roky jsou komprimovány do testů bezpečnosti, účinnosti a dávkování probíhajících současně po několik měsíců, což potenciálně ohrožuje zajištění bezpečnosti.[34][35] Například čínští vývojáři vakcín a čínské vládní středisko pro kontrolu a prevenci nemocí zahájily své úsilí v lednu 2020[61] a do března sledovaly řadu kandidátů v krátkých časových lhůtách s cílem předvést čínské technologické silné stránky nad Spojenými státy americkými a ujistit Číňany o kvalitě vakcín vyráběných v Číně.[35][62]
Předklinický výzkum

V dubnu 2020 vydala WHO prohlášení zastupující desítky vědců z celého světa věnujících se vakcínám a přislíbila spolupráci k urychlení vývoje vakcíny proti covidu-19.[63] Koalice WHO podporuje mezinárodní spolupráci mezi organizacemi vyvíjejícími kandidáty na vakcíny, národními regulačními a politickými agenturami, finančními přispěvateli, sdruženími veřejného zdraví a vládami pro případnou výrobu úspěšné vakcíny v množství dostatečném pro zásobení všech postižených regionů, zejména zemí s nízkými příjmy.[11]
Průmyslová analýza vývoje minulých vakcín ukazuje míru selhání 84–90 %.[11][64] Protože covid-19 je nový cílový virus s vlastnostmi, které se stále odhalují a vyžadují inovativní technologie a vývojové strategie, rizika spojená s vývojem úspěšné vakcíny ve všech krocích předklinického a klinického výzkumu jsou vysoká.[11]
Aby bylo možné posoudit potenciál účinnosti vakcín, došlo v průběhu roku 2020 k vývoji nadnárodních, do té doby nebývalých, počítačových simulací a též nových zvířecích modelů specifických pro covid-19, ale tyto metody zůstávají nevyzkoušené kvůli neznámými vlastnostem viru covid-19.[11] Z potvrzených kandidátů na aktivní vakcínu bylo asi 70 % vyvíjeno soukromými společnostmi, zbývající projekty jsou vyvíjeny akademickými, vládními koalicemi a zdravotnickými organizacemi.[10]
Většina vývojářů vakcín jsou malé firmy nebo univerzitní výzkumné týmy s malými zkušenostmi s úspěšným plánem vývoje vakcín a omezenou kapacitou platit náklady na pokročilé klinické studie a výrobu, bez partnerství s nadnárodními farmaceutickými společnostmi.[10][11]
Historicky je pravděpodobnost úspěchu kandidáta na vakcínu proti infekční chorobě, která překoná předklinické bariéry a dosáhne I. fáze klinických testů na lidech 41–57 %.[12]
Technologické platformy

Od září 2020 bylo ve výzkumu a vývoji devět různých typů vakcín proti covidu‑19.[10] Většina kandidátních vakcín v klinických studiích byla zaměřena na spike protein koronaviru a jeho varianty jako primární antigen infekce covid‑19.[10] Typy vakcín vyvíjených v roce 2020 zahrnovaly vakcíny na bázi nukleových kyselin (nukleosidem modifikovaná mRNA a DNA), nereplikující se virové vektory, peptidy, rekombinantní proteiny, živé oslabené viry a inaktivované viry.[10][11][40][65]
Mnoho typů vakcín vyvíjených proti covidu-19 nejsou jako konvenční vakcíny proti chřipce, ale používají spíše strategie „nové generace“ pro efektivnější tlumení infekce covid‑19.[10][11][65] Moderní vakcíny nových typů mohou přinést flexibilitu při přípravě antigenů a tím i zvýšit účinnost pro potlačení infekce covidem‑19 u některých citlivých podskupin populace, jako jsou zdravotničtí pracovníci, starší lidé, děti, těhotné ženy a lidé s oslabeným imunitním systémem.[10][11]
| Molekulární platforma | Celkový počet kandidátů | Počet kandidátů ve fázi testování na lidech |
|---|---|---|
| Neaktivní virus | ||
| Nereplikující se virový vektor | ||
| na bázi RNA | ||
| Proteinová podjednotka | ||
| založené na DNA | ||
| Částice podobné virům | ||
| Replikující virový vektor | ||
| Živý oslabený virus |
Typy vakcín
V klinických studiích fáze III byla pro několik vakcín prokázána účinnost až 95 % při prevenci symptomatické infekce covidem-19.[67] Národní regulační orgány alespoň jednoho státu schválily k listopadu 2021 dvacet šest vakcín pro veřejné použití. Jsou to následující vakcíny: jedna DNA vakcína (ZyCoV-D), dvě RNA vakcíny (Pfizer–BioNTech a Moderna), deset konvenčních inaktivovaných vakcín (BBIBP–CorV od čínské společnosti Sinopharm, CoronaVac od čínské společnosti Sinovac, Covaxin od indické společnosti Bharat Biotech, čínská WIBP–CorV, ruská CoviVac, kazašská QazCovid-in, čínský Covidful, íránský COVIran Barakat, čínský KCONVAC a íránský FAKHRAVAC), pět vakcín s virovým vektorem (vakcíny Sputnik V a Sputnik Lajt od ruského Gamalejova institutu, Oxford–AstraZeneca, Convidecia od čínské společnosti CanSino Biologics a Johnson & Johnson) a pět peptidových vakcín (ruská EpiVacCorona, čínská RBD-Dimer (ZF2001), kubánská Abdala, kubánská Soberana 02, tchajwanská MVC-COV1901 a australská COVAX-19 nebo americká Novavax).
Podle Světové zdravotnické organizace bylo k březnu 2022 celosvětově ve vývoji 340 vakcín, z toho v klinických studiích 122 vakcín proti covidu-19, z toho 30 v první fázi, 31 ve fázi I. až II., 16 ve II. fázi, 36 ve III. fázi a 9 ve IV fázi.[66]
V současné době probíhá výzkum a vývoj nejméně deseti různých technologických platforem s cílem vytvořit účinnou vakcínu proti covidu-19.[68][69] Většina platforem kandidátů na vakcínu v klinických studiích se zaměřuje na koronavirový spike protein (S protein) a jeho varianty jako primární antigen infekce covid‑19,[68] protože S protein spouští silné B-lymfocyty a T-lymfocyty imunitní reakce.[70][71] Pro vývoj vakcíny se však zkoumají i další proteiny koronaviru, jako je kapsida, protože také indukují silnou odpověď T-lymfocytů a jejich geny jsou konzervovanější a méně často se rekombinují (ve srovnání se spikem).[71][72][73]
Platformy vyvíjené v roce 2020 zahrnovaly technologie nukleových kyselin (nukleosidy modifikované messenger RNA a DNA), nereplikující se virové vektory, peptidy, rekombinantní bílkoviny, živé oslabené viry a inaktivované viry.[68][74][75][76]
Mnoho technologií vakcín vyvíjených proti covidu-19 nejsou jako vakcíny, které se již používají k prevenci chřipky, ale spíše využívají strategie nové generace pro přesné zacílení mechanismů infekce covid-19.[68][68][76] Několik syntetických vakcín používá mutaci 2P k uzamčení spike proteinu do jeho prefuzní konfigurace, čímž stimuluje adaptivní imunitní odpověď na virus předtím, než se připojí k lidské buňce.[77] Vyvíjené očkovací platformy mohou zlepšit flexibilitu manipulace s antigeny a účinnost pro zacílení mechanismů infekce covid-19 u citlivých podskupin populace, jako jsou zdravotničtí pracovníci, senioři, děti, těhotné ženy a lidé s oslabeným imunitním systémem.[68][75]
mRNA vakcíny
Několik vakcín proti covidu-19, včetně vakcín Pfizer–BioNTech a Moderna, bylo vyvinuto tak, aby využívaly RNA ke stimulaci imunitní reakce. Když je vakcína zavedena do lidské tkáně, obsahuje buď samoreplikující se RNA, nebo messenger RNA (mRNA), které obě způsobují, že buňky exprimují spike protein SARS-CoV-2. Tím se tělo naučí, jak identifikovat a zničit odpovídající patogen. RNA vakcíny často, ale ne vždy, používají mediátorovou RNA modifikovanou nukleosidy. Dodání mRNA je dosaženo koformulací molekuly do lipidových nanočástic, které chrání vlákna RNA a pomáhají jejich absorpci do buněk.[78][79][80][81]
RNA vakcíny byly prvními vakcínami covid-19, které byly povoleny ve Spojeném království, Spojených státech amerických a Evropské unii.[82][83] Autorizovanými vakcínami tohoto typu jsou vakcíny Pfizer–BioNTech[84][85][86] a Moderna.[87][88] Vakcína CVnCoV RNA od CureVac v klinických studiích selhala.[89]
Závažné alergické reakce jsou vzácné. V prosinci 2020 vedlo 1 893 360 prvních dávek vakcíny Pfizer–BioNtech ke 175 případům těžké alergické reakce, z nichž 21 bylo anafylaktických. Ze 4 041 396 podání dávek vakcíny Moderna v prosinci 2020 a lednu 2021 bylo hlášeno pouze deset případů anafylaxie. Za alergické reakce byly s největší pravděpodobností zodpovědné lipidové částice.[90]
Adenovirové přenašečové vakcíny
Nereplikující se virové přenašečové (vektorové) vakcíny používají obal adenoviru obsahující DNA, která kóduje bílkovinu SARS-CoV-2.[91][92] Vakcíny proti covidu-19 založené na virových vektorech se nereplikují, což znamená, že nevytvářejí nové virové částice, ale produkují pouze antigen, který vyvolává systémovou imunitní odpověď.[91]
Autorizovanými vakcínami tohoto typu jsou vakcína Oxford–AstraZeneca,[93][94][95] vakcína Sputnik V,[96] Convidecia a vakcína Janssen.[97][98]
Convidecia a Janssen jsou jednorázové vakcíny, které nabízejí méně komplikovanou logistiku a mohou být skladovány v běžném chlazení po dobu několika měsíců.[99][100]
Sputnik V používá Ad26 pro svou první dávku, která je stejná jako jediná dávka Janssen, a Ad5 pro druhou dávku, která je stejná jako jediná dávka Convidecia.[101]
Inaktivované vakcíny
Inaktivované vakcíny se skládají z virových částic, které vyrostly v kultuře a pak jsou zabity teplem, nebo formaldehydem, aby ztratily schopnost vyvolat onemocnění, přičemž stále stimulují imunitní odpověď.[102]
Autorizovanými vakcínami tohoto typu jsou čínské vakcíny CoronaVac,[103][104][105] Sinopharm BIBP[106] a WIBP; indický Covaxin; ruský CoviVac;[107] kazašská vakcína QazVac[108] a íránský COVIran Barekat.[109] Mezi vakcíny v klinických studiích patří vakcína Valneva.[110]
Podjednotkové vakcíny
Podjednotkové vakcíny prezentují jeden nebo více antigenů bez zavedení celých částic patogenu. Zapojené antigeny jsou často proteinové podjednotky, ale může to být jakákoli molekula, která je částí patogenu.[111]
Tři autorizované vakcíny tohoto typu jsou peptidová vakcína EpiVacCorona,[112] ZF2001,[69] a MVC-COV1901[113]. Další schválenou vakcínou je například ta od společnosti NovaVax.[8]
Vakcína V451 byla dříve v klinických studiích, které byly ukončeny, protože bylo zjištěno, že vakcína může potenciálně způsobit nesprávné výsledky pro následné testování na HIV.[114]
Nosní vakcíny
Nosní vakcíny se zaměřují na slizniční imunitu v nosní sliznici, která je portálem pro vstup viru do těla.[115][116] Tyto vakcíny jsou navrženy tak, aby stimulovaly nosní imunitní faktory, jako je imunoglobulin A.[115] Dříve byly nosní vakcíny schváleny pro jiné infekce, jako je například chřipka.[116][117]
Další typy
Mezi další typy vakcín, které jsou v klinických studiích, patří viru podobné částicové vakcíny, vícenásobné DNA plazmidové vakcíny,[118][119][120][121][122][123] lentivirové vektorové vakcíny,[124][125] konjugované vakcíny a virus vezikulární stomatitidy vykazující spike protein SARS-CoV-2.[126]
Vědci zkoumali, zda by stávající vakcíny pro nesouvisející stavy mohly nastartovat imunitní systém a snížit závažnost infekce koronaviru.[127] Existují experimentální důkazy, že BCG vakcína proti tuberkulóze má nespecifické účinky na imunitní systém, ale neexistuje žádný důkaz, že je tato vakcína účinná proti covidu-19.[128]
Výzvy
Rychlý vývoj a naléhavost výroby vakcíny proti pandemii covidu‑19 mohla a může zvýšit rizika a míru selhání při dodávání bezpečné a účinné vakcíny.[11][65][129] Jedna studie zjistila, že v letech 2006 až 2015 míra úspěšnosti získání souhlasu od fáze I. do úspěšné fáze III. klinické studie vakcín byla 16,2 % [64] a CEPI naznačuje potenciální úspěšnost pouze 10 % u kandidátů na vakcíny ve vývoji v roce 2020.[11]
Zpráva CEPI z dubna 2020 uvádí: „Bude nutná silná mezinárodní koordinace a spolupráce mezi vývojáři vakcín, regulačními orgány, tvůrci politik, finančními institucemi, orgány veřejného zdraví a vládami, aby bylo zajištěno, že nadějné kandidátní vakcíny v pozdním stadiu mohou být vyráběny v dostatečném množství a spravedlivě dodávány do všech postižených oblastí, zejména do regionů s nízkými příjmy.“[11]
Protilátkami zprostředkovaný enhancement

Ačkoli je kvalita a množství protilátek indukovaných vakcínou určena k neutralizaci infekce covid-19, vakcína může mít nezamýšlený opačný účinek tím, že způsobí protilátkami zprostředkovaný enhancement (ADE), což je zvýšená přilnavost viru k jejím cílovým buňkám, která může vyvolat cytokinovou bouři, pokud je očkovaná osoba později napadena virem.[65][130] Typ vakcíny (modifikovaná DNA nebo RNA, protein, peptid, inaktivovaný virus), dávka vakcíny, načasování přeočkování proti možnému opakování infekce covid‑19 a starší věk jsou faktory určující riziko a rozsah ADE.[65][130] Protilátková odpověď na vakcínu je proměnnou ve vývoji vakcínových technologií, včetně toho, zda má vakcína přesný mechanismus,[65] a výběr způsobu, jakým je podávána (nitrosvalová, podkožní, ústní nebo nosem).[130]
Náklady
Účinná vakcína na covid-19 by podle jednoho odborníka mohla ušetřit biliony dolarů na globálním ekonomickém propadu, a proto každá cenovka v miliardách vypadá ve srovnání s globálním propadem malá.[131] V počátečních stádiích pandemie nebylo známo, zda bude možné vytvořit bezpečnou, spolehlivou a dostupnou vakcínu pro tento virus, a nebylo přesně známo, kolik může vývoj vakcín stát.[35][40][54] Existovala možnost, že miliardy dolarů budou investovány bez úspěchu.[34]
Jakmile se vyvine účinná vakcína, je třeba vyrobit a distribuovat miliardy dávek po celém světě. V dubnu 2020 odhadovala Gatesova nadace, že výroba a distribuce mohou stát až 25 miliard amerických dolarů.[132] Z klinických studií I. fáze se 84–90 %[11][64] kandidátů na vakcínu během vývoje nedostalo ke konečnému schválení a z fáze III 25,7 %.[64] Investice výrobce do kandidáta na vakcínu může přesáhnout 1 mld. dolarů a zahrnuje miliony zbytečných dávek z důvodů daných pokročilými dohodami o výrobě.[34][35][40]
K listopadu 2020 stanovily společnosti dotované v rámci amerického programu Operation Warp Speed počáteční ceny od 19,50 do 25 $ za dávku, v souladu cenou vakcíny proti chřipce.[133] V prosinci 2020 belgická politička krátce zveřejnila důvěrné ceny dohodnuté mezi výrobci vakcín a Evropskou unií (EU), které se pohybovaly přibližně od 46 Kč do 385 Kč za dávku.[134]
| Výrobce | Cena pro EU za dávku[135] | Cena pro EU za dávku (Kč) | Počet dávek objednaných do EU[136] | Vakcína schválena v EU |
|---|---|---|---|---|
| Pfizer / BioNTech | 12,00 € | 314 Kč | 800 mil.[137] + 1800 mil.[138] | Ano |
| Moderna | 18,00 € | 385 Kč | 300 mil.[139] | Ano |
| AstraZeneca | 1,78 € | 46 Kč | 400 mil. | Ano |
| Johnson & Johnson | 8,50 $ | 222 Kč | 400 mil. (jednodávková) | Ano |
| Sanofi / GSK | 7,56 € | 198 Kč | 300 mil. | |
| CureVac | 10,00 € | 262 Kč | 405 mil. | |
| Novavax / CEPI | 200 mil. v jednání | |||
| Valneva | 60 mil. v jednání |
Historie

Vakcína proti covidu-19 může rychlým způsobem pomoci získat v populaci kolektivní imunitu bez masových ztrát na životech, poškození zdraví, chronických následků a dalších komplikací, kdy je imunita získána přirozenou cestou (tj. proděláním onemocnění). Stejně jako u jiných onemocnění, u kterých již vakcinace funguje, je k tomu potřeba proočkovanost až 70 % dospělé populace, což by mělo zabránit nekontrolovanému komunitnímu šíření nákazy.[140] Ovšem není jasné, zda vakcinovaní nebudou podstatně šířit virus dále, neboť klinické testy potvrdily určité procento ochrany proti onemocnění covid-19, avšak do jaké míry ochrání před samotným virem SARS-CoV-2 není jasné.[141][142] takže i pro ně je nadále doporučováno používat ochranné prostředky.[143]
Data zveřejněná čínskými vědci 7. dubna 2020 ukazují, že u téměř třetiny ze 175 vyléčených pacientů, kteří měli mírnější příznaky nemoci, se nevytvořily téměř žádné protilátky. Obecně měla vyšší titr (koncentraci) protilátek věková skupina 60–85 let, zatímco v mladší populaci 15–39 let byl titr třikrát nižší a někteří neměli detekovatelné množství protilátek. To značně zkomplikuje přípravu vakcín i možnost získání kolektivní imunity postupným promořením populace virovou infekcí.[144]
V současnosti neexistují vhodné zvířecí modely pro testování, kromě transgenních myší, které nesou gen pro lidský receptor ACE2. Potenciálním modelem jsou fretky a vakcíny lze eventuálně testovat in vitro, ale odhadovaná doba samotné přípravy je 3–6 měsíců. Pro vakcíny proti SARS-CoV-2 také zatím není stanoven proces zvaný Good Manufacturing Practice (cGMP). Jako vhodný cíl pro indukci protilátek se jeví kromě oslabeného nebo usmrceného viru zejména rekombinantní spike protein SARS-CoV-2 nebo virové vektory (vaccinia, adenovirus, VSV virus) nesoucí tento protein.[145] Ve Spojeném království se na jaře 2020 experimentálně testovala vakcína ChAdOx1 nCoV-19, založená na modifikovaném šimpanzím adenoviru (ChAdOx1), který není schopen infikovat lidské buňky, do něhož byla vložena informace pro S protein SARS-CoV-2.[146] Později se stala známá jako vakcína Oxford–AstraZeneca proti covidu-19.
Vakcína založená na mRNA kódující spike protein využívá lipidové nanočástice, které mRNA dopraví do buněk. Syntéza spike proteinu a jeho exprese v buňkách příjemce by měla indukovat imunitní odpověď. Tuto vakcínu vyvíjela na jaře 2020 společnost Moderna spolu s Vaccine Research Center v National Institutes of Health.[147][148][149] Také firma BioNTech začala na jaře 2020 testovat svou vakcínu založeném na stejném principu.[150]
K pasivní léčbě protilátkami je možné využít transgenní krávy, které produkují lidský imunoglobulin typu G 1 v množstvích 150–600 g/měsíc na jedno zvíře. Při imunizaci oslabeným virem SARS-CoV nebo jeho spike proteinem byly získány polyklonální imunoglobuliny, které u infikovaných myší snížily titr viru pod detekční limit.[151] Na rozdíl od přímé vakcinace lidí nehrozí komplikace, která někdy vede k tvorbě nefunkčních protilátek a infekci buněk, které nemají receptor viru (antibody-dependent enhancement of infection).[152]
První vakcíny
V listopadu 2020 bylo známo pouze šest vakcín z Číny a Ruska, schválených k omezenému testování, nebo nouzovému použití. Čínské vakcíny firem Sinovac Biotech (CoronaVac) a Sinopharm využívají oslabený nebo inaktivovaný virus SARS-CoV-2. Sinovac Biotech má však pošramocenou pověst vzhledem ke schvalování jejich vakcín, což vyvolalo otázky ohledně jejich bezpečnosti. Ředitel Sinovacu Biotech byl usvědčen z podplácení hlavního čínského regulátora Yin Hongzhanga za rychlé schvalování jejich vakcín bez dostatečného testování, k uplácení docházelo mezi lety 2007 a 2016.[153] Nouzově se v Číně očkovalo již od července 2020. V brazilské studii z ledna 2021 dosáhla vakcína CoronaVac účinnost 50,4% při prevenci symptomatických infekcí.[154] Dřívější výsledky prozatímní analýzy malého vzorku z Turecka z prosince 2020 uváděly účinnost 91 %.[155]

V srpnu 2020 byla v Rusku schválena první vakcína na světě proti covidu-19 s názvem Sputnik V, která jako nosič využívá lidský adenovirus. V říjnu byla představena druhá s názvem EpiVakKorona.[156] K říjnu 2020 byly Sputnikem V naočkovány desetitisíce lidí.[157] Účinnost vakcíny dosahovala 92 % a k zahájení hromadné produkce došlo začátkem listopadu.[158]
V říjnu 2020 bylo v EU zahájeno první průběžné hodnocení vakcíny Oxford–AstraZeneca,[159] která jako nosič využívá pozměněný šimpanzí adenovirus neschopný replikace, do jehož DNA byla rekombinací vnesena informace pro spike protein koronaviru.[160] První miliony dávek byly mohly být k dispozici začátkem roku 2021.[161] Při prvních klinických testech se jako účinnější jevila poloviční dávka vakcíny, proto se společnost zaměřuje na vyladění optimální koncentrace viru, která vyvolá maximální imunitní reakci.[162] V Evropské unii vakcínu ji podmínečně[pozn. 1] schválila Evropská komise 29. ledna 2021. Může se tak používat v celém Evropském hospodářském prostoru pro osoby starší 18 let.[163][164] V souvislosti s hlášením některých vzácných komplikací (41 případů anafylaktické reakce z celkem 5 milionů vakcinovaných ve Velké Británii) vydal Výbor pro hodnocení farmakovigilančních rizik (Pharmacovigilance Risk Assessment Committee (PRAC)) Evropské lékové agentury stanovisko, že dokumenty k vakcíně již obsahují varování před možnými vedlejšími efekty a není třeba měnit dosavadní klinickou praxi. Osoby, u nichž nastaly komplikace, by neměly obdržet druhou dávku stejné vakcíny.[165]
Vakcína Johnson & Johnson proti covidu-19 je rovněž založena na rekombinantním adenoviru (Janssen’s AdVac® technology). Ačkoli byla dostupná až v dubnu 2021,[166] získala schválení americkou FDA již 27. února 2021.[167] Firma v době schválení měla problémy s výrobou vakcíny a mohla aktuálně nabídnout pouze 4 miliony dávek. Počátkem března nabídla firma Merck & Co., že poskytne své výrobní kapacity, což umožní zvýšit produkci vakcíny Johnson & Johnson o 100 milionů dávek ještě do léta 2021.[168]

V listopadu 2020 byla oznámena 90 % účinnost RNA vakcíny Pfizer–BioNTech vyvíjené německou firmou BioNTech a distribuovanou americkým Pfizerem,[169] která k imunizaci využívá část mRNA koronaviru kódující spike protein. Vedlejším účinkem vakcinace je bolest hlavy.[170] První miliony dávek by měly být pro Evropskou unii k dispozici v prvním čtvrtletí roku 2021.[171] Cena této vakcíny, založené na zcela novém principu,[172] má být téměř sedmkrát vyšší než u vakcíny Oxford–AstraZeneca.[173]
Další mRNA vakcínu, Modernu, s účinností 94,5 % (vyšší, než předtím oznámil Pfizer), oznámila v listopadu stejnojmenná americká firma Moderna.[174][175] Tato vakcína má v nanočásticích větší koncentraci mRNA (100 μg) než ta od Pfizeru (30 μg).[176] Vakcínu schválil v pátek 18. prosince 2020 americký Úřad pro kontrolu potravin a léčiv (FDA).[177] V zájmu urychlení vakcinace vědci zvažují, zda by se vakcinační dávka firmy Moderna dala rozdělit na polovinu. Ve druhé fázi klinických zkoušek byly vyzkoušeny varianty 50 i 100 μg RNA a ve věkové skupině 18 až 55 let byla účinná i poloviční dávka vakcíny.[178] Nebyly zaznamenány žádné vedlejší účinky vakcíny kromě běžné únavy nebo bolesti svalů.[158] Podobnou účinnost (přes 94 %) má vakcína firmy Pfizer[179][180] i ruská vakcína.[181] Ve třetí fázi testování je podobná vakcína, vyvíjená německou biofarmaceutickou společností CureVac z Tübingenu.[182] Ta bude mít nejnižší koncentraci mRNA (do 12 μg).[183]
Australská univerzita v Queenslandu ve spolupráci s biotechnologickou firmou CSL a počáteční investicí 25 mil. dolarů vyvíjela vakcínu proti SARS-CoV-2, označenou jako v451. Byla založena na spike proteinu viru, jehož nativní konformace je stabilizována pomocí syntetického proteinu gp41, který vytváří tzv. molekulární svorku (molecular clamp). Vakcína užívala adjuvans MF59 (skvalen). Při testech na zvířecím modelu[184] a prvních klinických zkouškách byla potvrzena tvorba protilátek proti SARS-CoV-2, ale zároveň u části dobrovolníků byly indukovány i protilátky proti gp41, které vytvořily falešnou pozitivitu na HIV. Další klinické testy byly pozastaveny.[185]
Francouzská firma Sanofi vyvíjí ve spolupráci s firmou GlaxoSmithKline rekombinantní vakcínu s adjuvans, která je stabilní při normální chladicí teplotě (vakcíny pro pokojovou teplotu se teprve vyvíjí).[186] Při preklinických studiích na primátech tato vakcína vedla k rychlému vymizení příznaků onemocnění horních cest dýchacích a zabránila infekci plic. V klinických zkouškách vyvolala imunitní odpověď srovnatelnou s imunizací pacientů, kteří prodělali covid-19, ale pouze ve věkové skupině 18-49 let a nikoli u starších pacientů. Firma prohlásila, že upraví koncentrace antigenu a že plánuje zahájit další zkoušky v únoru 2021.[187] Vakcína by pak mohla být schválena v druhé polovině roku 2021.[188]
Vlastní experimentální vakcínu vyvinul a vyzkoušel prof. Winfried Stöcker ve své soukromé laboratoři v Gross Grönau (Šlesvicko-Holštýnsko). Stöcker byl zakladatelem úspěšné firmy Euroimmun, zaměřené na laboratorní diagnostiku, kterou prodal americké společnosti za 1,2 miliardy eur. Nyní ve své laboratoři zaměstnává kolem 50 lidí.[189] Jeho vakcína je založená na rekombinantním proteinu, který obsahuje klíčovou část spike proteinu koronaviru (Arg319-Phe541), včetně vazebného místa a čtyř nových mutací (K417N, N439K, E484K, N501Y). Vakcína obsahuje 15 mikrogramů peptidu o délce 220 aminokyselin a běžné anorganické adjuvans Alhydrogel a nehrozí u ní nebezpečí vyvolání alergické reakce. U 97 % ze stovek prvních dobrovolníků byly prokázány neutralizující protilátky proti SARS-CoV-2. Vakcína se skladuje v lyofilizovaném stavu při 4 °C a lze ji snadno připravit. Ve 2000 l reaktoru lze denně vyrobit dávku pro 1 milion lidí.[190]

První západní země, která autorizovala nouzovou aplikaci experimentální vakcíny firem Pfizer/BioNTech, byla v prosinci Velká Británie.[191] První osobou, která dostala první ze dvou potřebných dávek vakcíny se stala devadesátiletá Margaret Keenan.[192]
Společnosti Pfizer, BioNTech, nebo Moderna zahájily nebo uvedly, že brzy zahájí, testování vakcíny na dětech. Lékaři doufají, že vakcína schválená pro děti bude dostupná do začátku školního roku 2021.[193]
S objevením nového kmene koronaviru SARS-CoV-2, který se vyskytl v prosinci 2020 na jihu Anglie zahájily společnosti Pfizer, BioNTech a Moderna testování účinnosti svých vakcín proti tomuto kmeni. Dle společností však nic nenaznačuje tomu, že by vakcína neměla být účinná.[194]
Ruské úřady informovaly, že 20. ledna 2021 požádaly o registraci vakcíny Sputnik V v Evropské unii. EMA však ten samý den uvedla, že vakcína prozatím neprochází žádným přezkumem, první přezkum dokumentů se očekává k únoru.[195] Luboš Palata uvedl, že Rusko ve skutečnosti teprve zjišťovalo, jaké dokumenty bude k registraci potřebovat. V Maďarsku proti povolení vakcíny veřejně protestovala maďarská Lékařská komora, která uvedla, že „nejsou veřejně dostupné údaje“ k registraci Sputniku V.[196] EMA zahájila dne 4. března 2021 průběžné hodnocení vakcíny Sputnik V, které má ukázat, zda jsou data na dostatečné úrovni, aby mohlo být u EMA požádáno o její registraci.[197] Teprve poté bude Rusko mít možnost podat formální žádost o registraci této vakcíny.[198]
Falešné vakcíny
Interpol vydal varování, že vakcíny proti covidu-19 nelze objednat a zakoupit prostřednictvím internetu. V Jihoafrické republice mezitím policie objevila ve skladu poblíž Johannesburgu 2 400 dávek falešných vakcín a zatkla v této souvislosti tří čínské občany a jednoho Zambijce. Další výrobna falešných vakcín byla objevena přímo v Číně, kde policie zadržela 80 lidí a zabavila velké množství padělků. Generální ředitel Interpolu Jürgen Stock varuje, že v případě zločinu spojeného s vakcínami proti covidu-19 se jedná pouze o špičku ledovce. Jednotka Interpolu pro kybernetickou kriminalitu odhalila kolem 3 000 e-shopů, které podezírá z prodeje falešných léků. Zároveň 1 700 z nich obsahovalo škodlivý malware. Podle Interpolu má trh s falešnými léky, z nichž většina vzniká v Asii, roční obrat kolem 200 miliard dolarů.[199]
Hodnocení účinnosti vakcinace
Izrael, který předčil ostatní země v rychlosti vakcinace, zveřejnil první výsledky účinnosti vakcíny společností Pfizer-BioNTech, označované BNT162b2. V týdenním odstupu po první dávce se riziko nákazy snížilo o 33 %. Po druhé dávce vakcíny se v prvním týdnu nakazilo ze 428 000 pouze 0,014 % vakcinovaných a s delším než týdenním odstupem pouze 0,01 % ze 200 000 vakcinovaných.[200] Z předběžného sdělení, publikovaného v březnu 2021 v časopisu New England Journal of Medicine vyplývá, že protilátky v séru lidí vakcinovaných dvěma dávkami BNT162b2 neutralizují v pokusech in vitro všechny známé mutace SARS-CoV-2.[201] Ovšem je třeba uvést, že například podíl 99,96 % nenakažených mezi očkovanými,[202] neznamená takovou účinnost vakcíny. Ta podle své definice vždy srovnává skupinu vakcinovaných vůči skupině nevakcinovaných.
V Itálii byla zkoumána účinnost vakcinace na vzorku 248 zdravotníků a bylo potvrzeno, že sedm dní po druhé dávce vakcíny Pfizer/BioNTech mělo 99,5 % z nich specifické protilátky i buněčnou imunitu. Jako potenciálně závažný výsledek výzkumu se jeví zjištění, že u obézních lidí a lidí s hypertenzí je množství vytvořených specifických protilátek zhruba poloviční ve srovnání s jedinci s normálním nebo nižším než normálním Indexem tělesné hmotnosti (BMI).[203]
V USA byla účinnost vakcín firem Pfizer–BioNTech a Moderna vyhodnocena u téměř 4 000 zdravotníků, policistů a hasičů pracujících v první linii. Vakcinace chrání před nákazou z více než 90 %. Z celkem 2 479 plně vakcinovaných osob onemocněli pouze čtyři, ze 477 osob, které obdržely jen první dávku, byla infekce hlášena u osmi. V kontrolní nevakcinované skupině onemocnělo celkem 161 z 994 osob.[204] V květnu zveřejnilo Středisko pro kontrolu a prevenci nemocí (CDC) Spojených států souhrnné údaje o účinnosti vakcinace od celkem 101 milionů plně vakcinovaných osob. Ze statistických údajů vyplývá, že mezi lednem a dubnem 2021 se po plné imunizaci koronavirem znovu nakazilo 0,01 procenta lidí (nejedná se o účinnost vakcíny 99,99 %), 0,0007 procenta jich muselo být hospitalizováno a 0,0001 procenta jich po nákaze zemřelo.[205] CDC však dodatečně upozorňuje na to, že počet infikovaných osob byl téměř jistě vyšší, protože řadu především bezpříznakových případů nákazy se lékařům nepodařilo zaznamenat, a do budoucna budou již evidovat pouze ty případy nákazy u naočkovaných lidí, které povedou k hospitalizaci či úmrtí.[205] Podle nové studie ze září 2021 se covidem v USA znovu nakazilo 0,008 % plně vakcinovaných lidí, kteří buď potřebovali hospitalizaci, nebo zemřeli (nejsou zde tedy zahrnuty všechny možné případy infekce s méně rizikovým průběhem). Většina těchto pacientů měla další komorbidity jako je kardiovaskulární onemocnění a cukrovka 2. typu, nebo užívali imunosupresiva. Nemoci podlehli tři pacienti ve věku 65–95 let.[206]
Existují studie, že po prodělání onemocnění by dostačovala již jen jedna dávka vakcíny,[207] ale podle jiných je nedostatečná.[208]
Vakcína čínské firmy Sinovac nechrání dostatečně před další infekcí covid-19. Na Seychelách, kde je plně očkováno 60 % populace a jednu dávku dostalo 70 % lidí, nezabránilo očkování vzniku další vlny pandemie. Ve Spojených arabských emirátech nabízejí kvůli slabé imunitní odpovědi na tuto vakcínu ještě třetí očkování.[209] Ze studie Hongkongské univerzity, která porovnávala koncentrace neutralizačních protilátek u zdravotníků očkovaných vakcínou Sinovac a Pfizer/Biontech vyplývá, že účinnost mRNA vakcíny je desetkrát vyšší než u vakcíny Sinovac, založené na inaktivovaném viru.[210]
Očkovaní se znovu nakazí dvakrát méně pravděpodobně než neočkovaní lidé.[211] U očkovaných osob se předpokládá, že budou i méně infekční.[212] Nicméně výzkumy ukazují, že vliv očkování na komunitní přenos cirkulujících variant SARS-CoV-2 se zřejmě významně neliší od vlivu mezi neočkovanými osobami.[213] Například studie u varianty delta ukázaly, že očkování sice snižuje riziko nákazy v domácnosti zhruba o třetinu a snižuje rychleji virovou nálož osoby, ale plně očkovaní jedinci s průlomovými infekcemi mají vrchol virové zátěže podobný těm neočkovaným. Riziko předání nákazy v domácnosti je tedy od očkovaných i neočkovaných jedinců srovnatelné,[214][215] což dokládají i vypozorované průlomové infekce covidu-19 mezi plně očkovanými zdravotnickými pracovníky v Izraeli, kteří mohli tuto infekci přenést na své pacienty.[216][217] Přibývá totiž důkazů, že koncentrace viru setrvávajícího v horních cestách dýchacích nebo v plicích je u očkovaných a neočkovaných osob podobná, stejně jako kultivovatelnost viru.[214][215][216][218][219] Studie zkoumající účinnost bivalentních vakcín ukázala, že očkování v produktivním věku poskytovalo 29% ochranu o varianty BA.4/5, 20% ochranu u varianty Pekelný pes a 4% ochranu o varianty Kraken. S uplynulým časem se riziko onemocnění zvyšovalo.[220]
Výzkum publikovaný v roce 2022, který se zabýval reálným přínosem třetí dávky vakcíny mRNA u mladých lidí ve věku od 18 do 29 let, poukazuje na to, že na jednu hospitalizaci v důsledku onemocnění covidem-19, které se díky očkování zabrání, může připadat až 18,5 závažných vedlejších účinků vakcíny, včetně 1,5–4,6 případů myoperikarditidy (zánětů srdečního svalu) obvykle vyžadující hospitalizaci.[221] Výzkum byl však zpochybněn pro zkreslenou práci s daty.[222]
Rychlý nárůst případů koronavirového onemocnění v důsledku varianty omikronu u vysoce očkovaných populací znovu vyvolal obavy o účinnosti současných vakcín.[223] Omikronové subvarianty BA.4 a BA.5 unikají protilátkovým odpovědím jak u lidí, kteří měli předchozí infekci covid-19, tak u těch, kteří byli plně očkováni.[224] Očekává se však, že očkování bude stále poskytovat ochranu před závažným onemocněním.[224] Účinnost čtvrté dávky vakcíny na samotnou variantu omikron je tak kromě seniorů diskutabilní.[217][225] V lednu 2022 regulační orgán EU vyjádřil pochybnosti o potřebě čtvrté posilovací dávky. Přeočkovací strategie (podání vakcíny každé čtyři měsíce) může přetížit imunitní systém lidí a vést k únavě v populaci.[226]
Na konci roku 2022 tým vědců z univerzity Erlangen-Norimberk objevil jev, při němž několik měsíců po druhé dávce vakcíny začíná organismus tvořit jiný typ IgG (místo prozánětlivých podtříd IgG1 a IgG3), který je v boji s nákazou covidem-19 znatelně slabší. Při nákaze IgG4 své úspěšnější starší typy „vytlačuje“, takže se tělo hůře a pomaleji brání v důsledku snížené kapacity protilátek. Ještě hůře dopadly protilátky u posilovacích dávek vakcíny.[227]
Stav vývoje vakcín
Povolené a schválené vakcíny
Národní regulační orgány udělily povolení pro nouzového použití celkem pro čtrnáct vakcín. Šest z nich byly schváleny pro nouzové nebo úplné použití tzv. přísnými regulačními orgány (na seznamu 35 národních autorit) uznávanými Světovou zdravotní organizací.
| Vakcína vývojáři a sponzoři | Země původu | Technologie | Skladovací teplota | Aktuální fáze, účinnost (symptomatická) | Schválené nouzové použití | Plné schválení |
|---|---|---|---|---|---|---|
| Vakcína Pfizer–BioNTech proti covidu-19 (Comirnaty) BioNTech, Pfizer, Fosun Pharma | Spojené státy americké, Německo | genová, RNA vakcína, lipid. nanočástice[228] | −70 °C[229] | Třetí fáze (43 448 osob) Znáhodněná, placebem kontrolovaná studie. Pozitivní výsledky prozatímní analýzy byly oznámeny 18. listopadu 2020 a zveřejněny 10. prosince 2020 a uváděly celkovou účinnost 95 %,[230] 94,7 % ve skupině nad 65 let[231] |
| |
| Vakcína Moderna proti covidu-19 (Spikevax) Moderna, NIAID, BARDA, CEPI | Spojené státy americké | genová, RNA vakcína, lipid. nanočástice[228] | −20 °C[281] | Třetí fáze (30 000 osob) Intervenční; znáhodněná, placebem kontrolovaná studie účinnosti, bezpečnosti a imunogenicity. Pozitivní výsledky prozatímní analýzy byly oznámeny 15. listopadu 2020 a zveřejněny 30. prosince 2020 a uváděly celkovou účinnost 94,1 %,[282] 86,4 % ve skupině nad 65 let[283] | ||
| Vakcína Oxford–AstraZeneca proti covidu-19 (Vaxzevria, Covishield) Oxfordská univerzita, AstraZeneca, CEPI | Spojené království | rekombinantní, modif. šimpanzí adenovirus ChAdOx1 | +2 až +8 °C[228] | Třetí fáze (30 000 osob) Intervenční; znáhodněná, placebem kontrolovaná studie účinnosti, bezpečnosti a imunogenicity. |
| |
| Sputnik V (Gam-COVID-Vac) Gamalejův institut | Rusko | rekombinantní, lidský adenovirus Ad26 a Ad5 | +2 až +8 °C[335] | Třetí fáze (40 000 osob) Znáhodněná, dvojitě zaslepená, placebem kontrolovaná studie pro hodnocení účinnosti, imunogenicity a bezpečnosti. Účinnost je prozatím stanovena na 91,6 % (podle PCR testů, nikoli pouze symptomaticky) vůči placebo skupině na základě analýzy dat průběžné klinické studie (u skupiny nad 60 let 91,8 % po první dávce).[336] Účinnost proti závažným případům koronaviru je 100 %.[337] |
| |
| CoronaVac Sinovac | Čína | chemicky inaktivovaný kompletní virus SARS-CoV-2, hydroxid hlinitý jako adjuvans | +2 až +8 °C[382] | Třetí fáze (33 620 osob) Dvojitě zaslepená, znáhodněná, placebem kontrolovaná pro hodnocení účinnosti a bezpečnosti. Vakcína firmy Sinovac nechrání před závažným průběhem onemocnění ani po absolvování obou dávek vakcíny. V Indonésii se nakazilo a zemřelo deset zdravotníků, kteří byli plně očkovaní touto vakcínou a Seychely po 50 % proočkování populace zažily další silnou vlnu pandemie.[387] |
| |
| BBIBP-CorV Sinopharm: Pekingský institut biologických produktů, Wuchanský institut biologických produktů | Čína | chemicky inaktivovaný kompletní virus SARS-CoV-2, hydroxid hlinitý jako adjuvans | +2 až +8 °C[399] | Třetí fáze (48 000 osob) 86 %,[399] 79 %[400] Vakcína není vyzkoušena pro lidi starší 60 let a v Číně se užívá pouze pro věkové skupiny 18 až 59 let.[383] | ||
| BBV152 (Covaxin) Bharat Biotech, Indická rada lékařského výzkumu | Indie | chemicky inaktivovaný kompletní virus SARS-CoV-2, adjuvovaná | +2 až +8 °C[420] | Třetí fáze (25 800) Znáhodněná, pozorovatelem zaslepená, placebem kontrolovaná; účinnost zatím neoznámena | zatím nikdo | |
| Ad5-nCoV (Convidicea) CanSino Biologics, Pekingský biotechnologický institut Akademie vojenských lékařských věd | Čína | rekombinantní, lidský adenovirus Ad5[424] | Třetí fáze (40 000) Globální multicentrická, znáhodněná, dvojitě zaslepená, placebem kontrolovaná pro hodnocení účinnosti, bezpečnosti a imunogenicity. | zatím nikdo | ||
| EpiVacCorona (ЭпиВакКорона)[427] Vector | Rusko | peptidová vakcína[427] | Třetí fáze (40 000) Znáhodněná, dvojitě zaslepená, placebem kontrolovaná k hodnocení účinnosti, imunogenicity a bezpečnosti | |||
| Vakcína Johnson & Johnson proti covidu-19 Janssen Pharmaceuticals (Johnson & Johnson) | Spojené státy americké | rekombinantní, lidský adenovirus Ad26[228] | +2 až +8 °C[432] | Třetí fáze (40 000 osob) Znáhodněná, dvojitě zaslepená, placebem kontrolovaná Účinnost 66 % při jedné dávce[433] | ||
| CoviVac Výzkumné centrum Michaila Čumakova | Rusko | chemicky inaktivovaný kompletní virus SARS-CoV-2 | Třetí fáze (3 000 osob) Dvojitě zaslepená, znáhodněná, placebem kontrolovaná k hodnocení účinnosti a bezpečnosti. |
| zatím nikdo | |
| ZF2001 (RBD-Dimer) Anhui Zhifei Longcom Biopharmaceutical Co. Ltd. | Čína | peptidová vakcína | 2–8 °C | Třetí fáze (29 000 osob) Dvojitě zaslepená, znáhodněná, placebem kontrolovaná |
| zatím nikdo |
| WIBP-CorV Sinopharm | Čína | chemicky inaktivovaný kompletní virus SARS-CoV-2 | Třetí fáze (51 600 osob) Dvojitě zaslepená, znáhodněná, placebem kontrolovaná |
| zatím nikdo | |
| QazCovid-in Výzkumný ústav pro problémy biologické bezpečnosti | Kazachstán | chemicky inaktivovaný kompletní virus SARS-CoV-2 | Třetí fáze (3 000 osob) zaslepená, znáhodněná, placebem kontrolovaná |
| zatím nikdo |
Kandidáti na vakcínu proti covidu-19 v I. až III. fázi klinických studií
| Název Výrobce | Technologie | Skladovací teplota | Aktuální fáze klinických studií, účinnost | Předpoklad schválení |
|---|---|---|---|---|
| NVX-CoV2373 Novavax a CEPI | rekombinantní, S protein,[445] nanočásticově MatrixM adjuvovaná[228] | +2 až +8 °C | Třetí fáze (45 000) Znáhodněná, placebem kontrolovaná studie zaslepená pozorovatelem Účinnost 89 %[446] a proti novým mutacím viru předběžně 85 % | |
Sanofi / GSK | rekombinantní, bakulovirus, AS03 adjuvovaná[228] | +2 až +8 °C[447] | 2. polovina roku 2021 | |
| ZF2001 Anhui Zhifei Longcom Biopharmaceutical | Vakcína podjednotky (rekombinantní) | Třetí fáze (29 000) Znáíhodnění, dvojitě zaslepená, placebem kontrolovaná | ||
| Zorecimeran (CVnCoV) CureVac | genová, RNA vakcína, lipid. nanočástice[228] | +5 °C[448] | Třetí fáze (36 500) Fáze 2b/3: Multicentrická studie účinnosti a bezpečnosti u dospělých | 3. čtvrtletí 2021 |
| ZyCoV-D Cadila Healthcare | DNA vakcína (plazmid exprimující protein SARS-CoV-2 S) | Třetí fáze (26 000)[449] | ||
| VLA2001 Valneva | inaktivovaný kompletní virus, hydroxid hlinitý a CpG 1018 jako adjuvans[450] | +2 až +8 °C | ||
| Medigen Vaccine Biologics Corp. (MVC) , Tchaj-wan | podjednotková vakcína obsahující stabilizovaný SARS-CoV-2 spike antigen, hydroxid hlinitý a CpG 1018 jako adjuvans[451] | Druhá fáze (3 700, včetně 850 seniorů> 65), 28.4.2021[452] |
Vakcíny v České republice a některých dalších státech
Česká republika si vakcínu zatím neobjednává sama, ale podle rozhodnutí z léta 2020 jsou vakcíny objednávány centrálně Evropskou komisí (EK). Poté jsou rozdělovány mezi státy Evropské unie (EU) podle počtu obyvatel. Tím je do značné míry zajištěna spravedlnost. Větší státy nemohou objednávat na úkor menších, je naplněn princip evropské soudržnosti a vůči výrobcům je při jednání EU ve větší výhodě, neboť jedná za 450 milionů obyvatel. Členské státy uzavřely s EU dohodu, že nebudou zahajovat paralelní jednání s výrobci, kteří se účastní kolektivního vyjednávání o dodávkách vakcíny s Evropskou komisí do EU. Evropská komise zajistila pro EU 4,2 miliardy dávek vakcín, tedy téměř desetkrát více než odpovídá populaci Unie. K lednu 2022 bylo dodáno 1,3 miliardy dávek. Česko pro roky 2020 až 2023 objednalo celkem 48 741 454 dávek, přičemž dodáno už bylo přes 29 milionů. Zdravotníci podali 17,6 milionu dávek. Česko za vakcíny zaplatilo 12 085 840 834 korun. Část nevyužitých dávek Česko daruje.[453] Část vakcín zhruba za miliardu korun byla zlikvidována.[454]
Jednotlivé státy však mohou vyjednávat s dodavateli, kteří nespadají pod centrální systém EU a schválit dočasné nouzové povolení. V lednu 2021 zahájilo Maďarsko vyjednávání o dodávkách ruské vakcíny Sputnik V a čínské vakcíny od firmy Sinopharm,[455] u čínské vakcíny však panují pochybnosti o její deklarované účinnosti.[455] Vakcína je ale patrně účinná a bezpečná.[456]
Česko mělo k lednu 2021 objednáno zhruba 16 milionů dávek vakcíny.[457] Čísla se však mění podle toho, jaký je stav vyjednávání Evropské komise o dodávkách.[457]Ke květnu 2021 se v České republice očkuje vakcínami Pfizer–BioNTech, Modernou, a Oxford–AstraZeneca a Johnson & Johnson.[458]
Izrael, Spojené království a Spojené státy americké dosáhly rychlejšího postupu očkování než Evropská unie, protože vyjednaly své smlouvy s výrobci a dodavateli dříve než EU a platí vyšší cenu, případně slíbily dodávat data o očkování.[459] Rychlejšího proočkování obyvatelstva než v EU dosáhly do začátku března 2021 také Spojené arabské emiráty, Chile a Maroko.[460]
V listopadu 2020 ohlásilo Německo výstavbu velkokapacitních očkovacích center pro všechny městské a zemské okresy[461] s dokončením do 15. prosince 2020 včetně zajištění podpůrné logistiky.[462] Tato centra byla od 24. prosince 2020 v provozu, avšak ještě začátkem března 2021 nebyla pro určitý nedostatek očkovacích látek plně vytížená. Uvažuje se o zapojení praktických lékařů do očkovací kampaně.

Dne 12. prosince 2020 prohlásil český ministr zdravotnictví Jan Blatný, že v Česku není zapotřebí mnoho velkých očkovacích center a že k očkování budou využity mj. nemocnice, avšak regiony začaly očkovací centra připravovat.[463][464] Dne 12. ledna 2021 oznámil premiér Babiš, že vláda postaví velké očkovací centrum v sále kongresového centra O2 universum a jeho poradce Prymula sdělil, že začne fungovat do konce ledna,[463] ale 1. března bylo oznámeno, že začne fungovat až 11. dubna 2021.[465]
Koncem ledna 2021 byl v Česku nedostatek vakcín, očkování se tak muselo utlumit a rezervace byly pozastavené.[466] V únoru daroval Česku 5 000 dávek vakcín Izrael a 100 000 dávek poskytne Francie.[467][468] Tři spolkové země Německa (Sasko, Bavorsko a Durynsko) slíbily poskytnout celkem 15 000 dávek vakcín.[469]
První dávky vakcíny Oxford–AstraZeneca dorazily do České republiky 5. února 2021, do konce toho měsíce se očekávalo celkem 81 tisíc dávek.[470] Očkování touto vakcínou však v druhé polovině února 2021 nabralo zpoždění kvůli nevyjasněnému systému distribuce a také kvůli nejasnostem ohledně použití této vakcíny pro věkovou kategorii nad 65 let, protože tato aplikace byla sice Evropskou lékovou agenturou (EMA) schválena, ale v České republice a v řadě jiných států k ní panuje nedůvěra,[471] přestože vakcína chrání i seniory.[472] Systém distribuce a rezervace vakcín Oxford–AstraZeneca u praktických lékařů je komplikovaný, což zpomaluje očkování.[473] Zásoby nevyočkovaných vakcín v ČR neustále stoupají (k 10. březnu 2021 je v ČR celkem přes 219 000 nevyočkovaných vakcín).[474] Od března 2021 mělo očkování v ČR zrychlit.[475] Protože v březnu 2021 neexistoval v ČR způsob, jak využít nespotřebované vakcíny (objednaný člověk nedorazí), některé byly zlikvidovány (k 11. březnu 2021 to bylo 664 dávek, převážně vakcíny firmy Pfizer).[476]
Ke dni 17. prosince 2023 bylo celkem v České republice plně naočkováno 6 479 551 osob, částečně naočkováno 495 988 osob a celkem tak obdrželo alespoň jednu dávku vakcíny 6 975 539 lidí. Podrobnější informace o očkování v České republice jsou v článku Pandemie covidu-19 v Česku.
Vedlejší účinky a úmrtí v Česku
K dubnu 2021 bylo hlášeno na 3 091 nežádoucích účinků po očkování a 39 úmrtí po aplikaci vakcíny, Lékový ústav prověřoval souvislost.[477] Do června 2022 přijal SÚKL více než 12 000 hlášení na nežádoucí účinky očkování proti covidu a prověřoval 174 úmrtí (do dubna 2022). SÚKL potvrdil, že eviduje jeden případ úmrtí, jenž pravděpodobně souvisí s očkováním proti covidu, kde příčinou smrti byla trombóza po vektorové vakcíně.[478]
Vývoj české vakcíny
Vláda roku 2020 poskytla 30 milionů korun na vývoj vlastní české vakcíny proti covidu-19. Vedením týmu pověřila kardioložku a poslankyni za ANO Věru Adámkovou, vědeckým vedoucím byl Marek Petráš. V první fázi probíhaly experimenty s vakcínou na principu oslabeného živého viru na hlodavcích a byly dokončeny v září 2020.[479]
Celý projekt od počátku kritizovala řada odborníků, včetně předsedy České vakcinologické společnosti Romana Chlíbka. Ředitel Biologického centra AV ČR, virolog Libor Grubhoffer k tomu uvedl: „Považuji tento projekt za naivní a vynaložené finanční prostředky za zmařené. Je to nesmírně zastaralý přístup východního typu a nepochopení situace, která vládne v oblasti farmaceutické výroby a byznysu.“ Přestože výsledky výzkumu nebyly publikovány a Ministerstvo zdravotnictví další výzkum nedoporučilo, v březnu 2021 vláda změnila názor a chce uvolnit dalších 250 milionů korun na pokračování projektu. Kromě odborníků toto rozhodnutí kritizovali i opoziční poslanci.[480] Někteří odborníci se staví pozitivně a např. vidí ve vyvíjené vakcíně strategickou výhodu.[481]
Možná rizika a kontroverze

Kromě běžných příznaků spojených s vakcinací, jako lokální bolest, únava nebo mírná horečka, vyvolaly pozornost zprávy v tisku o ojedinělých případech krevních sraženin a plicních trombóz, které byly dávány do souvislosti zejména s vakcínou Oxford–AstraZeneca. Dvě desítky zemí přerušily v březnu 2021 vakcinaci tímto přípravkem a čekají na verdikt Evropské lékové agentury (EMA). Pozastavení přišlo nedlouho poté, co začátkem března po podání vakcíny Oxford–AstraZeneca zemřela v Rakousku devětačtyřicetiletá, na Slovensku osmatřicetiletá a v Dánsku šedesátiletá žena, úmrtí souvisely s poruchami krevní srážlivosti.[482][483]
Evropská léková agentura (EMA) prohlásila, že vakcíny Oxford–AstraZeneca a Johnson & Johnson mohou v krajních případech vyvolat krevní sraženiny, ale přesto přínos převažuje nad rizikem.[484] Podle statistik, které zveřejnila Britská regulační agentura, bylo z celkem 10,7 milionu lidí naočkovaných v Británii v souvislosti s vakcínou Pfizer–BioNTech registrováno 38 případů trombózy, což je 0,0004 %. Vakcínu Oxford–AstraZeneca dostalo 9,7 milionu osob a trombóza se vyskytla ve 30 případech, což je 0,0003 %. Statistiky společnosti AstraZeneca uvádějí, že po naočkování více než 17 milionů lidí bylo registrováno 15 případů hluboké žilní trombózy a 22 případů plicní embolie. Taková frekvence žilních příhod odpovídá běžnému výskytu ve starší populaci, která dostala ve všech státech přednost a nemá příčinnou souvislost, ale pouze časovou shodu s vakcinací.[485][486]
Totéž platí pro statistiky úmrtnosti. Americké Středisko pro kontrolu a prevenci nemocí (CDC) uvádí četnost u očkovaných 0,002 procenta a podle úřadu mezi úmrtími a očkováním neexistuje žádná vazba. Britský úřad pro léky uvedl, že do 28. února 2021 evidoval celkem 227 brzkých úmrtí po podání vakcíny Pfizer–BioNTech a 275 po podání vakcíny Oxford–AstraZeneca. Naprostá většina se týkala starších lidí nebo vážně nemocných a nic nenaznačuje, že by úmrtí souviselo s očkováním. Také Norsko, Německo, Hongkong a Výbor Světové zdravotnické organizace uvádějí, že počet úmrtí vakcinovaných osob odpovídá běžné mortalitě v této populační skupině a přínos vakcíny přesahuje rizika.[487]
Zodpovědnost za nežádoucí účinky vakcín v EU nesou jejich výrobci, ale patrně se nevztahuje na ty vedlejší účinky, i závažnější, které jsou v příbalové informaci k vakcíně.[488][489]
K 23. září 2021 Evropská léková agentura (EMA) evidovala přibližně jeden milion případů možných nežádoucích účinků po očkování vakcínami proti onemocnění covid-19. Dále uváděla, že podezření na závažné nežádoucí účinky byly hlášeny u přibližně 75 000 osob po očkování vakcínou Pfizer.[490][491] K 30. září 2021 pak EMA informace upravila s tím, že možných vedlejších účinků vakcín bylo méně než 700 tisíc.[490] EMA dále uváděla, že po očkování zemřelo přibližně 5 731 osob (v rámci EU),[491][492] (pro srovnání 5 201 lidí k červenci 2021[492]). Na základě toho europoslankyně Virginie Joronová v září roku 2021 podala neúspěšný návrh na zřízení fondu pro odškodnění obětí očkování proti onemocnění covid-19. Joronová uvedla, že o fond usiluje také z toho důvodu, že poslanci Evropského parlamentu neměli přístup k vyjednávání o smlouvách, které Evropská komise (EK) uzavírala s farmaceutickými společnostmi, a dále proto, že podle jejího názoru si EK nepřála, aby farmaceutické laboratoře nesly jakoukoli odpovědnost.[490][491]
K lednu 2022 Evropská léková agentura (EMA) evidovala 913 330 případů možných nežádoucích účinků po očkování vakcínami proti onemocnění covid-19, z toho 522 530 případů u vakcíny Pfizer BioNTech z 545 milionů očkovaných, 231 363 případů u vakcíny AstraZeneca z 69 milionů očkovaných, 124 410 případů u vakcíny Moderna ze 103 milionů očkovaných a 35 027 případů u vakcíny Janssen z 19 milionů očkovaných.[493] Z těchto nahlášených podezření na nežádoucí účinky se v rámci EU jednalo o 8 807 úmrtí, z toho 6 490 lidí po vakcíně Pfizer, 1 378 osob po vakcíně AstraZeneca, 685 lidí po vakcíně Moderna a 254 osob po vakcíně Janssen.[493] Na základě této skutečnosti byl 14 poslanci v březnu 2022 znovu podán neúspěšný návrh na zřízení fondu pro odškodnění obětí očkování proti onemocnění covid-19.[494]
Skandinávská studie vycházející z dat z Norska, Dánska a Finska, zveřejněná v létě 2022 na webu JAMA, časopisu vydávaného Americkou lékařskou asociací, zjistila souvislost mezi vakcínou proti covidu-19 a vyšším výskytem jak mozkové žilní trombózy, tak i trombocytopenie.[495]
Čínští vědci na konci roku 2022 publikovali studii, v níž zkoumali opakované posilující dávky, které aplikovali myším, a došli k závěru, že mohou narušit protilátkovou i buněčnou imunitu.[496]
V dubnu roku 2023 zahltily nemocnici v německém Marburgu tisíce pacientů stěžující si na poškozené zdraví po vakcinaci proti covidu-19.[497]
Kontroverze
Podle zpravodajského serveru Echo24, v článku vydaném 18. ledna 2023, sedm švédských lékařů v otevřeném dopise vyzývalo svou vládu, aby okamžitě zastavila masové očkování posilující dávkou s odkazem na několik nedávných studií o korelaci mezi vakcínou proti covidu-19 a nárůstem případů myokarditidy a také perikarditidy.[498]
V březnu 2023 japonský zákonodárce Yanagase Hirofumi obvinil japonskou vládu ze zatajování poškození a úmrtí způsobená mRNA vakcínami proti covidu-19.[499] Vyjádřil jisté pochybnosti s ohledem na podezřelý nárůst počtu úmrtí, kdy v roce 2022 přesáhl počet mrtvých 1 580 000 (nejvíce od druhé světové války) a že oproti roku 2021 se počet mrtvých zvýšil o více než 140 tisíc,[499][500][501][502] přičemž k říjnu 2021 bylo plně naočkováno už celkem 70 % populace.[503] Za manipulativní považuje také to, že bylo oficiálně nahlášeno pouze jedno úmrtí související s vakcínou, přestože je známo asi 2000 podezření na úmrtí po očkování, z toho u 260 označil odpovědný lékař pravděpodobnou souvislost s očkováním a 52 případů bylo dokonce potvrzeno pitvou.[499][504]
Na serveru iDNES vyšel 19. dubna 2023 rozhovor s imunologem Vojtěchem Thonem z Centra RECETOX Masarykovy univerzity v Brně, který označil mRNA vakcínu za genovou terapii, nebo že vakcína může paradoxně způsobit těžší průběh onemocnění.[505] Na to reagoval na svém twitterovém účtu imunolog Zdeněk Hel z University of Alabama at Birmingham, který považuje některá jeho tvrzení za nepravdivá nebo matoucí.[506]
Stav očkování proti covidu-19
Evropský komisař pro jednotný trh Thierry Breton koncem března 2021 prohlásil, že Evropská unie je schopna s využitím dostupného očkování proti covidu-19 dosáhnout imunity na celém kontinentu do 14. července 2021.[507] Očkování je dobrovolné,[508] a v dubnu 2021 převažoval v mnoha zemích postoj, že by mělo být povinné.[509]
Povinné očkování
WHO ke konci roku 2020 informovala o tom, že nepředpokládá, že by očkování, vzhledem k povaze vakcín (tj. relativně nových), mělo být povinné.[510] Na počátku roku 2022 bylo povinné očkování některými odborníky doporučováno a považováno za to, co není v rozporu s lidskými právy.[511] Důvodem byl veřejný zájem, a to, že klady vakcín podle zastánců významně převažují nad negativy.[512][511] Jiní odborníci nebo skupiny bojující za lidská práva se s těmito názory neshodují, například proto, že podle nich je povinné očkování proti covidu-19 zřídka opodstatněné.[513][514][515][516][517][221] Ačkoli vakcíny prokazují účinnost proti onemocnění covid-19, váhavost vůči očkování odhaluje obavy z krátkodobých a dlouhodobých vedlejších účinků, nebo nežádoucích účinků, jako je úmrtí po očkování. Navíc důkazy svědčí o tom, že očkování nemůže zaručit prevenci infekce a dokonce ani opětovné infekce, nebo, že očkovaný nemoc nebude šířit dál.[513][213][518]
V závěru roku 2021 bylo povinné očkování proti covidu-19 zavedeno v některých zemích EU:[519]
- Itálie – zdravotníci, pracovníci v sociálních službách
- Francie – zdravotníci, sociální pracovníci, hasiči, policisté
- Maďarsko – zdravotníci, státní zaměstnanci
- Rakousko – povinné očkování od 1. 2. 2022 pro všechny
- Řecko – zdravotníci, zaměstnanci pečovatelských domů
- Spojené království – zaměstnanci pečovatelských domů, od dubna 2022 i zdravotníci
- Ukrajina – zaměstnanci veřejného sektoru včetně učitelů, návrh na rozšíření povinnosti pro zdravotníky a zaměstnance magistrátu
Odkazy
Poznámky
Reference
V tomto článku byl použit překlad textu z článku COVID-19 vaccine na anglické Wikipedii.
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu vakcína proti covidu-19 na Wikimedia Commons
Obrázky, zvuky či videa k tématu vakcína proti covidu-19 na Wikimedia Commons - SÚKL: Příbalové informace k vakcínám proti covid-19 Archivováno 4. 12. 2021 na Wayback Machine.
- SÚKL: Aktualizace bezpečnosti vakcín proti covid-19
- Protokol mRNA-1273-P301 [online]. Moderna. Dostupné online.
- Protokol C4591001 PF-07302048 (BNT162 RNA-Based COVID-19 Vaccines) [online]. Pfizer [cit. 2021-01-06]. Dostupné v archivu pořízeném dne 2020-09-28.
- Protokol AZD1222 – D8110C00001 [online]. AstraZeneca. Dostupné online.
- Protocol VAC31518COV3001; Phase 3 [online]. Janssen Vaccines & Prevention. Dostupné online.
