锗
即使地球表面上鍺的豐度地殼蘊含量相對较高,但由於礦石中很少含有高濃度的鍺,所以它在化學史上發現得比較晚。德米特里·伊万诺维奇·门捷列夫在1869年根據元素周期表的位置,預測到鍺的存在與其各項屬性,並把它稱作eka-矽。克萊門斯·溫克勒於1886年在一種叫硫銀鍺礦的稀有礦物中,除了找到硫和銀之外,還發現了一種新元素。儘管這種新元素的外觀跟砷和锑有點像,但是新元素在化合物中的化合比符合硅下元素的預測。温克勒以他的國家——德国的拉丁語名來為這種元素命名。
鍺是一種重要的半导体材料,用於製造晶体管及各種電子裝置。主要的終端應用為光纖系統與紅外線光學,也用於聚合反應的催化剂,制造電子器件與太陽能電力等。現在,開採鍺用的主要礦石是閃鋅礦(锌的主要礦石),也可以在銀、铅和铜中,用商業方式提取鍺。一些鍺化合物,如四氯化鍺(GeCl4)和甲锗烷(GeH4),会刺激眼睛、皮膚、肺部與喉嚨。
发现史
門捷列夫於1869年發表了一份名為《化學元素週期律》的研究報告,當中預測了數種未知元素的存在,其中一種填補了碳族中硅及錫之間的空缺[5]。由於它在週期表的位置,門捷列夫把它命名為擬硅(Ekasilicon, Es),並將其原子量定為72。

1885年夏季,在薩克森王國弗赖堡附近的一個礦場,發現了一種新的礦物。由於這種礦物的含銀量高,所以被命名為硫銀鍺礦[b]。克萊門斯·溫克勒檢驗了這種礦物,並於1886年成功從中分離出一種與銻相似的元素[6]。在他發表成果之前,他原本打算用海王星來為新元素命名,因為在1846年被發現的海王星,數學理論也預測它的存在[c]。然而,镎(Neptunium)這個名字當時已被另一元素佔用(不過不是今天叫镎的那種元素,它到1940年才被發現)[d],因此溫克勒改用他的祖國——德國的拉丁語(germanium)來為元素命名[6]。由於鍺跟砷和銻相近,所以它當時是否該出現在週期表上仍備受爭論,不過它的性質與門捷列夫的擬硅很像,因此才確立了它在週期表的確實位置[6][7] 在發現後,薩克森的礦場再給了溫克勒五百公斤的礦石,因此他能進行後續研究,並在1887年確立了這種新元素的化學性質[8][9][10]。他通過分析純四氯化鍺,得出鍺的原子量為72.32,而德布瓦博德蘭則通過比較該元素的火花光譜線,得出72.3[11]。
溫克勒當時成功製備了幾種新的鍺化合物,包括氟化物、氯化物、硫化物、二氧化鍺及四乙基鍺,而四乙基鍺則是第一種有機鍺烷[9]。有了從這些化合物而來的物理數據——它們符合門捷列夫的預測——鍺的發現成為了確認門捷列夫元素週期的重要證據。下表比較了預測與溫克勒的數據[9]:
| 特性 | 擬硅(预测) | 鍺 |
|---|---|---|
| 原子質量 | 72 | 72.59 |
| 密度(g/cm3) | 5.5 | 5.35 |
| 熔點(℃) | 高 | 947 |
| 顏色 | 灰色 | 灰色 |
| 氧化物種類 | 耐火(refractory)二氧化物 | 耐火二氧化物 |
| 氧化物密度(g/cm3) | 4.7 | 4.7 |
| 氧化物性质 | 弱鹼 | 弱鹼 |
| 氯化物熔點 | 100℃以下 | 86℃ (GeCl4) |
| 氯化物密度(g/cm3) | 1.9 | 1.9 |

直至1930年代末期,科學家們一直以為鍺只是一種導電性差的金屬[12]。因為它的半導體特性對電子元件來說是非常有價值的,所以到1945年鍺成了一種有利可圖的材料。在第二次世界大戰期間的1941年,鍺二極體就開始取代電子裝置中的真空管[13][14]。它的第一項主要用途為製造蕭特基二極體的接點,該二極體在二戰期間用於雷達接收[12]。第一種矽鍺合金誕生於1955年[15]。在1945年以前,鍺的年產量只有幾百千克,但到了1950年代末,世界年產量就已經達到40公噸[16]。
鍺晶體管在1948年的出現[17],開啟了固態電子無數的應用之門[18]。從1950年至1970年代初,這個領域為鍺提供了增長中的市場,但之後晶體管、二極體和整流器都開始轉用高純度硅[19]。硅的電子特性比鍺優越,但是所需的純度就高得多——這樣的純度用早年的商業方法實在達不到[20]。
與此同時,光纖通訊網絡、紅外線夜視系統及聚合反應催化劑對鍺的需求量正在急速增長[16]。這些終端應用代表了2000年鍺用量的80%[19]。美國政府甚至把鍺定為戰略及關鍵材料,並因此於1987年下令國家防禦儲備中心存入132公噸的鍺[16]。生產鍺與硅不同的是,硅的產量只受生產力限制,而鍺的產量則受開採來源的短缺所限制。正因如此,硅在1998年的價格為每千克10美元以下[16],而當時鍺的價格達每千克1800美元[16]。
特性
在標準狀況下,鍺是一種銀白色的半金屬元素,硬但易碎[21]。這種形式構成一種同素異形體,技術上叫α鍺,它帶金屬光澤,結構與鑽石一樣,為鑽石立方晶體結構[19]。當壓力高於120kPa時,會形成另一種同素異形體,叫β鍺,它的結構與β錫一樣[22]。與硅、鎵、鉍、銻與水一樣,鍺在熔化態固體化時(即凝固)會膨脹[22],而有這種特性的物質並不多。
鍺是一種半導體。用區熔技術生產出的半導體用鍺晶體,其雜質含量只有一百億分之一[23],因此這種晶體是史上最純的材料之一[24]。第一種在極強電磁場下成為超導體的金屬材料,是一種含鍺、銠和鈾的合金,於2005年被發現[25]。
已知純鍺能自發地擠出非常長螺旋位錯,叫“鍺鬚”。這些晶鬚的增長,是較舊的鍺製二極體和晶體管壞掉的主要原因,因為晶鬚很可能會構成短路,但短路與否視最終接觸到的物質而定[25]。
化學性质
在250℃時,鍺會緩慢地氧化成GeO2[26]。鍺不溶於稀酸及鹼,但溶於濃硫酸,並與熔鹼反應,生成鍺酸鹽(GeO32-)。鍺最常出現的氧化態是+4,但是已知它在不少化合物中的氧化態為+2[27]。其他的氧化態則很罕見,例如化合物Ge2Cl6中为+3,以及在氧化物表面測得的+3與+1氧化态[28],或者鍺化物中的負氧化態,像是Mg
2Ge中的-4。多種含鍺的陰性簇離子(津特耳離子)已經被製備出來,當中包括Ge42-、Ge94-、Ge92-及[(Ge9)2]6-,其中一種方法是在乙二胺或穴醚的催化下,從置於液態氨的鍺與鹼金屬合金中進行提取[27][29]。這些離子中鍺的氧化態並非整數——這點跟臭氧根離子中的氧一樣。
已知鍺共有兩種氧化物:二氧化鍺和一氧化鍺[22]。焙燒二硫化鍺(GeS2)後可得二氧化鍺,二氧化鍺是一種白色的粉末,微溶於水,但與鹼反應並生成鍺酸鹽[22]。當二氧化鍺與鍺金屬在高溫下反應時,會生成一氧化鍺[22]。二氧化鍺(及其相關的氧化物及鍺酸鹽)有一種很不尋常的特性,就是對可見光有着高折射率,但同時對紅外線隱形[30][31]。而鍺酸鉍則被用作閃鑠器(scintillator)[32]。
鍺還能與其它氧族元素生成二元化合物,例如二硫化物(GeS2)、二硒化物(GeSe2)、一硫化物(GeS)、一硒化物(GeSe)及碲化物(GeTe)[27]。把硫化氫氣體通過含Ge(IV)的強酸溶液時,會生成白色沉澱物,即二硫化鍺[27]。二硫化鍺能很好地溶於水、苛性鈉溶液及鹼金屬硫化物溶液中。但是,它不溶於酸性溶液,溫克勒就是凭借這項性質才發現了鍺[33]。把二硫化鍺置於氫氣流中加熱,會生成一硫化鍺(GeS),它昇華後會形成一圈色暗但具金屬光澤的薄層,它可溶於苛性鈉溶液中。把一硫化鍺、鹼金屬碳酸鹽與硫一起加熱後,會生成一種鍺鹽化合物,叫硫代鍺酸鹽[34]。
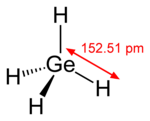
鍺共有四種已知的四鹵化物。在正常狀況下四碘化鍺(GeI4)為固體,四氟化鍺(GeF4)為氣體,其餘兩種為揮發性液體。把鍺與氯一塊加熱,會得到一種沸點為83.1℃的無色發煙液體,即四氯化鍺[22]。鍺的所有四鹵化物都容易水解,生成带结晶水的二氧化鍺[22]。四氯化鍺用於製備有機鍺化合物[27]。跟四鹵化物相反的是,全部四種已知的二鹵化物,皆為聚合固體[27]。另外已知的鹵化物還包括Ge2Cl6及GenCl2n+2[22]。還有一種奇特的化合物Ge6Cl16,其中含有类似新戊烷結構的Ge5Cl12[35]。
甲鍺烷(GeH4)是一種結構與甲烷相近的化合物。多鍺烷(即與烷烃相似的鍺化合物)的化學式為GenH2n+2,現時仍沒有發現n大於五的多鍺烷[27]。相對於硅烷,鍺烷的揮發性和活性都較低[27]。GeH4在液態氨中與鹼金屬反應後,會產生白色的MGeH3晶體,當中含有GeH3−陰離子[27]。含一、二、三個鹵素原子的氫鹵化鍺,皆為無色的活性液體[27]。

溫克勒於1887年合成出第一種有機鍺化合物(organogermanium compound);四氯化鍺與二乙基鋅反應生成四乙基鍺(Ge(C2H5)4)[9]。R4Ge型(其中R為烴基)的有機鍺烷,如四甲基鍺(Ge(CH3)4)及四乙基鍺,是由最便宜的鍺前驅物四氯化鍺及甲基親核劑反應而成。有機鍺氫化物,如異丁基鍺烷((CH3)2CHCH2GeH3)的危險性比較低,因此半導體工業會用液體的氫化物來取代氣體的甲鍺烷。已知鍺有不少活性中間物:鍺代自由基、鍺烯(與碳烯相近)和鍺炔(與卡賓相近)[36][37]。有機鍺化合物2-羧乙基鍺倍半氧烷(2-carboxyethylgermasesquioxane),於1970年被發現,曾經有一段時間被用作膳食補充劑,當時認為它可能對腫瘤有療效[38]。
同位素
鍺共有五種天然存在的同位素:70Ge、72Ge、73Ge、74Ge和76Ge。當中,76Ge帶微弱的放射性,其衰變模式為雙β衰變,半衰期為1.58 × 1021年。74Ge是最常見的同位素,豐度約為36%。76Ge的自然豐度是最低的,約為7%[39]。當72Ge被α粒子轟擊時,會產生穩定的77Se,並在過程中釋放出高能量的電子[40]。因此,它與氡組合後可用作核電池[40]。
鍺最少有27種合成放射性同位素,各原子質量介乎58至89之間。當中最穩定的是68Ge,其衰變模式為電子捕獲,半衰期則為270.95 d。而當中最不穩定的則是60Ge,其半衰期為30 ms。儘管大部份鍺同位素的衰變模式皆為β衰變,但是也有例外。61Ge及64Ge的衰變模式為β+遲延質子發射(proton emission)[39],而84Ge至87Ge則有可能進行β-遲延中子發射[39]。
自然豐度
鍺是由恆星核合成所創造的,主要是透過漸近巨星分支上恆星內的S-過程。S-過程是一種慢中子捕獲過程,發生於脈衝紅巨星中的輕元素[41]。在木星的大氣層中能探測到鍺[42],在一些遙遠的恆星中也能探測到鍺[43]。鍺在地球的地殼豐度約為1.6 ppm[44]。含鍺量可觀的礦石只有幾種,如硫銀鍺礦、灰鍺礦(briartitie)、硫鍺銅礦(germanite)及硫鍺鐵銅礦(renierite),而它們都沒有可供開採的礦床。儘管如此,開採這些礦石都不是為了它們所含的鍺[19][45]。一些鋅銅鉛礦體的含鍺量夠高,因此可以從它們最終的濃縮礦物中提取鍺[44]。
德國礦物學家威特·戈斯密(Victor Goldschmidt)在測量鍺礦床時,發現了一種奇特的濃縮過程,它使得一些煤礦層能擁有高含鍺量[46][47]。最高的含鍺量出現在英國諾森伯蘭郡哈特萊村(Hartley)的煤灰中,達1.6%[46][47]。內蒙古錫林浩特市附近的煤礦層含鍺量估計達1600公噸[44]。
製備

2007年鍺的年生產量約為100公噸[19]。現在,主要的方法是從鍺濃度達0.3%的閃鋅礦中提取鍺[48],它是當中的副產品,這種礦石最常出現於以沉積物為主體的大型Zn-Pb-Cu(-Ba)礦床,及以碳酸鹽為主體的Zn-Pb礦床[44]。儘管沒有全球鍺儲備量的確實數字,但是估計美國的儲備量約在500公噸左右[44]。在2007年,鍺的需求量有35%是由循環再造所滿足[44]。
鍺主要是由閃鋅礦中製取,而閃鋅礦是一種鋅礦石,但是也可以在銀、鉛及銅礦中找到鍺。若煤炭發電廠用的煤是從高鍺濃度的礦床來的話,那麼發電廠的飛灰(fly ash)也是鍺的一個來源。俄羅斯與中國都有在用這種鍺源[49]。俄羅斯的鍺礦床位於其遠東的庫頁島,而海參崴東北的煤礦也被用作鍺源[44]。中國的鍺礦床主要位於雲南省臨滄市的褐煤礦場,及內蒙古自治區錫林浩特市附近的煤礦,而它們都是開採中的鍺源[44]。
鍺的大部份濃縮礦物為硫化物;它們在空氣中加熱後會變成氧化物,這個過程叫焙燒(roasting):
- GeS2 + 3O2 → GeO2 + 2SO2
在這個過程中,部份鍺會進到所產生的灰塵中,而剩下的鍺則被轉化成鍺酸鹽,然後被硫酸淋溶,此時在爐渣中的鋅也被淋溶。在中和反應後,只有鋅留在溶液中,沉澱物中含有鍺及其他金屬。在用威爾茲冶鋅法(Waelz process)把沉澱物中的含鋅量減少後,而殘餘的威爾茲氧化物則接受第二次淋溶。此時從沉澱物中可得二氧化鍺,與氯氣或氯化氢反應後被轉化成四氯化鍺,由於它的沸點低,因此可用蒸餾法進行分離[49] :
- GeO2 + 4HCl → GeCl4 + 2H2O
- GeO2 + 2Cl2 → GeCl4 + O2
四氯化鍺會被水解成二氧化鍺,或用分餾法淨化後再被水解[49]。極純的GeO2適用於製造鍺玻璃。純二氧化鍺與氫反應後被還原成鍺,用這種還原方式所得的鍺,適用於紅外線光學或半導體工業:
- GeO2 + 4H2 → Ge + 2H2O
用於鋼鐵生產及其他工業過程的鍺,一般會用碳來還原[51]:
- GeO2 + C → Ge + CO2
應用
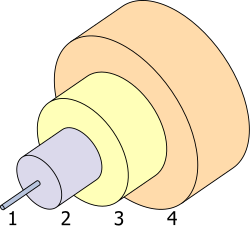
1. 核心 8 µm
2. 包層 125 µm
3. 緩衝層 250 µm
4. 護套 400 µm
鍺在2007年的估計全球終端應用為:光纖系統佔35%,紅外線光學(infrared optics)佔30%,聚合催化劑佔15%,及電子和太陽能發電也佔15%[19]。餘下的5%為其他應用,如磷光體(phosphor)、冶金及化學治療[19]。
光學
二氧化鍺最值得注意的物理特性,就是它的高折射率,和低色散。因此特別適用於廣角鏡、顯微鏡和光纖核心[52][53]。它更取代了二氧化鈦,成為了二氧化硅光纖核心的摻雜物,這樣就不用再做後續熱處理,而這種處理會使光纖變得易碎[54]。在2002年末,光纖工業佔美國鍺用量的60%,但只佔全球用量不到10%[53]。鍺銻碲(GeSbTe)是一種相變合金,以其光學特性著稱,應用例子包括可重寫光碟[55]。
由於紅外線可以無損失的穿透鍺,因此它成了一種重要的紅外線光學材料,能很容易地被切割或打磨成鏡片及窗戶。它在紅外線光學中的一項重要應用,就是製作熱圖像照相機(thermal imaging camera)的鏡頭塗層。含鍺的這一種鏡頭用於波長為8至14微米的紅外線,這樣的紅外線可用於被動熱成像及熱點探測,因此能被應用於軍事、汽車夜視系統及消防[51]。這樣的鏡頭還能用於顯微鏡光譜儀,及其他需要極敏感紅外線探測的光學儀器[53]。鍺這種材料有着非常高的折射率(4.0),因此需要抗反射塗層。特別是類金剛石碳的抗反射塗層,這是一種特別堅硬的特殊塗層,其折射率為2.0,與鍺相若,而且會產生一層如鑽石堅硬的表面,足以面對戶外的各種嚴苛環境[56][57]。
電子工业
晶体管主要由锗和硅两种高纯度半导体制作,而锗晶体管(简称锗管)曾是晶体管时代早期(于40年代末开始)最重要的半导体产品,因为当时制作高纯硅和制造硅管的工艺都不够成熟。锗晶体管相比硅管,有B-E结压降低(锗管约0.2V,而硅管为0.6V左右)的优势,但是热稳定性较差,且响应速度的极限明显不如硅管。锗管的大规模应用大概持续到1970年左右,此后从发达国家开始逐渐淘汰,到1980年,几乎在全世界范围完全被硅管取代而退出电子工业[58]。然而,一些音响发烧友认为锗管具有独特的音色,相对于硅管的“冷硬”,锗管温暖醇厚的声音特性被一些玩家称为‘低压电子管’[59]因此一些生产于60年代的电声设备和零件至今受到部分玩家的追捧,一些音樂用的踏板效果器還在用鍺晶體管,因為這種效果器能產生早期搖滾特有的“模糊”音質,當中最有名的是Dallas Arbiter公司所生產的Fuzz Face效果器[60]。
後來电子材料界又燃起了对锗材料的兴趣,不过已不局限于纯锗晶体。鍺化硅合金(一般稱為“硅鍺”)正急速地成為一種重要的半導體材料,用於高速集成電路。使用了Si-SiGe接面的電路,由於這種接面的特性,而比只用Si的要快得多[61]。在無線通訊(wireless communication)裝置中,鍺化硅正開始取代砷化鎵[19]。有着高速特性的SiGe晶片,可以用硅晶片工業傳統的生產技巧,並以低廉的成本生產[19]。
隨著能源成本的上漲,使得太陽能板的經濟價值有所提高,而這也是鍺的一大潛在應用[19]。鍺是太空用高效多結光伏電池的晶圓基板。因為鍺的晶格常數(lattice constant)與砷化鎵相近,所以可以用鍺基板來製造砷化鎵太陽能電池[62]。火星探測漫遊者及數個人造衛星,都有使用鍺上三聯點砷化鎵電池[63]。
上鍺下絕緣體的基板,有望可以取代微型晶片中的硅[19]。其他電子應用還包括螢光燈的磷光體(phosphor)[23],及鍺基固態發光二極體[19]。
其他應用
在生產聚對苯二甲酸乙二酯的過程中,二氧化鍺還可以用於催化聚合作用[64]。這樣生產出來的成品耀度很高,所以在日本銷售的PET瓶子都專門選用這一種聚酯[64]。然而,美國不把鍺用作聚合催化劑[19]。由於二氧化硅與二氧化鍺相近,所以氣相色譜柱中的固定相二氧化硅,可用二氧化鍺來取代[65]。
近年,在貴金屬合金中加入鍺是愈來愈多。例如,在英幣標準銀(sterling silver)(含銀量達95%以上的合金)中加入鍺,就能減少火紋(firescale)、增加抗鏽色性(tarnish)及增加對析出硬化(precipitation hardening)的反應。有一種抗鏽色的銀合金,商標名叫Argentium,其含鍺量需達1.2%[19]。
高純度鍺單晶探測器,能準確地探測出輻射的來源,因此可用於機場保安系統[66]。鍺亦被用於晶體單光儀(crystal monochromator),這台儀器能生成單晶中子散射(neutron scattering)及同步X射線繞射所需的線性束。在中子及高能X射線的應用,鍺的反射性比硅優勝[67]。高純度的鍺晶體還被用於伽瑪光譜學(gamma spectroscopy)和探尋暗物質的探測器中[68]。
鍺的一些化合物對哺乳類動物沒甚麼毒性,可是對某些細菌則有着相當的毒性[21]。就因為這項特性,所以這些鍺化合物可用作化學治療劑[69]。
对生物的影响
一般認為鍺對動植物的健康並不重要。[70]由於鍺在礦石與碳質材料中是一種稀有元素,加上在商業應用中使用的量也不算多,所以它對自然並沒有甚麼影響[19]。
锗化合物被用于白血病与肺癌的替代療法[16],但沒有醫學實證證實鍺的好处,甚至有证据表明它们有害[70]。美國食品藥品監督管理局的研究結論認為,當鍺被用作膳食補充劑時“有可能危害人體健康”[38]。
锗本身不危险,但某些活泼的锗化合物有毒。[71]例如四氯化鍺及甲鍺烷,分別為液體及氣體,能對眼睛、皮膚、肺部及喉嚨造成很大的刺激[72]。有些锗化合物对哺乳动物的毒性低,但对细菌来说有毒。[21]
参见
注釋
參考資料
外部链接
| 维基共享资源中相关的多媒体资源:锗 |
- 元素锗在洛斯阿拉莫斯国家实验室的介紹(英文)
- EnvironmentalChemistry.com —— 锗(英文)
- 元素锗在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素锗在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 锗(英文)