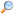Nátrium
A nátrium (nyelvújításkori magyar nevén szikeny) a periódusos rendszer egy kémiai eleme, vegyjele Na, rendszáma 11. Elemi állapotban ezüstös színű, lágy, jól nyújtható, igen reakcióképes könnyűfém. Az I. főcsoportba, az alkálifémek közé tartozik és a többi csoportbeli elemhez hasonlóan egyetlen elektron található a vegyértékhéján, melyet könnyedén lead pozitív töltésű kationt alkotva. Egyetlen stabil izotópja a 23Na. Reakcióképessége nagy, a vízzel rendkívül heves reakcióba lép, a levegő oxigénjével érintkezve gyorsan oxidálódik, ezért inert körülmények között kell tárolni. Nagy reakciókészsége miatt a természetben nem fordul elő elemi állapotban, csak vegyületeiben. A földkéreg hatodik leggyakoribb eleme, számos ásványban megtalálható, például földpátokban, szodalitben, vagy a kősóban. Égetéskor a lángot sárgára festi. Elemi nátriumot először 1807-ben Humphry Davy állított elő nátrium-hidroxid elektrolízisével.
Története

A nátrium egyik vegyületét, a szódát (Na2CO3) már régóta ismerték a vegyészek. Humphry Davy 1808-ban jelentette be, hogy a szódából nyert marónátron (NaOH) elektrolízise során sikerült elemi nátriumot előállítania. Az angolok mind a mai napig Davy elnevezését használják, amely a szóda angol megfelelőjéből képzett sodium. A nátrium elnevezése Klaprothtól származik, aki az egyiptomi-mezopotámiai eredetű nátron (neter = szóda) szóból képezte.
Tulajdonságai

A nátrium késsel vágható, puha, könnyű, vágási felületén ezüstfehér színű nagyon reakcióképes fém, jó elektromos vezető. Reakciókészségének köszönhetően a természetben elemi állapotban nem, csak vegyületeiben fordul elő. Az elemi nátrium és vegyületei a Bunsen-égő lángjába tartva a lángot sárgára színezi. A vízbe dobott nátrium, a víz tetején gyorsan keringve, heves hidrogéngáz (H2) képződéssel járó reakció során (mely az exoterm reakció során fejlődő hőtől meggyullad) maró tulajdonságú nátrium-hidroxiddá alakul. A kísérlet elvégzésénél ez a heves „úszkálás” látható, ami egyébként az első csoport elemeire jellemző (a hidrogént kivéve ).
A legtöbb anyagnak a légkörinél nagyobb nyomáson magasabb az olvadáspontja, mint normál légnyomás esetén. Ez azzal magyarázható, hogy az őket alkotó atomok közelebb kerülnek egymáshoz, és kevesebb helyük marad a mozgáshoz. A nátriumnál ettől eltérő jelenség figyelhető meg. 30 GPa nyomásnál (a légköri nyomás 300 000-szerese) a nátrium olvadáspontja csökkenni kezd. 100 GPa nyomásnál pedig már szobahőmérsékleten megolvad.
E szokatlan viselkedés egyik lehetséges magyarázata a következő: a nátrium atom külső elektronhéján található elektron a nagy nyomás hatására a lezárt héjakon található többi elektron közelébe kerül. Ez olyan kölcsönhatásokat vált ki, melyek normál körülmények között nem játszódnak le. Amíg nagy nyomás alatt a szilárd halmazállapotú nátrium kristályos tulajdonságokat mutat, a folyékony halmazállapotú szokatlan tulajdonságokkal rendelkezik: szupravezetővé válik.[forrás?]
Előfordulása, előállítása, vegyületei
A nátrium a csillagok egyik gyakori alkotóeleme. A csillagok emissziós színképeinek elemzésekor szinte mindig megtalálható a nátrium által kibocsátott D színképvonal.
A Föld tömegének mintegy 2,6%-át adja, és így a 6. leggyakrabban előforduló elem (az alkálifémek közül pedig az első). Legközönségesebb vegyülete a konyhasó, ami a tengerekben hozzávetőleg 3%-os koncentrációban található. Nagy mennyiségben található a sóbányákban (például Máramarossziget környékén, vagy a lengyelországi Wieliczkában).
A 19. század végén a szóda és szén 1100 °C-on történő hevítésével állították elő.
- Nátrium-karbonát reakciója szénnel, elemi nátrium képződése és szén-monoxid fejlődése közben. /egyensúlyi folyamat/
Manapság nátrium-klorid (NaCl) olvadékának elektrolízisével állítják elő. A nátrium-kloridot kalcium-kloriddal (CaCl2) keverik össze, így a keverék olvadáspontja lényegesen alacsonyabb lesz a tiszta nátrium-kloridénál (700 °C alatt). A katódon kiválik a tiszta elemi nátrium. Ez az eljárás jóval olcsóbb, mint a nátrium-hidroxid elektrolízise.
Gyakoribb vegyületei: lásd A nátrium vegyületei
Felhasználása
- szappangyártáshoz
- világítástechnikában: nátriumgőzlámpa
- fémolvadékok tisztításához
- hőelvezető folyadékként nukleáris erőművekben, és csúcsteljesítményű belsőégésű motorokban
- redukálószer más könnyen oxidálódó fémek előállítására (alumínium (Al))
Élettani tulajdonságai
Az emberi szervezetben körülbelül 80-100 gramm nátrium található. Nagyobb része oldott állapotban van, kisebb részét pedig a csontok, kötőszövetek raktározzák. A nátrium – szorosan összefüggve a káliummal (K) – az úgynevezett ozmotikus nyomás fenntartásában fontos szerepet játszik. Ugyanilyen elengedhetetlen az idegrendszeri ingerületek átvitelénél is.
Izotópjai
20 izotópja ismert. Ezek közül csak a 23-as tömegszámú stabil.
A két legjelentősebb kozmogén radioaktív izotópja:
- 22Na, felezési ideje 2,602 év
- 24Na, felezési ideje 15 óra
Az erős neutronsugárzás (például nukleáris baleset esetén) a vérplazmában előforduló 23Na-ot 24Na izotóppá alakítja.
A 24Na izotóp koncentrációjából megállapítható az elszenvedett sugárzás mértéke.
Óvintézkedések
Ahogy más alkálifémek, úgy a nátrium is elemi formában erősen gyúlékony és kismértékben robbanásveszélyes amikor vízzel érintkezik. Tárolása kémiailag kevéssé reakcióképes folyékony szénhidrogén, például petróleum alatt történik.Ártalmatlanítása metanollal vagy etanollal történik.
Jegyzetek
Források
- www.webelements.com
- A kémia története (Dr. Balázs Lóránt, Nemzeti Tankönyvkiadó)
Kapcsolódó szócikkek
További információk
- a magyar Wikipédia nátriumot tartalmazó vegyületeinek listája belső lapon és külső keresővel